Clear Sky Science · fr
Les cellules de glioblastome qui échappent à la mort induite par la chimioradiothérapie présentent un programme glycolytique bifurqué
Pourquoi cette étude sur le cancer du cerveau est importante
Le glioblastome est l’un des cancers du cerveau les plus meurtriers chez l’adulte et récidive presque toujours après chirurgie, chimiothérapie et radiothérapie. Cette étude pose une question cruciale : qu’ont de particulier le petit groupe de cellules tumorales qui survivent au traitement et relancent ensuite la maladie ? En suivant sur la durée la façon dont ces cellules gèrent le sucre, les chercheurs mettent au jour une stratégie de survie cachée qui pourrait expliquer l’échec fréquent des traitements actuels — et suggèrent de nouvelles façons de couper la « ligne de vie » du tumeur.
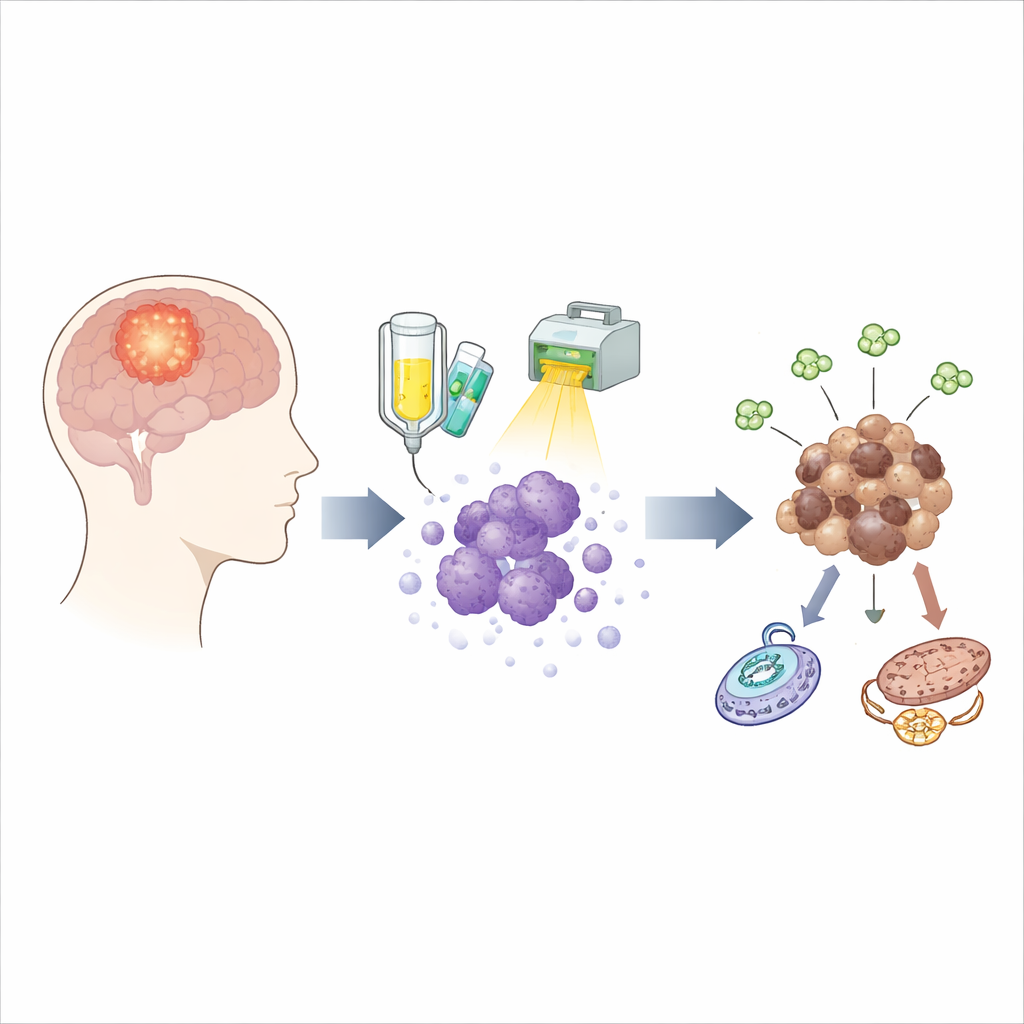
Les survivants dissimulés après le traitement
La prise en charge standard du glioblastome associe un médicament appelé témozolomide à la radiothérapie. Si cette combinaison élimine la majorité des cellules tumorales, une minorité tenace survit et peut engendrer une nouvelle tumeur des mois plus tard. Pour surprendre ces survivants en pleine action, l’équipe a utilisé des cellules tumorales prélevées directement chez dix patients différents et les a exposées à un schéma de traitement conçu pour reproduire fidèlement ce que reçoivent les patients en clinique. Ils ont prélevé des cellules vivantes à plusieurs moments pendant et après le traitement, et ont aussi étudié des tumeurs assorties implantées chez la souris, ce qui leur a permis de suivre l’évolution des survivants dans le temps plutôt que de simplement comparer tumeurs avant et après rechute.
Comment les cellules tumorales modifient leur utilisation du sucre
Le tissu cérébral consomme une part remarquable du sucre de l’organisme, et les cellules de glioblastome en sont particulièrement voraces. Les chercheurs ont constaté qu’au fur et à mesure du traitement, les cellules survivantes absorbaient encore plus de glucose de leur environnement. Pourtant, de manière surprenante, elles n’augmentaient pas simplement la fermentation de ce carburant. À l’inverse, ces cellules réduisaient leur production de lactate, le déchet typique d’une dégradation rapide du sucre dans le cancer. Les mesures des protéines clés ont révélé un schéma nettement scindé : les éléments qui importent le sucre dans la cellule et en initient la dégradation étaient augmentés, tandis que ceux intervenant dans les étapes ultérieures et la production de lactate diminuaient. Ce programme « bifurqué » signifie que le sucre entre et commence à être traité, mais que la voie usuelle menant au lactate est en partie fermée.
Rediriger le carburant vers les éléments de construction et les centrales énergétiques
Où va le sucre détourné ? En utilisant du glucose spécialement marqué et des mesures avancées de métabolites, l’équipe a montré que les cellules survivantes détournent une grande partie de ce carbone vers deux destinations principales. La première est une voie annexe appelée voie des pentoses phosphate, qui génère les matières premières nécessaires à la fabrication des blocs d’ADN et d’ARN. Dans ces cellules, de nombreux composants nucléotidiques et gènes associés étaient renforcés, suggérant une impulsion forte vers la reconstruction et la préparation d’une reprise de croissance. La seconde destination concerne les centrales énergétiques de la cellule, les mitochondries. Les enzymes du cycle énergétique mitochondrial augmentaient, et des travaux antérieurs du même groupe avaient montré une plus grande importation de carburant issu du glucose vers ces structures. Ensemble, cela révèle un réaménagement coordonné : moins de fermentation gaspilleuse en lactate, plus d’investissement dans la réparation, les matériaux de croissance et une production d’énergie plus flexible.
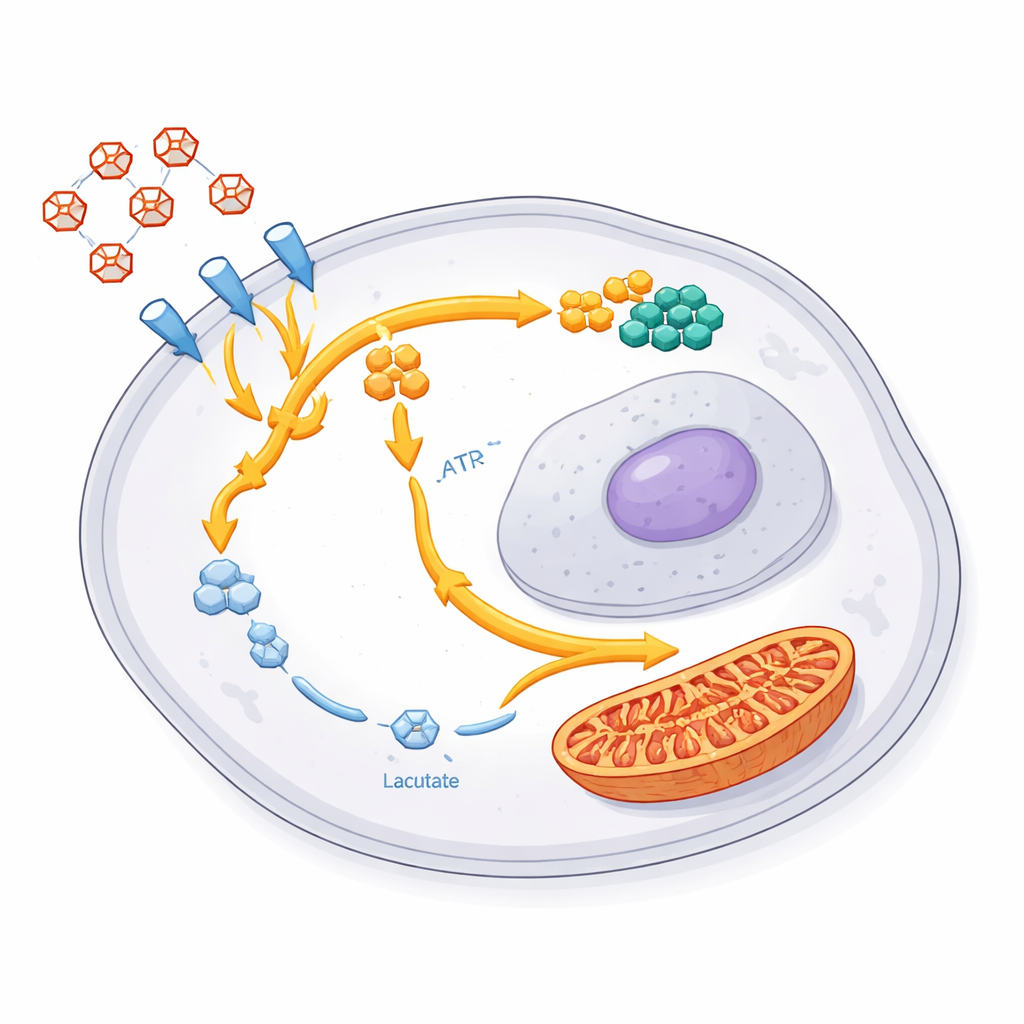
Une stratégie de survie commune aux tumeurs et aux modèles animaux
Les tumeurs de glioblastome varient fortement d’un patient à l’autre, ce qui compromet souvent les traitements universels. Malgré cette diversité, chacun des dix modèles dérivés de patients a montré le même changement de base après chimioradiothérapie : augmentation des premières étapes du traitement du sucre, diminution des étapes tardives et de la production de lactate, et activité mitochondriale accrue. Fait important, la même signature est apparue dans des tumeurs cérébrales de souris issues de cellules de patients et traitées par des versions adaptées de la thérapie standard. Les tumeurs récurrentes chez ces animaux présentaient toujours le programme sucré altéré, indiquant qu’il ne s’agit pas d’un effet transitoire mais d’un trait stable des cellules qui survivent au traitement et reconstruisent la tumeur.
Ce que cela signifie pour les traitements futurs
Pour un non-spécialiste, le message central est que les cellules de glioblastome survivantes ne se contentent pas de « se cacher » du traitement ; elles reprogramment activement leur usage du sucre pour rester en vie. Elles importent davantage de glucose, évitent de le transformer en déchet et le canalisent vers la fabrication des blocs d’ADN et l’alimentation des mitochondries — les aidant ainsi à réparer les dégâts, à maintenir un état flexible proche de celui de cellules souches, et finalement à regénérer la tumeur. En révélant cet état métabolique de survie partagé, l’étude ouvre des pistes thérapeutiques : cibler les étapes précoces du traitement du glucose, la voie annexe de synthèse des nucléotides ou la dépendance mitochondriale de ces cellules pourrait rendre la chimioradiothérapie standard plus complète et laisser moins d’échappées pour relancer la maladie.
Citation: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
Mots-clés: glioblastome, métabolisme du cancer, utilisation du glucose, résistance aux traitements, voie des pentoses phosphate