Clear Sky Science · fr
La LAM332 produite par les CAF favorise la formation et la survie des CTC via ITGA3 et contribue aux métastases de l’adénocarcinome canalaire pancréatique
Pourquoi cette recherche importe pour les patients
Le cancer du pancréas est réputé pour se disséminer tôt et de façon silencieuse, laissant souvent peu d’options thérapeutiques aux patients au moment du diagnostic. Cette étude examine l’une des étapes les plus dangereuses de cette dissémination : la façon dont les cellules cancéreuses se détachent de la tumeur primaire, survivent dans la circulation sanguine et implantent de nouvelles tumeurs dans des organes comme le foie et les poumons. En révélant une « conversation » spécifique entre les cellules tumorales et leurs cellules de soutien environnantes, les auteurs identifient de nouvelles voies pour prédire, et potentiellement bloquer, des métastases mortelles.
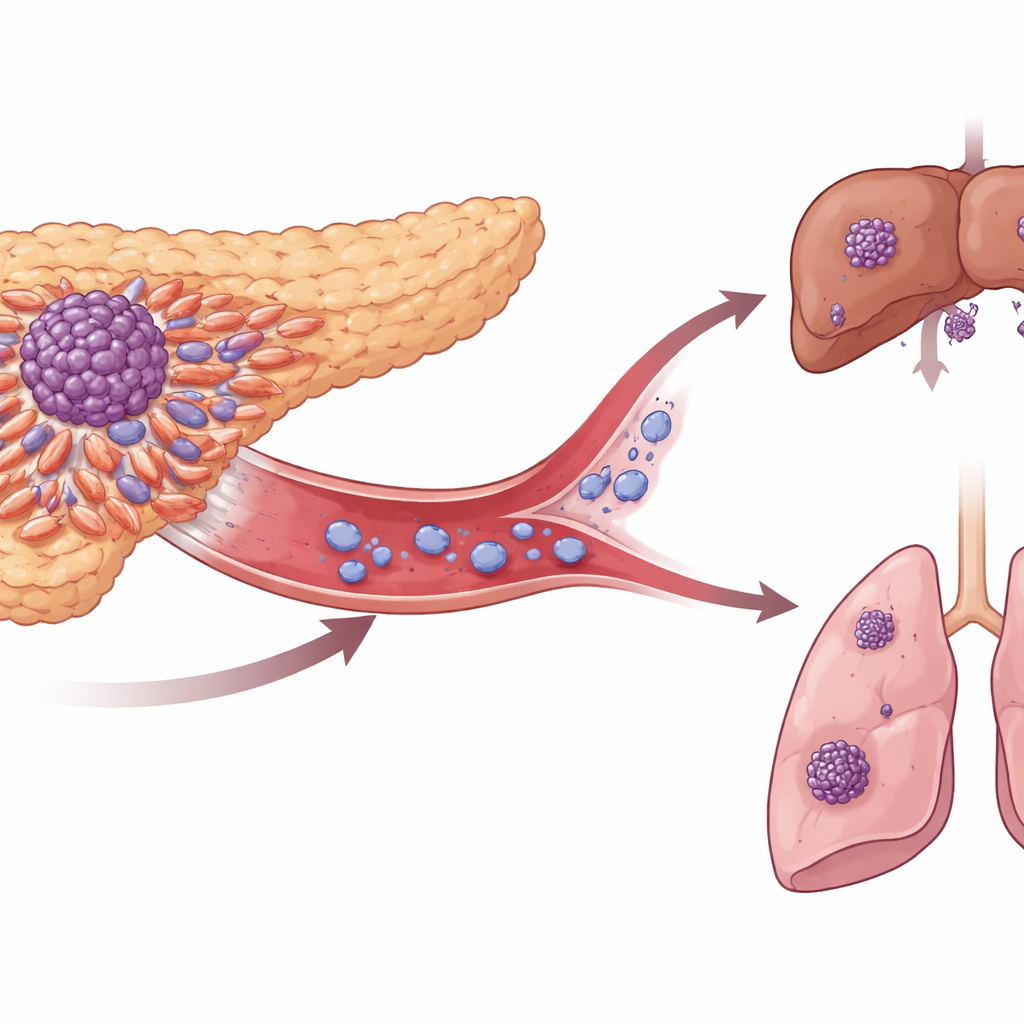
Voyageurs cachés dans le sang
Lorsque les tumeurs pancréatiques se propagent, elles le font via des cellules tumorales circulantes — des cellules dissidentes qui s’échappent dans le sang. L’équipe a analysé des échantillons tumoraux et de larges jeux de données génétiques et protéiques provenant de patients avec et sans ces cellules dans leurs vaisseaux, ainsi que de patients présentant une maladie localisée versus métastatique. Ils ont retrouvé de façon répétée une molécule de surface, appelée ITGA3, qui se distinguait. Les tumeurs et les cellules circulantes exprimant davantage ITGA3 étaient plus fréquentes dans les cancers avancés, en particulier au niveau du bord invasif de la tumeur où les cellules se détachent en premier. Les patients dont la tumeur exprimait davantage ITGA3 avaient tendance à présenter plus de cellules tumorales circulantes, des caractéristiques plus agressives comme l’invasion des tissus et des vaisseaux voisins, et une survie plus courte.
Comment les cellules tumorales acquièrent la capacité de se libérer
Pour comprendre ce que fait réellement ITGA3, les chercheurs ont modifié son expression dans des lignées cellulaires de cancer du pancréas et implanté ces cellules chez la souris. Lorsque ITGA3 était réduit, les cellules cancéreuses croissaient plus lentement, se déplaçaient moins et étaient moins capables de dégrader le tissu environnant. Les cellules retournaient également vers un état plus ordonné, « épithélial », retrouvant des contacts cellulaires serrés et perdant les traits flexibles et migratoires qui favorisent l’évasion. Chez la souris, les tumeurs dépourvues d’ITGA3 étaient plus petites et montraient moins de signes de comportement invasif. Ces résultats suggèrent qu’ITGA3 agit comme un interrupteur clé qui aide les cellules tumorales à se détacher de la masse principale, pénétrer dans les vaisseaux sanguins et commencer leur voyage en tant que cellules tumorales circulantes.
Agression collective pour survivre au voyage
La vie dans la circulation sanguine est rude pour les cellules cancéreuses isolées, mais les amas de cellules tumorales semblent mieux survivre et donner des métastases. L’étude a montré qu’ITGA3 est particulièrement abondant sur les cellules au sein de tels amas. Dans des expériences en culture conçues pour empêcher les cellules d’adhérer au plastique, les cellules cancéreuses exprimant ITGA3 formaient facilement des amas compacts et résistaient à la mort cellulaire, tandis que les cellules sans ITGA3 restaient principalement isolées et mouraient plus facilement. Dans des modèles murins où les tumeurs se développaient dans le pancréas, la perte d’ITGA3 entraînait moins d’amas circulants, moins de colonies métastatiques au foie et aux poumons, et une charge métastatique distante globale plus faible. Cela montre qu’ITGA3 aide non seulement les cellules à se détacher, mais aussi à s’agréger et à supporter les conditions hostiles du sang.
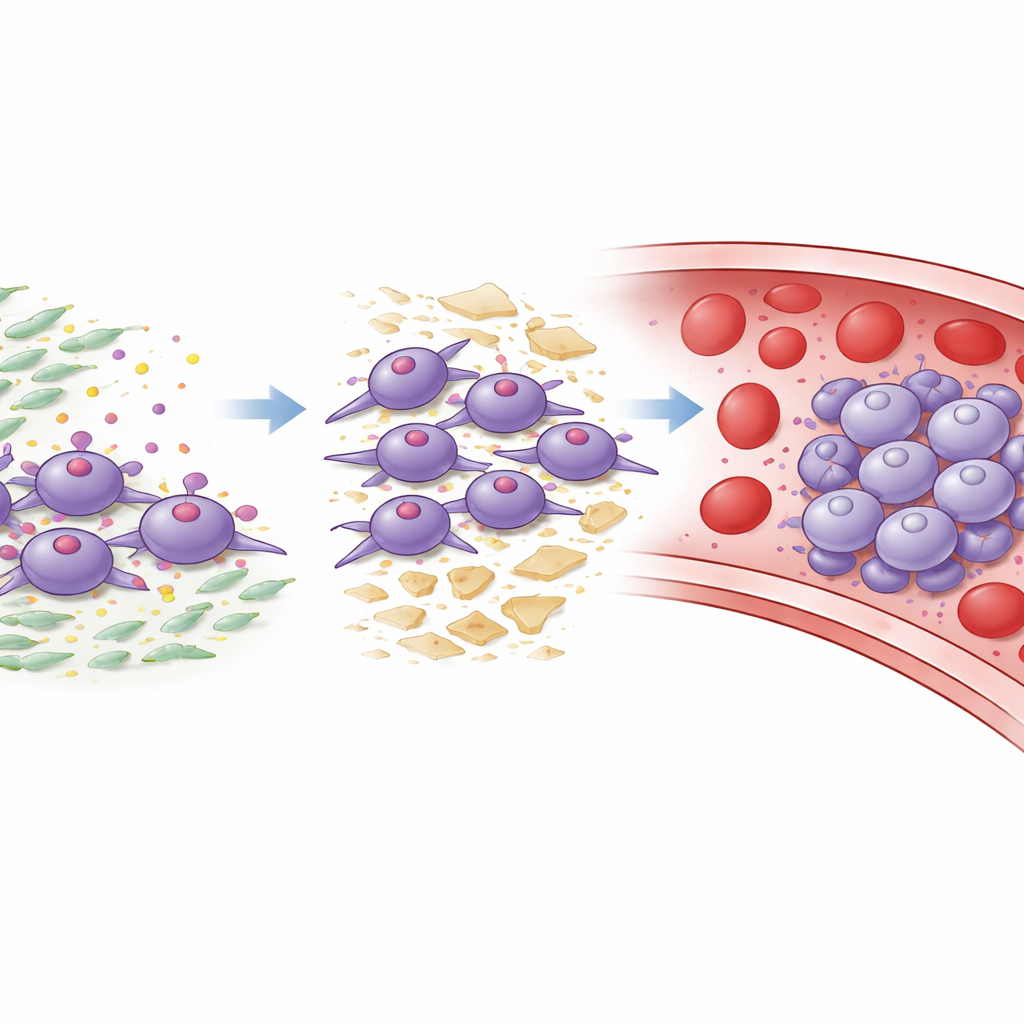
Le rôle des cellules stromales de soutien
Les tumeurs pancréatiques sont riches en fibroblastes associés au cancer, un type de cellule de soutien qui construit et remanie l’échafaudage tissulaire autour de la tumeur. Les auteurs ont découvert que ces fibroblastes sont une source majeure d’une protéine adhésive appelée laminine-332. Les cellules tumorales exprimant ITGA3 l’utilisent comme point d’ancrage pour la laminine-332. Dans des expériences cellulaires et animales, la liaison de la laminine-332 à ITGA3 déclenchait des signaux à l’intérieur des cellules tumorales qui augmentaient la croissance, la mobilité, l’invasion tissulaire et la transition vers un état plus mobile et agressif. Elle favorisait aussi l’agrégation et réduisait la mort cellulaire lorsque les cellules étaient en suspension, mimant les conditions de la circulation. Bloquer la laminine-332 par des anticorps, ou perturber ITGA3 ou ses partenaires de signalisation en aval, inversait en grande partie ces comportements malins et réduisait les métastases chez la souris.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, les travaux décrivent une chaîne d’événements claire : les fibroblastes dans et autour des tumeurs pancréatiques libèrent la laminine-332 ; cette protéine se fixe à ITGA3 sur les cellules tumorales ; le signal qui en résulte aide les cellules à se détacher, à se regrouper en amas protecteurs, à survivre dans la circulation et à coloniser des organes distants. Pour un non-spécialiste, le message clé est que les chercheurs ont cartographié une « ligne d’approvisionnement » spécifique que les tumeurs utilisent pour lancer et protéger leurs cellules disséminées. Parce que cette voie dépend de composants présents principalement dans la tumeur et son stroma, elle constitue une cible attractive pour de nouvelles thérapies. Des médicaments ou des anticorps qui bloquent la laminine-332, ITGA3 ou les signaux qu’ils déclenchent pourraient réduire le nombre et la résistance des cellules tumorales circulantes, ralentissant ou empêchant potentiellement les métastases mortelles du cancer du pancréas.
Citation: Tang, H., Shi, W., Tan, S. et al. CAFs-derived LAM332 promotes CTCs formation and survival via ITGA3 and contributes to the metastasis of pancreatic ductal adenocarcinoma. Cell Death Dis 17, 369 (2026). https://doi.org/10.1038/s41419-026-08642-z
Mots-clés: cancer du pancréas, métastase, cellules tumorales circulantes, microenvironnement tumoral, fibroblastes associés au cancer