Clear Sky Science · fr
L’axe DAG/PKC/CREB1/TGF-β1 conduit la rigidité mesurée par l’élastographie par ondes de cisaillement et la progression maligne dans le cancer du sein triple négatif via le reprogrammation du métabolisme lipidique
Pourquoi la rigidité tumorale compte
Les cliniciens ont depuis longtemps remarqué que certaines tumeurs mammaires sont plus dures que d’autres, et que cette rigidité signale souvent un cancer plus dangereux. Dans le cancer du sein triple négatif, une forme agressive dépourvue des cibles thérapeutiques classiques, l’obésité semble durcir les tumeurs et augmenter leur propension à se disséminer. Cette étude explique comment des changements du métabolisme lipidique chez les patientes obèses rigidifient les tumeurs et montre qu’une technique d’échographie spécialisée, l’élastographie par ondes de cisaillement, peut détecter cette rigidité depuis l’extérieur et en offrir une fenêtre sur le comportement tumoral.
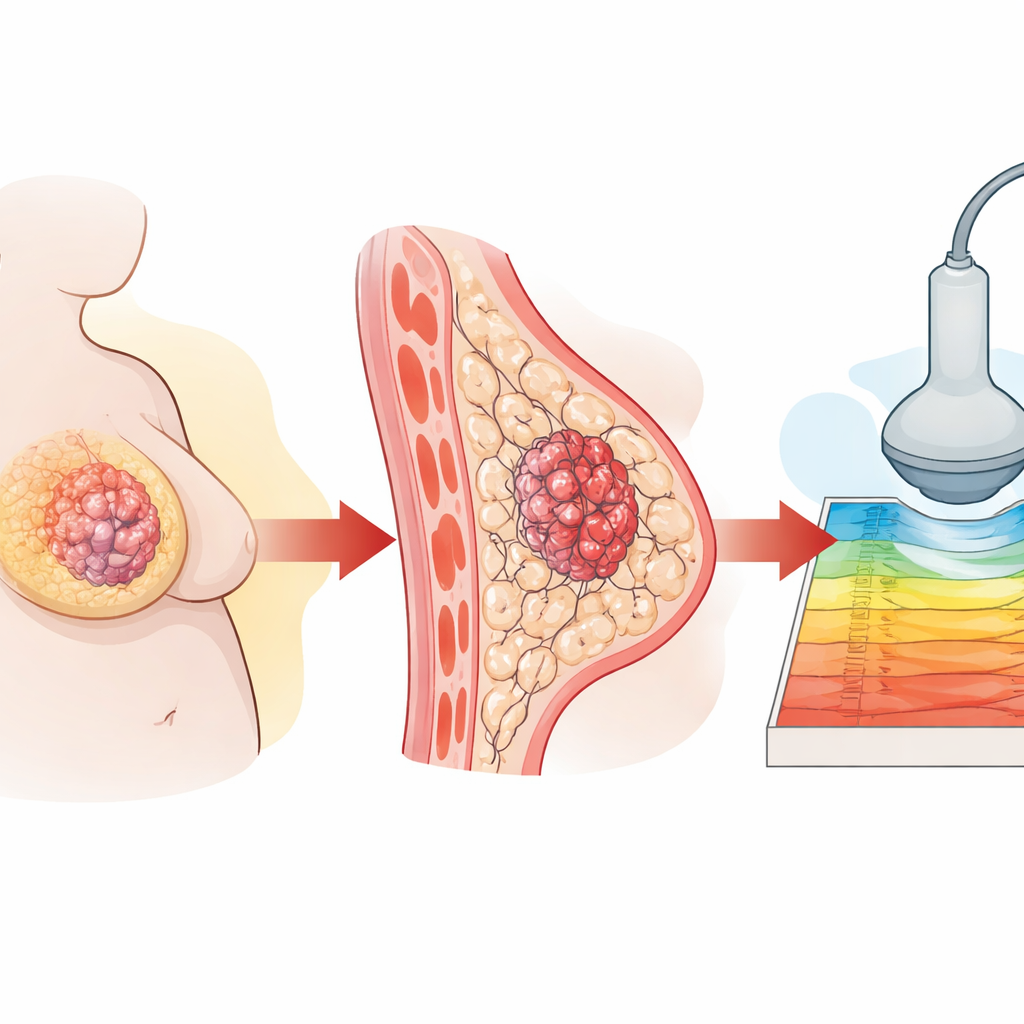
Poids corporel et risque tumoral
Les chercheurs ont commencé par suivre 147 femmes atteintes d’un cancer du sein triple négatif dans un centre anticancéreux majeur de Shanghai. Ils ont constaté que les femmes ayant un indice de masse corporelle (IMC) plus élevé présentaient de moins bons résultats à long terme, notamment davantage de récidives et de décès. En examinant les échographies, ils ont observé que les tumeurs chez les patientes plus lourdes étaient systématiquement plus rigides à l’élastographie par ondes de cisaillement, même si les images échographiques en niveaux de gris semblaient similaires. Les prélèvements tissulaires ont confirmé que les tumeurs des patientes en surpoids contenaient plus de collagène et un plus grand nombre de cellules en division active, deux signes d’un microenvironnement plus hostile.
Du régime aux tumeurs plus dures
Pour explorer la causalité, l’équipe s’est tournée vers des modèles murins, nourrissant certains animaux avec un régime riche en graisses et d’autres avec un régime normal avant d’implanter des tumeurs triple négatives. Les souris soumises au régime riche en graisses ont pris plus de poids, développé des tumeurs plus volumineuses et, fait crucial, ont montré une augmentation continue de la rigidité mesurée par élastographie au fil du temps. L’examen microscopique a révélé des réseaux de collagène plus denses, des fibroblastes activatés plus nombreux et des niveaux plus élevés d’une enzyme qui réticulise le collagène, autant d’éléments rendant les tissus plus rigides. Parallèlement, les cellules tumorales provenant des souris obèses affichaient des signes d’un métabolisme lipidique stimulé et accumulaient davantage de gouttelettes lipidiques intracellulaires.
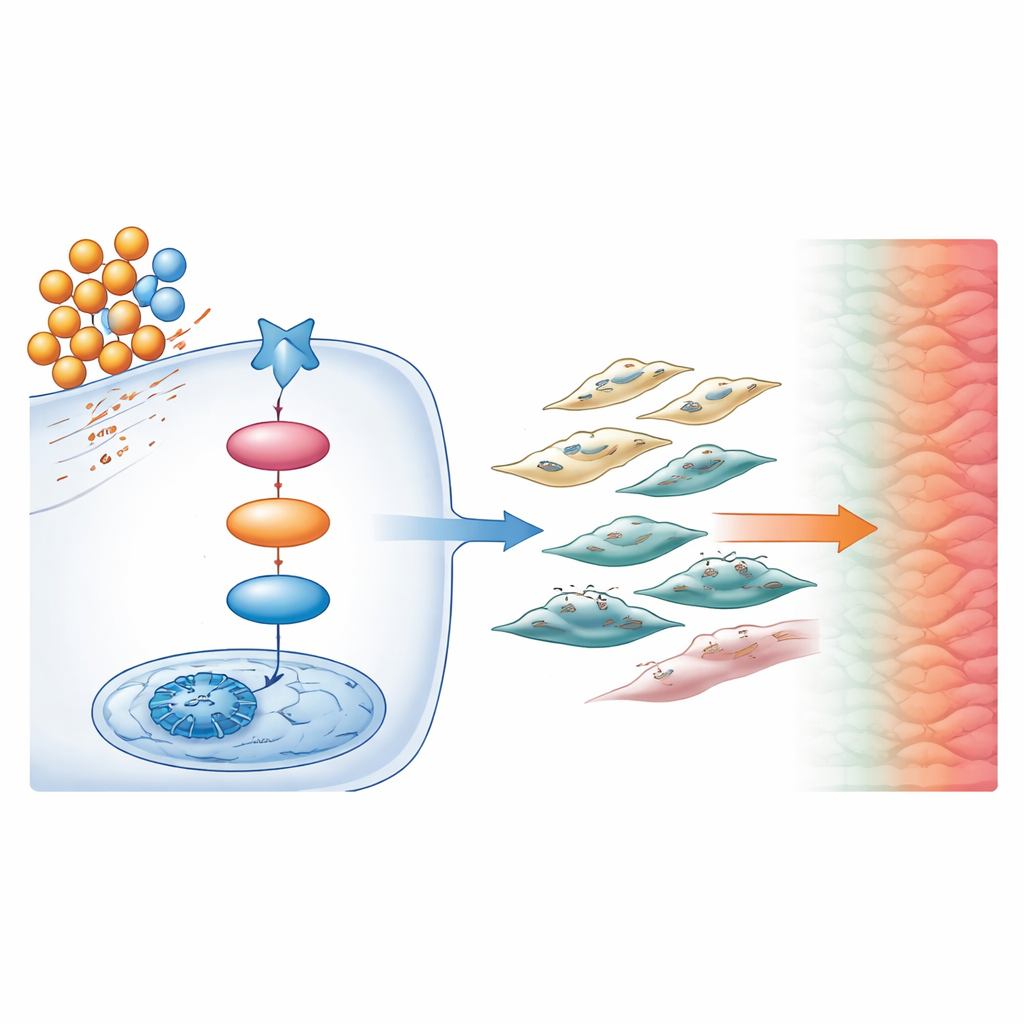
Une réaction chimique en chaîne cachée
En creusant davantage, les scientifiques ont utilisé le profilage lipidique et l’analyse de l’activité génique pour cartographier la chaîne moléculaire à l’origine de ces changements. Ils ont trouvé qu’une molécule lipidique particulière, le diacylglycérol (DAG), était élevée dans les tumeurs des souris obèses. Le DAG agissait comme un interrupteur biochimique, activant une protéine appelée PKC à l’intérieur des cellules cancéreuses. PKC augmentait à son tour l’activité d’un régulateur majeur, CREB1, dans le noyau cellulaire. Une fois activé, CREB1 stimulait la production de TGF-β1, une puissante molécule de signalisation connue pour favoriser la fibrose et la dissémination tumorale. Ensemble, cette séquence DAG → PKC → CREB1 → TGF-β1 forme une voie centrale reliant l’excès lipidique à une tumeur plus rigide et plus invasive.
Une conversation vicieuse entre cellules
TGF-β1 n’agissait pas seulement sur les cellules cancéreuses. Il activait également les fibroblastes environnants, les cellules structurelles qui construisent et remodèlent la trame tissulaire autour des tumeurs. Exposés aux signaux émis par les cellules cancéreuses stimulées par le DAG, les fibroblastes basculaient vers un état hautement actif, déposant du collagène supplémentaire et resserrant encore l’environnement tumoral. Ces fibroblastes activés renvoyaient à leur tour des signaux aux cellules cancéreuses augmentant leur métabolisme lipidique, leur prolifération et leur pouvoir invasif. Dans les modèles murins, cet échange réciproque créait une boucle auto‑entretenue qui rendait les tumeurs plus rigides à l’élastographie par ondes de cisaillement, plus fibreuses au microscope et plus susceptibles de former des métastases à distance.
Transformer les images en indications thérapeutiques
En combinant données cliniques, expérimentations animales et études moléculaires détaillées, les auteurs montrent que la rigidité mesurée par élastographie par ondes de cisaillement est plus qu’une curiosité structurelle : elle reflète l’activation d’une boucle de signalisation spécifique, pilotée par les lipides, qui aggrave le cancer du sein triple négatif. Pour le grand public, cela signifie qu’une mesure échographique non invasive de la « dureté » d’une tumeur peut révéler dans quelle mesure cette voie néfaste est activée. À l’avenir, les patientes avec un IMC élevé et des tumeurs très rigides à l’élastographie pourraient être identifiées comme à haut risque et envisagées pour des traitements ciblant la PKC, CREB1, TGF-β1 ou d’autres étapes de la boucle, transformant un simple signal d’imagerie en un guide pour des prises en charge plus précises et fondées sur la biologie.
Citation: Wang, S., Zheng, D., Wang, Z. et al. The DAG/PKC/CREB1/TGF-β1 axis drives shear-wave elastography stiffness and malignant progression in triple-negative breast cancer via lipid metabolic reprogramming. Cell Death Dis 17, 327 (2026). https://doi.org/10.1038/s41419-026-08625-0
Mots-clés: cancer du sein triple négatif, rigidité tumorale, obésité, métabolisme des lipides, élastographie par ondes de cisaillement