Clear Sky Science · fr
L’AATF soutient la prolifération des cellules de glioblastome en maintenant la respiration mitochondriale via un mécanisme dépendant de NRF-1
Pourquoi la consommation d’énergie des tumeurs cérébrales compte
Le glioblastome est la forme la plus agressive de cancer cérébral chez l’adulte et, malgré la chirurgie, la radiothérapie et la chimiothérapie, la plupart des patients survivent à peine plus d’un an. Cette étude pose une question apparemment simple mais aux conséquences étendues : comment les cellules de glioblastome alimentent-elles leur croissance implacable, et peut-on couper cette source d’énergie ? Les auteurs se concentrent sur une protéine régulatrice peu connue, appelée AATF, et montrent qu’elle aide les cellules tumorales à maintenir leurs centrales énergétiques — les mitochondries — à plein régime. Comprendre ce système de soutien caché pourrait ouvrir de nouvelles voies pour ralentir ou stopper ces tumeurs mortelles.
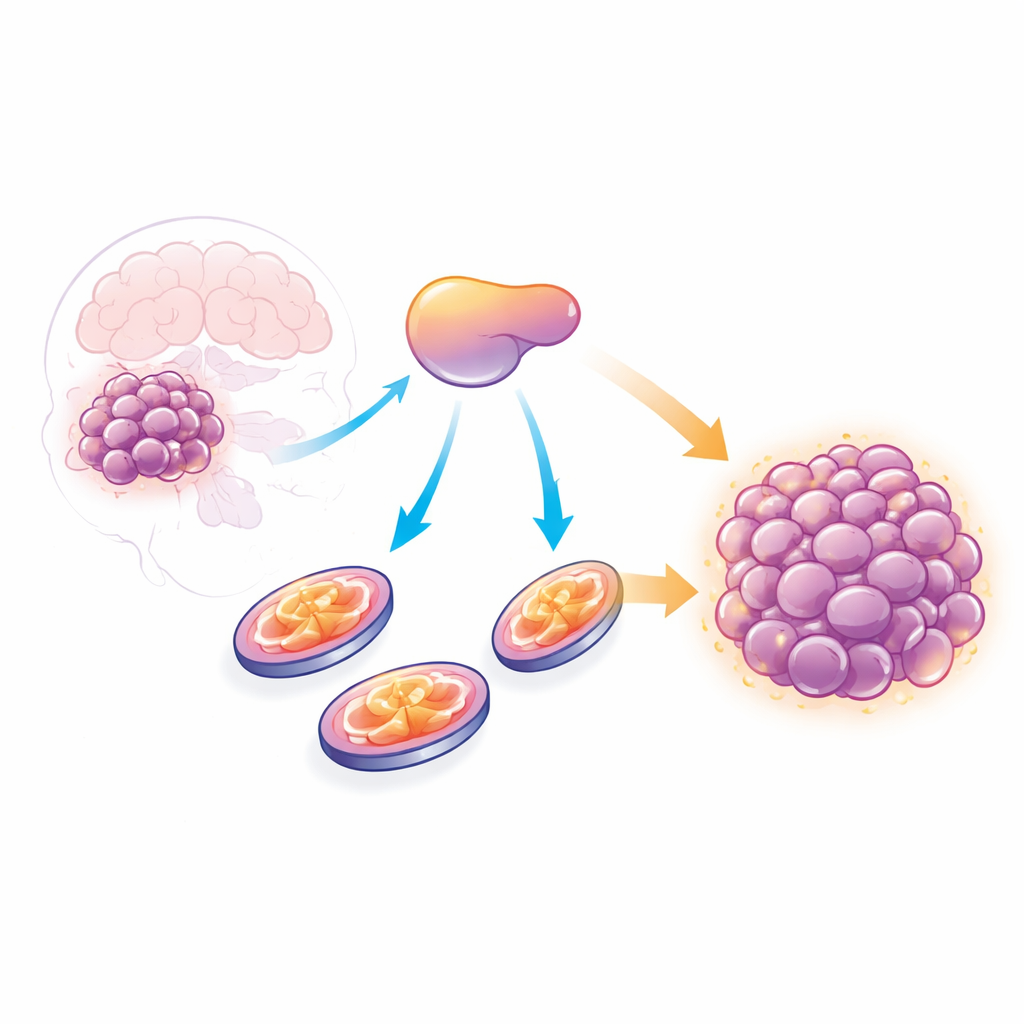
Un auxiliaire caché de la croissance tumorale
Les cellules cancéreuses s’appuient souvent sur une stratégie de combustion du glucose appelée glycolyse, longtemps considérée comme leur voie énergétique emblématique. Pourtant, des travaux récents ont révélé que de nombreuses tumeurs, y compris le glioblastome, dépendent également fortement des mitochondries, qui produisent de l’énergie via la phosphorylation oxydative (OXPHOS). En analysant de larges jeux de données de patients, les chercheurs ont constaté que les niveaux d’AATF sont plus élevés dans les tissus de glioblastome que dans le cerveau normal et augmentent avec le grade tumoral. Les patients dont les tumeurs exprimaient davantage d’AATF avaient tendance à avoir une survie plus courte, ce qui suggère que cette protéine est liée à une maladie plus agressive.
Bloquer l’AATF ralentit les cellules cancéreuses
Pour vérifier si l’AATF est simplement un marqueur ou un moteur actif de la croissance, l’équipe a réduit son expression dans plusieurs lignées cellulaires de glioblastome en utilisant des outils à base d’ARN et l’interférence CRISPR. Les cellules privées d’AATF se sont multipliées beaucoup plus lentement, se sont accumulées en phase de repos du cycle cellulaire et ont formé beaucoup moins de colonies à long terme. Fait important, ce ralentissement s’est produit sans déclencher une mort cellulaire massive ni un vieillissement prématuré (sénescence), ce qui signifie que les cellules étaient vivantes mais bloquées. Lorsque des cellules appauvries en AATF ont été implantées chez la souris, les tumeurs résultantes étaient beaucoup plus petites et présentaient moins de cellules en division, confirmant que l’AATF est nécessaire à une croissance tumorale robuste in vivo.
Reconfigurer le réseau énergétique tumoral
Étant donné que l’AATF influence l’activité génique, les auteurs ont examiné comment sa perte reconfigure le programme génétique de la cellule. Le séquençage de l’ARN a révélé que des centaines de gènes modifiaient leur activité lorsque l’AATF était silencée. Parmi les plus systématiquement réduits figuraient des gènes codant des composants clés de la machinerie OXPHOS mitochondriale. Les mesures protéiques ont confirmé que plusieurs éléments des complexes producteur d’énergie à l’intérieur des mitochondries étaient diminués. Lorsque les chercheurs ont mesuré directement la consommation d’oxygène et la production d’énergie, les cellules sans AATF présentaient une respiration plus faible et des niveaux d’ATP réduits. Parallèlement, leurs mitochondries produisaient plus d’espèces réactives de l’oxygène, adoptaient une morphologie fragmentée en anneaux associée à un dysfonctionnement, et surexprimaient des gènes favorisant la fission mitochondriale, autant de signes d’un réseau énergétique stressé et compromis.
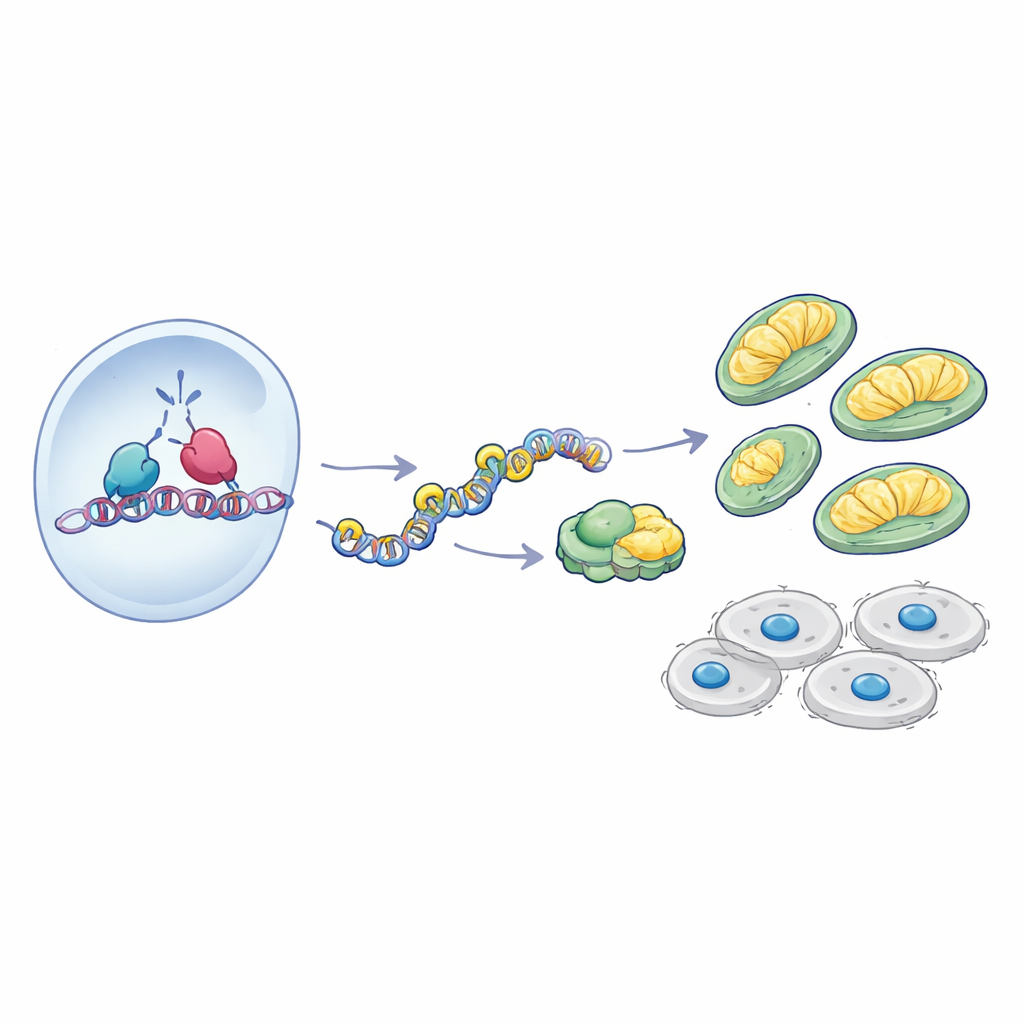
Un partenariat au niveau de l’ADN
Comment l’AATF exerce-t-elle un tel contrôle sur les gènes mitochondriaux ? L’étude s’est focalisée sur NRF-1, un facteur de transcription déjà connu comme régulateur maître de la biogenèse mitochondriale et de l’OXPHOS. Les données patients montrent que les niveaux d’AATF et de NRF-1 varient de concert dans le glioblastome, et des expériences en lignées cellulaires ont révélé que les deux protéines interagissent physiquement. Par immunoprécipitation de la chromatine, les auteurs ont démontré que l’AATF est présente aux régions promotrices de plusieurs gènes OXPHOS, précisément aux sites où NRF-1 se lie. Lorsque NRF-1 a été réduit, la liaison de l’AATF à ces promoteurs a fortement diminué, indiquant que NRF-1 contribue au recrutement de l’AATF sur l’ADN. De plus, dans les cellules dépourvues d’AATF, NRF-1 pouvait encore se lier à l’ADN, mais le recrutement de l’enzyme de transcription ARN polymérase II était altéré et la chromatine environnante devenait plus condensée, avec moins de marques d’histones activatrices et davantage de marques répressives. En substance, sans AATF, NRF-1 reste sur les interrupteurs, mais les lumières ne s’allument pas.
Ce que cela signifie pour les traitements futurs
Pour un non-spécialiste, le message est que les cellules de glioblastome utilisent un partenariat spécialisé entre AATF et NRF-1 pour maintenir leurs moteurs mitochondriaux à haute puissance, fournissant l’énergie nécessaire à la division rapide et à la résistance aux traitements. L’AATF agit comme un copilote sur les gènes mitochondriaux, modelant l’environnement local de l’ADN pour que NRF-1 puisse stimuler fortement l’expression des composants de l’OXPHOS. La suppression de l’AATF bloque ce système : les mitochondries faiblissent, des sous-produits dommageables s’accumulent et les cellules tumorales perdent leur avantage prolifératif en culture et chez la souris. Bien qu’il n’existe actuellement aucun médicament ciblant directement l’AATF, ce travail l’identifie comme une cible prometteuse dans le glioblastome et suggère que perturber l’axe AATF–NRF-1–mitochondries pourrait affaiblir l’approvisionnement énergétique de la tumeur et améliorer l’efficacité des thérapies existantes.
Citation: Sorino, C., Di Giovenale, S., Falcone, I. et al. AATF supports proliferation of glioblastoma cells by sustaining mitochondrial respiration through an NRF-1-dependent mechanism. Cell Death Dis 17, 349 (2026). https://doi.org/10.1038/s41419-026-08617-0
Mots-clés: glioblastome, respiration mitochondriale, phosphorylation oxydative, régulation transcriptionnelle, métabolisme du cancer