Clear Sky Science · fr
La transdifférenciation adipogénique reprogramme les cellules PDAC à EMT élevée en un état post-mitotique de type adipocyte et limite les métastases
Transformer des cellules cancéreuses agressives en graisse inoffensive
Le cancer du pancréas est l’un des plus meurtriers, en grande partie parce qu’il se propage tôt et résiste aux traitements conventionnels. Cette étude explore une idée résolument différente : au lieu d’essayer d’empoisonner ou d’affamer les cellules tumorales, et si l’on pouvait convaincre les cellules cancéreuses pancréatiques les plus dangereuses de se transformer en cellules de type adipeux qui ne se divisent plus et ne migrent plus dans l’organisme ? Les travaux décrivent comment les chercheurs ont poussé des cellules de cancer du pancréas très agressives vers un état stable proche des adipocytes, ce qui a ralenti la croissance tumorale et réduit la dissémination chez la souris, suggérant une nouvelle manière de contrôler cette maladie dévastatrice.
Pourquoi le cancer du pancréas est si difficile à arrêter
L’adénocarcinome canalaire pancréatique, la forme principale du cancer du pancréas, présente un pronostic très défavorable : seulement environ une personne sur huit est en vie cinq ans après le diagnostic. Une partie du problème tient au fait que de nombreuses cellules tumorales présentent un état plastique appelé EMT, qui les rend plus mobiles, invasives et résistantes aux médicaments. Les tentatives pour bloquer les nombreux signaux qui alimentent cet état ont apporté des bénéfices limités. Parallèlement, le pancréas et ses tumeurs montrent une tendance surprenante à accumuler des cellules graisseuses, ce qui pose la question de savoir si cette flexibilité cachée de l’identité cellulaire pourrait être exploitée. Les auteurs ont émis l’hypothèse que si les cellules cancéreuses pancréatiques riches en EMT sont déjà prêtes à changer, on pourrait peut‑être les rediriger vers une identité silencieuse de type adipeux plutôt que vers une identité invasive.
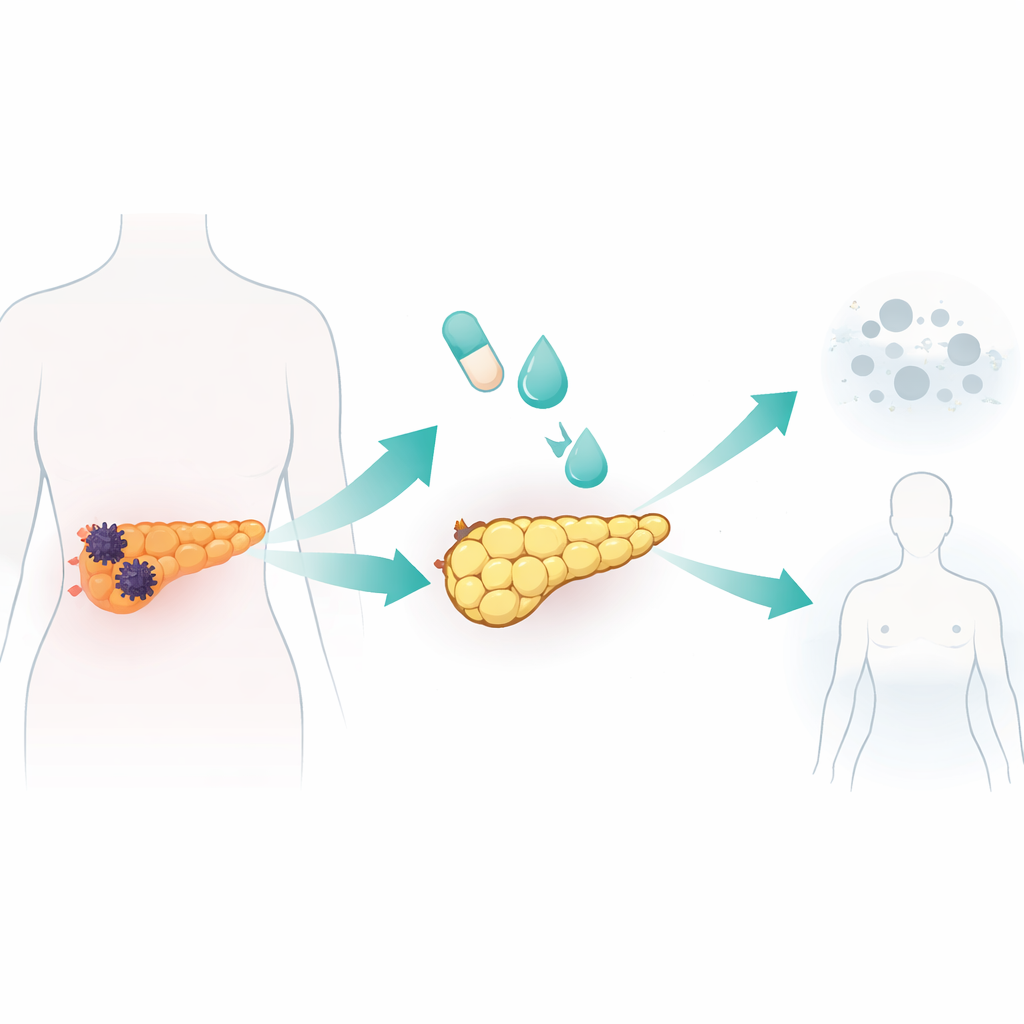
Reprogrammer des cellules cancéreuses en cellules de type adipeux en laboratoire
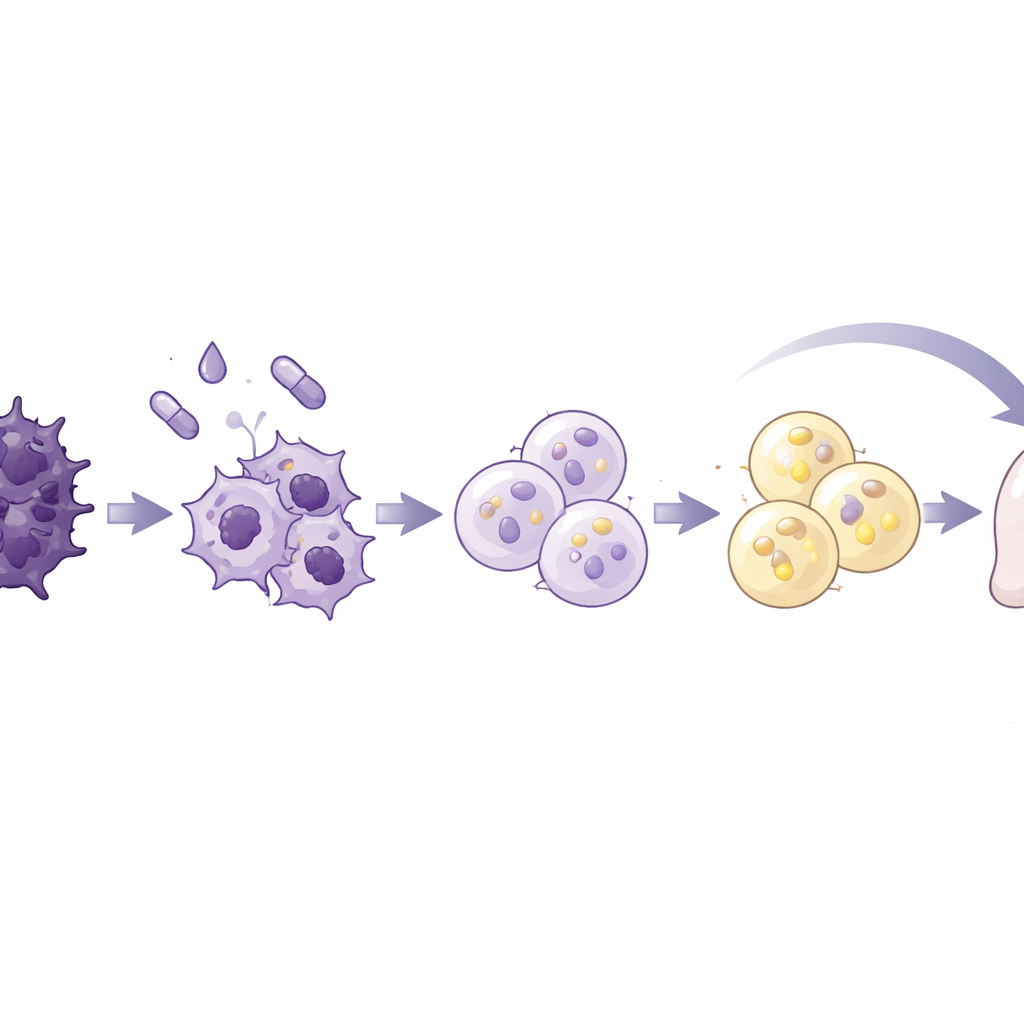
L’équipe a testé un cocktail standard de différenciation adipocytaire, utilisé dans des études antérieures sur la biologie des graisses et le cancer du sein, sur sept lignées cellulaires humaines de cancer du pancréas et une lignée cellulaire pancréatique normale. Le mélange associait de l’insuline et un stéroïde à la rosiglitazone, un médicament qui active un régulateur majeur de l’adipogenèse, plus une protéine de signalisation appelée BMP2 pour débloquer la plasticité cellulaire. Une lignée cancéreuse, nommée AsPC-1, a été particulièrement réceptive. En dix jours, ces cellules sont devenues plus grosses et plus rondes et se sont remplies de gouttelettes lipidiques, signes caractéristiques des adipocytes. Elles ont activé des gènes et des protéines typiques des cellules adipeuses matures et présenté un métabolisme lipidique robuste, incluant la sécrétion d’adiponectine et la mobilisation des graisses stockées sur stimulation. De manière cruciale, ces cellules converties ont cessé de proliférer, se sont arrêtées en phase précoce du cycle cellulaire et ont montré une motilité et une capacité d’invasion bien moindres que les cellules cancéreuses non traitées.
Éteindre le programme cancéreux au cœur de la cellule
Pour comprendre ce qui se passait au niveau moléculaire, les chercheurs ont profilé le compactage de l’ADN et l’activité génique des cellules converties. Ils ont observé un resserrement global de la chromatine, le complexe ADN–protéines qui contrôle l’accès aux gènes, ainsi qu’une baisse générale de l’expression génique, deux caractéristiques des cellules non divisantes. Les gènes qui soutiennent l’EMT, l’invasion et les métastases, y compris des enzymes dégradant la matrice et des régulateurs clés de l’EMT, ont été fortement réprimés, tandis que les gènes liés à l’adipogenèse ont été renforcés. Le profil d’expression a basculé d’une identité mésenchymateuse, très mobile, vers une identité proche des adipocytes matures. Les signaux associés à la croissance cellulaire et à la réponse à un important moteur de l’EMT, le TGF‑bêta, ont été atténués, alors que les voies liées au métabolisme des lipides et à l’adhésion cellulaire ont été renforcées. Ces changements suggèrent que les cellules n’ont pas seulement ralenti, mais ont été fondamentalement re-spécifiées.
Évaluer la stratégie chez la souris
Les scientifiques ont ensuite testé si cette conversion forcée en cellules de type adipeux pouvait aider à contrôler les tumeurs chez des animaux vivants. Ils ont implanté des cellules humaines de cancer du pancréas dans le pancréas ou la rate de souris pour modéliser des tumeurs primaires et des métastases hépatiques. Les souris traitées par rosiglitazone et BMP2 ont développé des tumeurs pancréatiques plus petites et ont montré des gouttelettes lipidiques plus abondantes et des marqueurs d’adipocytes au sein des tumeurs, ainsi que des niveaux plus faibles de gènes d’EMT et d’invasion. Dans le modèle de métastase, le traitement n’a pas modifié l’ensemencement tumoral initial, mais, au fil du temps, il a ralenti l’expansion de la charge tumorale hépatique par rapport aux animaux non traités. Fait important, les tissus pancréatiques normaux voisins n’ont pas montré de conversion évidente en cellules adipeuses, et l’état de type adipeux dans les tumeurs a persisté au moins un mois après l’arrêt des médicaments, suggérant une certaine durabilité et spécificité.
Ce que cela pourrait signifier pour la prise en charge future du cancer
Cette étude soutient un concept provocateur : pour les cancers pancréatiques très plastiques et riches en EMT, il pourrait être possible de « convertir plutôt que tuer », en redirigeant les cellules tumorales dangereuses et migrantes vers des cellules stables, non divisantes et de type adipeux, moins aptes à se disséminer. Bien qu’il s’agisse de travaux en phase préclinique sur des lignées cellulaires et des modèles murins, et que toutes les tumeurs pancréatiques ne répondent pas de la même manière, cela ouvre une nouvelle voie thérapeutique qui agit en changeant l’identité cellulaire plutôt qu’en bloquant uniquement les signaux de croissance. À l’avenir, de telles approches de transdifférenciation pourraient être combinées avec des médicaments ciblés ou des immunothérapies pour maintenir le cancer du pancréas dans un état plus calme et contrôlable et réduire le risque de métastases mortelles.
Citation: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Mots-clés: cancer du pancréas, plasticité cellulaire, transdifférenciation, transition épithélio-mésenchymateuse, cellules de type adipocyte