Clear Sky Science · fr
HNRNPH1 favorise la progression du glioblastome en régulant l’épissage des gènes du cycle cellulaire
Pourquoi cette étude sur le cancer du cerveau compte
Le glioblastome est l’une des formes les plus mortelles de cancer du cerveau, en partie parce que ses cellules se divisent rapidement tout en échappant à l’autodestruction. Cette étude révèle comment une molécule peu connue à l’intérieur des cellules tumorales les aide à continuer de se diviser de manière ordonnée, au lieu de se désagréger. En exposant ce système de soutien caché, le travail ouvre la voie à de nouvelles approches que les médecins pourraient un jour utiliser pour pousser les cellules de glioblastome au-delà du point de rupture et arrêter la croissance des tumeurs.
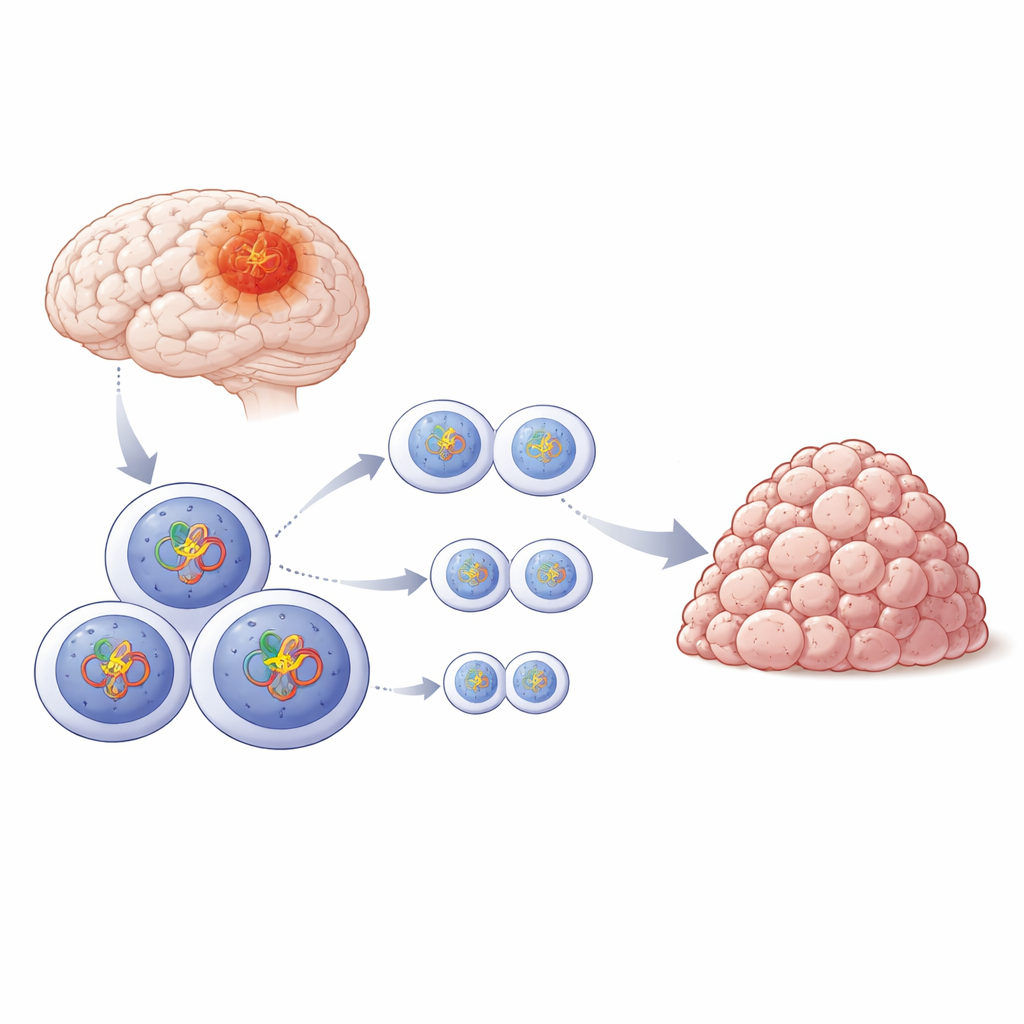
L’aide discrète à l’intérieur des cellules tumorales
Les chercheurs se sont concentrés sur le glioblastome, une tumeur cérébrale agressive qui résiste souvent à la chirurgie, à la radiothérapie et à la chimiothérapie. Les cellules cancéreuses portent généralement de nombreuses mutations de l’ADN qui les poussent à se diviser, mais elles dépendent néanmoins d’une machinerie intacte pour copier et séparer leurs chromosomes à chaque cycle cellulaire. Si cette machinerie échoue, les cellules peuvent mourir par un processus appelé « catastrophe mitotique ». L’équipe s’est donc demandé quels acteurs moléculaires aident les cellules de glioblastome à préserver ce processus délicat de division, malgré leurs génomes endommagés.
Un contrôleur du trafic pour les messages génétiques
Ils se sont concentrés sur une protéine nommée HNRNPH1, appartenant à une famille de molécules qui se lient à l’ARN — les messages de courte durée copiés à partir de l’ADN. Ces protéines contribuent à décider comment les transcrits d’ARN bruts sont découpés et recousus avant d’être transformés en protéines, un processus connu sous le nom d’épissage. En analysant de larges jeux de données de patients et des échantillons tumoraux, les scientifiques ont constaté que HNRNPH1 est produit à des niveaux beaucoup plus élevés dans les tissus de glioblastome que dans le cerveau normal. La cartographie à cellule unique et spatiale a montré qu’il est particulièrement abondant dans les cellules tumorales qui ressemblent à des cellules cérébrales immatures et à division rapide, ainsi que dans les régions bien oxygénées et fortement prolifératives de la tumeur, mais beaucoup moins présent dans les zones pauvres en oxygène et stressées.
Comment HNRNPH1 maintient la division cellulaire sur la bonne voie
Pour voir ce qui se passe quand HNRNPH1 est supprimé, l’équipe a utilisé des outils d’édition génétique et d’interférence par ARN pour réduire cette protéine dans des cellules de glioblastome cultivées. Cela a déclenché des changements massifs dans l’activité de milliers de gènes, avec des effets particulièrement marqués sur ceux qui gouvernent le point de contrôle G2/M — l’étape finale de contrôle qualité avant la division cellulaire. On a découvert que HNRNPH1 se lie directement aux plans d’ARN de plusieurs régulateurs clés de la division, y compris des protéines qui aident à séparer correctement les chromosomes. Lorsque HNRNPH1 était absent, ces ARN étaient mal épissés ou produits en moindre quantité, entraînant une diminution des protéines nécessaires à une mitose ordonnée.
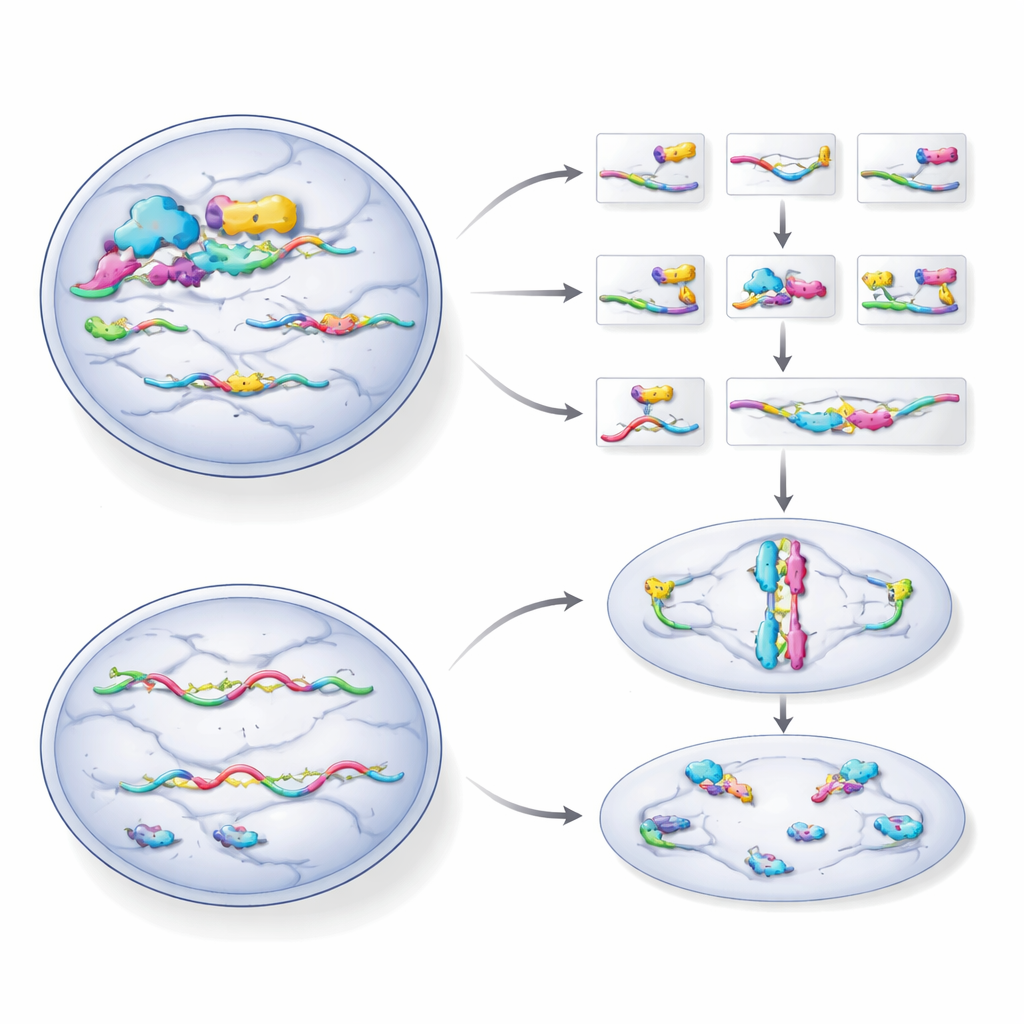
Quand l’aide disparaît, la division cellulaire déraille
Les cellules dépourvues de HNRNPH1 ont ralenti leur croissance, se sont accumulées aux stades tardifs du cycle cellulaire et ont développé des noyaux agrandis, déformés ou fragmentés — des signes classiques d’une division qui tourne mal. Au microscope, on observait moins de cellules en mitose normale et leur échafaudage interne destiné à séparer les chromosomes était perturbé. L’équipe a également découvert que HNRNPH1 oriente l’épissage d’un autre régulateur, UHRF2, faisant basculer son ARN entre une forme productive et une forme défectueuse. Sans HNRNPH1, davantage de messages UHRF2 étaient mal édités, réduisant la quantité de protéine fonctionnelle et perturbant encore davantage le contrôle du cycle cellulaire.
Preuves issues de tumeurs dans des cerveaux vivants
Les scientifiques ont ensuite testé l’importance de HNRNPH1 dans des modèles murins. Ils ont implanté des cellules de glioblastome humain, soit normales soit modifiées pour avoir une expression réduite de HNRNPH1, dans le cerveau de souris. Les animaux ayant reçu des cellules témoins ont rapidement développé de grosses tumeurs et sont morts plus tôt. Les souris ayant reçu des cellules avec HNRNPH1 diminué ont développé des tumeurs beaucoup plus petites ou retardées et ont survécu plus longtemps. Cependant, les tumeurs qui ont fini par croître avaient récupéré l’activité de HNRNPH1, ce qui suggère que les cellules incapables de restaurer cette protéine étaient fortement désavantagées et ne pouvaient pas soutenir la croissance tumorale.
Ce que cela signifie pour les traitements futurs
Dans l’ensemble, l’étude montre que les cellules de glioblastome dépendent de HNRNPH1 pour traiter correctement un réseau de messages génétiques contrôlant la division cellulaire, ce qui leur permet de proliférer sans se détruire immédiatement. Pour un non-spécialiste, cette protéine peut être vue comme un éditeur en coulisses qui maintient lisible le mode d’emploi de la cellule cancéreuse. Perturber HNRNPH1 — ou les événements d’épissage spécifiques qu’elle contrôle — pourrait rendre les cellules tumorales plus susceptibles d’accumuler des erreurs fatales pendant la division, ouvrant une nouvelle voie potentielle pour des thérapies qui pousseraient le glioblastome au-delà de son point de rupture tout en complétant les traitements existants.
Citation: Villa, G.R., Alimonti, P., Toker, J.S. et al. HNRNPH1 drives glioblastoma progression by regulating the splicing of cell cycle genes. Cell Death Dis 17, 352 (2026). https://doi.org/10.1038/s41419-026-08576-6
Mots-clés: glioblastome, cycle cellulaire, épissage de l’ARN, biologie tumorale, cancer du cerveau