Clear Sky Science · fr
L’inhibition de la kinase liée à la vaccine 2 révèle une vulnérabilité du métabolisme du glutathion dans le cancer du pancréas
Pourquoi cela importe pour le cancer du pancréas
Le cancer du pancréas est parmi les cancers les plus mortels, en partie parce que les traitements standards échouent souvent. Cette étude met au jour une faiblesse cachée de certains tumeurs pancréatiques : une dépendance à un « bouclier » cellulaire contre les sous-produits oxydants toxiques. En comprenant quand ce bouclier est fragile, et comment un gène cancéreux appelé VRK2 le renforce, les chercheurs proposent de nouvelles façons d’empoisonner sélectivement les cellules cancéreuses tout en épargnant les tissus sains.
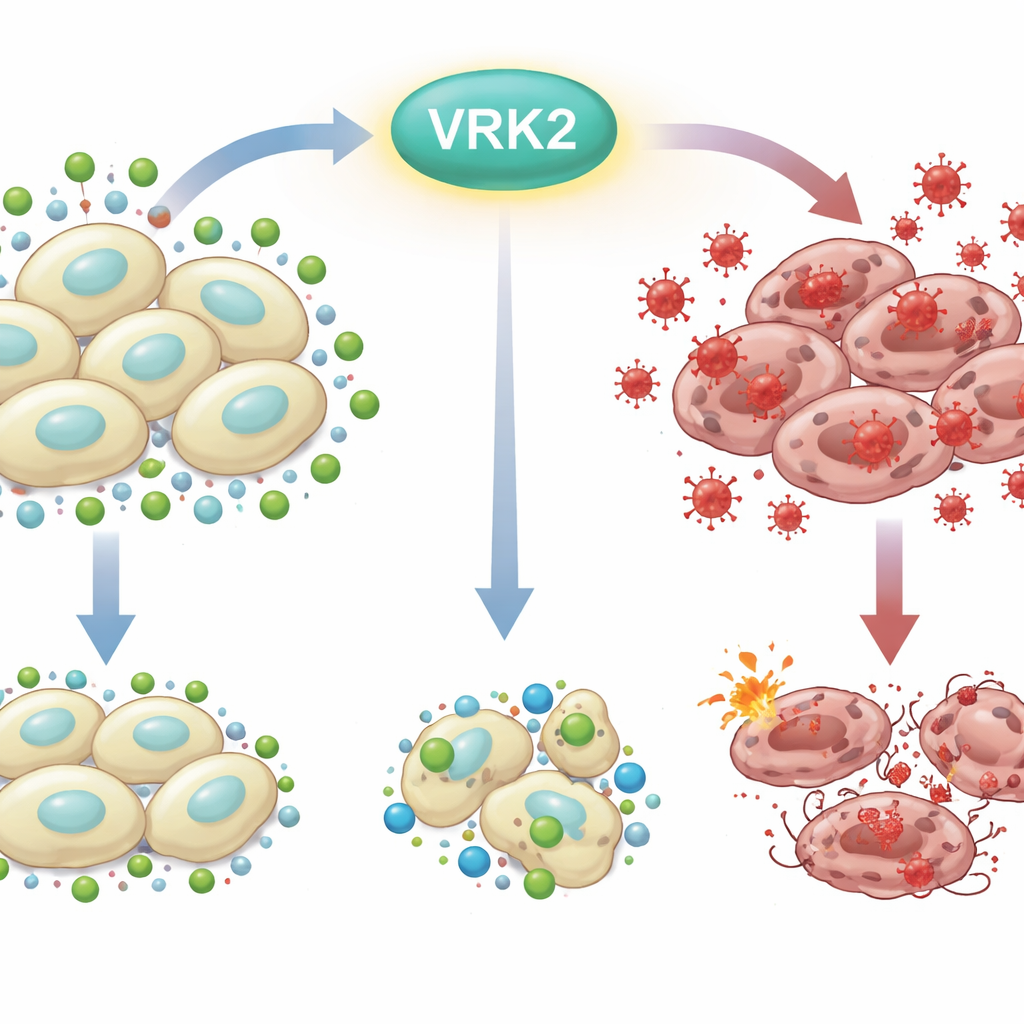
Le problème de la rouille à l’intérieur des cellules
Chaque cellule se bat constamment contre une « rouille interne » provoquée par les espèces réactives de l’oxygène : des formes très réactives de l’oxygène qui peuvent endommager l’ADN, les lipides et les protéines. Pour survivre, les cellules utilisent des défenses chimiques, le glutathion occupant l’un des rôles de protection les plus importants. Les cellules du cancer du pancréas, qui vivent dans des conditions difficiles et croissent rapidement, s’appuient fortement sur des astuces métaboliques pour maintenir des réserves suffisantes de glutathion. Perturber cet équilibre entre oxydants dommageables et antioxydants protecteurs peut pousser les cellules cancéreuses au-delà du point de rupture vers la mort cellulaire.
Découvrir un point faible caché
Les chercheurs ont commencé par inactiver VRK2, un gène favorisant le cancer déjà associé à de mauvais pronostics dans le cancer du pancréas, puis ont testé 281 composés ciblant le métabolisme. Ils ont découvert que les cellules dépourvues de VRK2 étaient remarquablement sensibles aux médicaments qui bloquent la production de glutathion. Dans ces cellules déficientes en VRK2, les niveaux de glutathion chutaient tandis que les espèces réactives de l’oxygène augmentaient, entraînant la mort cellulaire. L’apport d’antioxydants supplémentaires ou de molécules proches du glutathion les a sauvées, confirmant que la vulnérabilité clé résidait bien dans leur incapacité altérée à détoxifier le stress oxydatif.
Comment VRK2 aide à renforcer l’armure des cellules cancéreuses
Ensuite, l’équipe a cherché pourquoi VRK2 modifie le métabolisme du glutathion. Ils se sont concentrés sur une protéine transporteur appelée SLC7A11, qui se situe dans la membrane externe de la cellule et fait entrer la cystine, un élément nécessaire à la synthèse du glutathion. Fait surprenant, VRK2 n’altérait pas la quantité totale de SLC7A11 produite par la cellule ; il contrôlait plutôt si ce transporteur atteignait avec succès la surface cellulaire. Dans les cellules où VRK2 est actif, SLC7A11 voyage du réticulum endoplasmique vers l’appareil de Golgi puis vers la membrane. VRK2 favorise ce trafic en modifiant chimiquement une protéine de triage des cargaisons appelée Sec24C, qui aide à charger SLC7A11 dans les vésicules de transport. Quand VRK2 manque ou est bloqué, SLC7A11 reste coincé à l’intérieur, moins de transporteurs atteignent la surface et le bouclier de glutathion s’affaiblit.
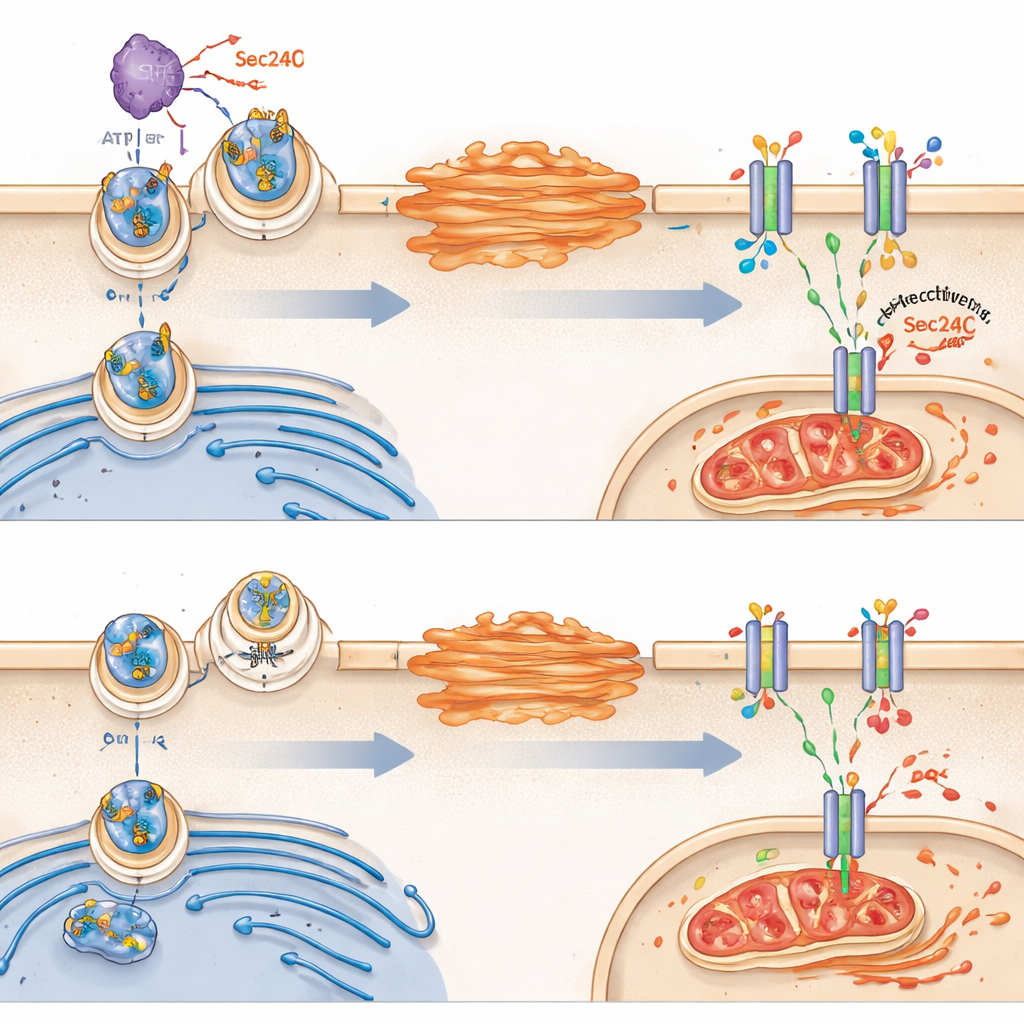
Du bouclier brisé à la ferroptose
Sans suffisamment de SLC7A11 à la membrane, les cellules déficientes en VRK2 peinent à importer la cystine et à maintenir le glutathion. Cela les rend particulièrement vulnérables à une forme de mort cellulaire dépendante du fer appelée ferroptose, caractérisée par une oxydation incontrôlée des lipides membranaires et des dommages mitochondriaux. L’étude a montré que les médicaments interrompant la synthèse du glutathion déclenchaient des signes de ferroptose dans les cellules déficientes en VRK2, notamment des mitochondries déformées et l’accumulation de produits d’oxydation des lipides. Bloquer la ferroptose, mais pas d’autres types de mort cellulaire, protégeait ces cellules, soulignant que leur talon d’Achille est une incapacité à contenir les dommages oxydatifs.
Orienter des choix de traitements personnalisés
Enfin, les chercheurs sont passés à des modèles animaux et à des cellules fraîchement dérivées de patients. Les tumeurs présentant de faibles niveaux de VRK2 ont régressé lorsqu’elles ont été traitées par un médicament ciblant le glutathion, tandis que les tumeurs à forte expression de VRK2 y résistaient largement. Cependant, lorsque les tumeurs à VRK2 élevé recevaient également un composé bloquant VRK2, elles retrouvaient une sensibilité à l’inhibition du glutathion. Cela suggère que le niveau de VRK2 peut classer les patients en groupes : ceux dont les tumeurs sont naturellement vulnérables à une thérapie ciblant le glutathion, et ceux qui pourraient bénéficier d’une stratégie en deux temps consistant d’abord à désactiver VRK2, puis à attaquer le métabolisme du glutathion.
Ce que cela signifie pour les patients
En termes simples, ce travail montre que certains cancers du pancréas survivent en utilisant VRK2 pour maintenir leur bouclier antioxydant. Enlever VRK2 amincit ce bouclier ; en supprimer le glutathion par-dessus et les cellules cancéreuses s’effondrent sous le stress oxydatif. Mesurer VRK2 dans les tumeurs pourrait donc aider les médecins à décider qui est le plus susceptible de bénéficier de médicaments perturbant le métabolisme du glutathion, et qui pourrait d’abord nécessiter une étape de ciblage de VRK2. Bien que des tests supplémentaires chez l’humain soient nécessaires, l’étude trace une voie claire vers des thérapies métaboliques plus personnalisées pour un cancer qui a désespérément besoin de meilleures options.
Citation: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Mots-clés: cancer du pancréas, métabolisme du glutathion, VRK2, ferroptose, SLC7A11