Clear Sky Science · fr
Répression de l’EGFR par le nouveau biguanide 4C potentialise l’efficacité des inhibiteurs PARP dans le cancer de l’ovaire par la régulation à la baisse de BRCA2 et Rad51
Pourquoi cette recherche est importante
Pour de nombreuses personnes diagnostiquées d’un cancer de l’ovaire, les médicaments ciblés actuels ne fonctionnent que pour une faible minorité dont les tumeurs portent des anomalies génétiques spécifiques. Cette étude explore un moyen d’étendre les bénéfices d’une classe importante de médicaments, les inhibiteurs PARP, à un groupe beaucoup plus large de patientes dont les tumeurs n’ont pas ces mutations. En associant un nouveau composé expérimental à des médicaments existants, les chercheurs présentent une stratégie pour pousser les cellules cancéreuses dans une impasse létale tout en épargnant les tissus sains.
Un obstacle dans le traitement actuel du cancer de l’ovaire
Le cancer de l’ovaire est souvent détecté tardivement et reste l’un des cancers féminins les plus mortels. Les inhibiteurs PARP, comme l’olaparib, peuvent être remarquablement efficaces, mais principalement chez les patientes dont les tumeurs présentent déjà des défauts dans une voie de réparation de l’ADN liée aux gènes BRCA1 et BRCA2. La plupart des tumeurs, cependant, disposent encore d’un appareil de réparation intact capable de corriger les lésions de l’ADN causées par ces médicaments, ce qui permet aux cellules cancéreuses de survivre. Un élément clé de cet ensemble de réparation implique deux protéines, BRCA2 et Rad51, qui aident à réparer les bris d’ADN par un processus appelé recombinaison homologue. Trouver des moyens d’affaiblir sélectivement cette voie de réparation dans les cellules cancéreuses pourrait rendre les inhibiteurs PARP utiles pour bien plus de patientes.
Le rôle d’un interrupteur de croissance bien connu
L’équipe s’est concentrée sur une molécule liée au cancer bien connue, le récepteur du facteur de croissance épidermique (EGFR), qui se trouve à la surface de nombreuses cellules tumorales et stimule leur croissance. Ils ont découvert que l’EGFR fait plus que transmettre des signaux de croissance : dans les cellules d’un cancer de l’ovaire avec des gènes BRCA normaux, des niveaux élevés d’EGFR étaient associés à une survie des patientes plus faible et à une résistance aux inhibiteurs PARP. Lorsque l’EGFR était réduit ou éteint dans des cultures cellulaires et chez la souris, les tumeurs devenaient beaucoup plus vulnérables à l’olaparib. Les chercheurs ont montré que l’EGFR favorise le transport de BRCA2 et Rad51 vers le noyau cellulaire après une lésion de l’ADN, où elles peuvent réparer les cassures et atténuer l’effet du traitement. Bloquer simplement l’activité enzymatique de l’EGFR n’était pas suffisant ; la quantité totale de protéine EGFR devait être diminuée pour perturber significativement cette voie de réparation.
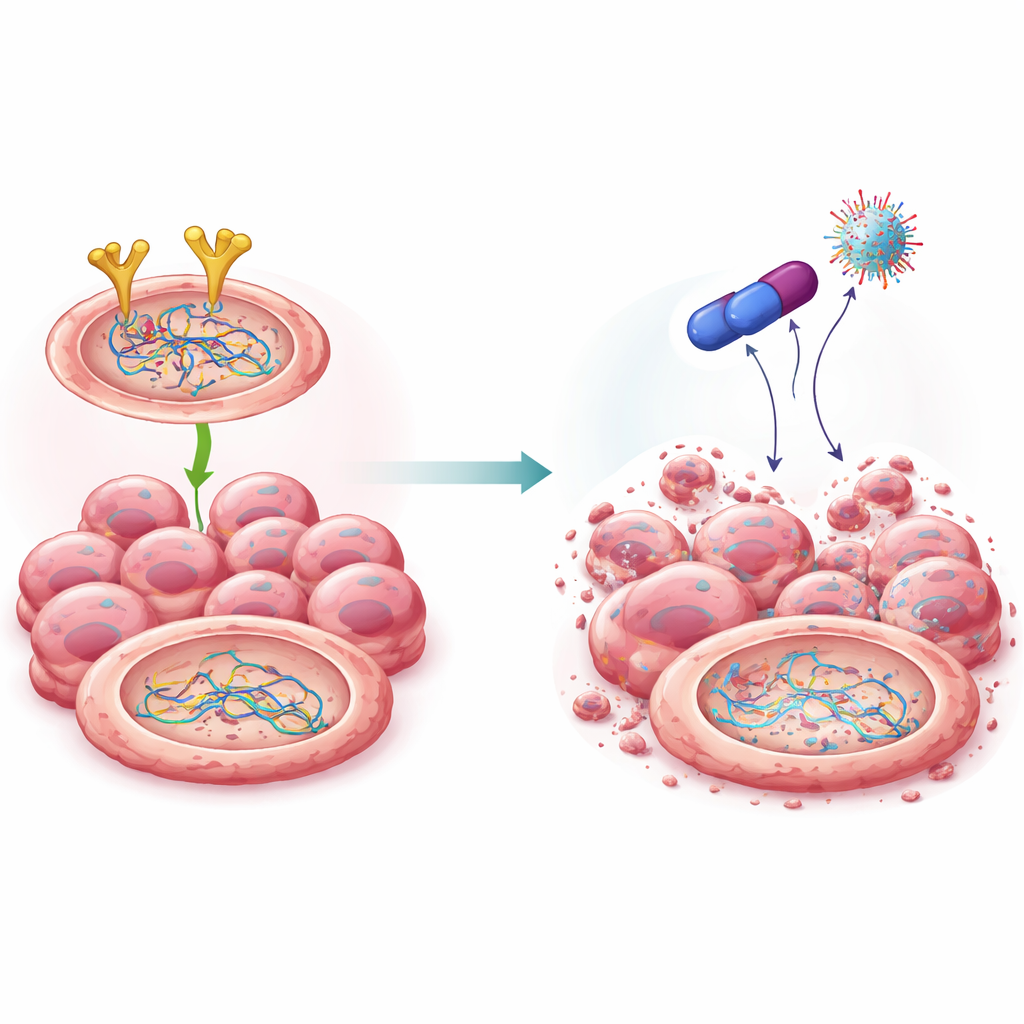
Un nouveau composé qui désarme l’équipage de réparation
En s’appuyant sur des travaux antérieurs sur une famille de médicaments connue sous le nom de biguanides, les scientifiques ont synthétisé plusieurs analogues chimiques et identifié une molécule remarquable, baptisée 4C. Ce composé était fortement toxique pour les cellules de cancer de l’ovaire tout en restant relativement doux pour les cellules normales. La modélisation informatique et les tests en laboratoire ont indiqué que 4C se lie directement à l’EGFR et le marque pour destruction par le système cellulaire de dégradation des protéines. Contrairement à certains médicaments ciblant l’EGFR existants, 4C réduisait la quantité globale d’EGFR plutôt que de simplement désactiver son activité. À mesure que les niveaux d’EGFR diminuaient, la stabilité de BRCA2 et Rad51 chutait également : elles étaient étiquetées pour être éliminées, dégradées, et n’étaient plus capables d’assurer une réparation efficace de l’ADN. Il est important de noter que cet élagage intervenait au niveau des protéines sans altérer les gènes sous-jacents.
Bloquer une voie de secours à l’intérieur de la cellule
L’étude a révélé une chaîne d’événements plus détaillée reliant les lésions de l’ADN à la survie tumorale. Après que les inhibiteurs PARP endommagent l’ADN, une autre protéine senseur appelée ATM envoie un signal du noyau vers le corps cellulaire. En réponse, l’EGFR s’associe à BRCA2 et Rad51 et les aide à pénétrer dans le noyau, où elles réparent les dégâts. Les chercheurs ont découvert qu’une troisième protéine, c-Cbl, joue normalement le rôle d’étiqueteur pour l’élimination de BRCA2 et Rad51. L’EGFR entre en compétition avec c-Cbl pour l’accès à ces protéines de réparation, les protégeant ainsi d’une marque de destruction. Lorsque 4C réduit les niveaux d’EGFR, c-Cbl peut se lier plus facilement à BRCA2 et Rad51, entraînant leur marquage, leur dégradation et leur disparition. Avec moins de protéines de réparation dans le noyau, les lésions d’ADN s’accumulent et les cellules cancéreuses deviennent beaucoup plus sensibles aux inhibiteurs PARP.
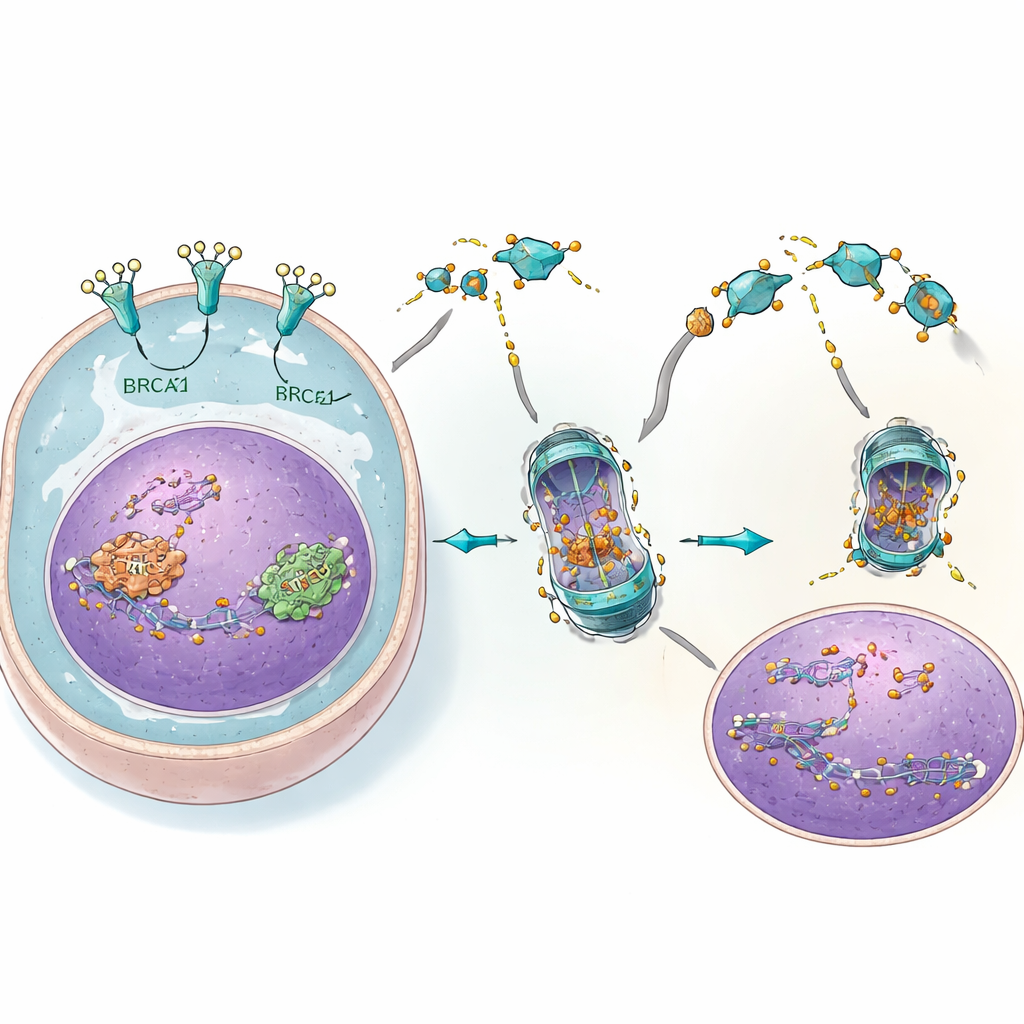
Des cellules aux animaux : un partenariat puissant
À la fois dans des cellules en culture et dans des modèles murins, l’association de 4C avec des inhibiteurs PARP a produit un coup de poing en deux temps très efficace. Les tumeurs avec des gènes BRCA normaux qui résistaient à l’un ou l’autre médicament seul ont fortement régressé ou cessé de croître lorsqu’elles ont été exposées aux deux simultanément. Les marqueurs de lésions de l’ADN ont augmenté nettement, ce qui est cohérent avec l’idée que la réparation était submergée. En même temps, les cellules normales et les organes clés tels que le foie et les reins n’ont montré que peu de signes de dommage, probablement parce qu’ils présentent des niveaux d’EGFR beaucoup plus bas et dépendent moins de cette voie de réparation particulière. Les bénéfices de la combinaison se sont également étendus à la réduction de la dissémination des cellules de cancer de l’ovaire dans l’organisme.
Ce que cela pourrait signifier pour les patientes
Ce travail propose un moyen de transformer la force d’une cellule cancéreuse en faiblesse. En ciblant l’EGFR avec le nouveau composé 4C, les chercheurs retirent la protection fournie par BRCA2 et Rad51, faisant en sorte que des tumeurs ayant autrement un appareil de réparation de l’ADN intact se comportent davantage comme des cancers porteurs de mutations BRCA en réponse aux inhibiteurs PARP. Cette vulnérabilité forcée, connue sous le nom de « létalité synthétique », pourrait étendre l’accès aux médicaments existants à beaucoup plus de femmes atteintes d’un cancer de l’ovaire, tout en maintenant des effets secondaires maîtrisables. Bien que 4C soit encore expérimental et nécessite des tests approfondis dans des modèles avancés et des essais cliniques, l’étude offre une feuille de route claire sur la façon dont le démantèlement de certains assistants de réparation dans les cellules tumorales pourrait améliorer les résultats thérapeutiques.
Citation: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Mots-clés: cancer de l’ovaire, inhibiteurs PARP, EGFR, réparation de l’ADN, thérapie ciblée