Clear Sky Science · fr
La perte de PRKACB facilite la métastase du cancer gastrique de type diffus via l’activation de la signalisation RhoA
Pourquoi cette étude compte pour le cancer de l’estomac
Le cancer gastrique de type diffus est une forme particulièrement agressive de cancer de l’estomac qui se propage souvent largement dans l’abdomen, ce qui complique le traitement et augmente la mortalité. Cette étude explore les raisons pour lesquelles ces tumeurs sont si enclines à se disséminer, en dévoilant un système moléculaire de freinage qui normalement empêche les cellules cancéreuses de migrer — et en montrant ce qui se passe lorsque ce frein lâche. Comprendre cet interrupteur de contrôle caché pourrait ouvrir de nouvelles voies pour prédire quels patients courent le plus de risque et pour développer des médicaments qui ralentissent ou arrêtent la propagation dangereuse.
Une forme dangereuse de cancer de l’estomac
Tous les cancers de l’estomac ne se comportent pas de la même manière. Les tumeurs de type intestinal ont tendance à former des masses plus structurées, tandis que le cancer gastrique de type diffus (CGD) est constitué de cellules disséminées qui s’échappent facilement de la tumeur primaire. Les patients atteints de CGD ont un risque de mortalité plus élevé que ceux atteints de la forme intestinale, en partie parce que leurs tumeurs ensemencent plus facilement de nouvelles croissances dans la cavité abdominale. Des études génétiques antérieures avaient déjà associé le CGD à des altérations récurrentes d’un gène appelé RHOA, qui influence la mobilité et la morphologie cellulaires. Mais il restait incertain comment ces modifications se reliaient aux réseaux de signalisation plus larges qui régulent si les cellules cancéreuses restent en place ou migrent.
Trouver un frein manquant dans des échantillons tumoraux
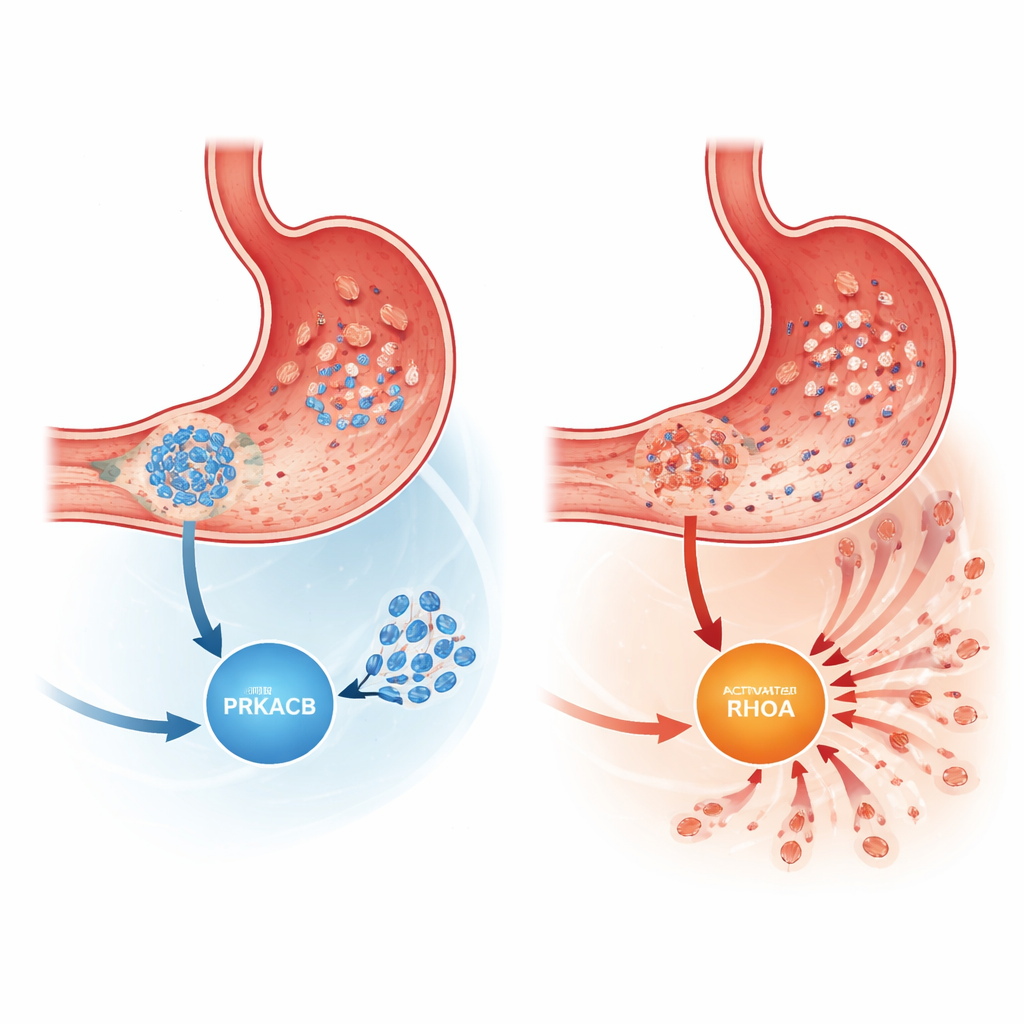
Les chercheurs se sont concentrés sur une protéine appelée PRKACB, une sous-unité catalytique de l’enzyme bien connue protéine kinase A, qui ajuste finement de nombreux comportements cellulaires en ajoutant des groupes phosphate à d’autres protéines. Une enquête protéomique antérieure avait suggéré que les niveaux de PRKACB étaient anormalement bas dans les CGD agressifs. Pour vérifier cela, l’équipe a examiné des échantillons tumoraux provenant de 376 patients, en comparant les cancers de type diffus et de type intestinal ainsi que les tissus non cancéreux adjacents. Ils ont constaté que les niveaux de PRKACB étaient nettement réduits dans les tumeurs de type diffus, en particulier aux stades avancés, mais pas dans les cancers de type intestinal. Les patients dont les tumeurs contenaient peu de PRKACB présentaient une survie globale significativement moindre, même après prise en compte d’autres facteurs cliniques, ce qui suggère que PRKACB joue un rôle de suppresseur tumoral dans ce contexte.
Comment une faible quantité de PRKACB favorise l’évasion cellulaire
Pour voir ce que fait PRKACB à l’intérieur des cellules cancéreuses, l’équipe a utilisé des lignées cellulaires en culture qui modélisent le CGD. Lorsqu’ils ont réduit artificiellement PRKACB, les cellules sont devenues plus mobiles et invasives dans des tests en laboratoire, traversant plus facilement des barrières et formant des projections en doigt appelées pseudopodes qui aident les cellules à ramper. Ces cellules ont aussi basculé d’un état épithélial plus ordonné vers un état plus lâche de type mésenchymateux associé aux métastases, perdant la molécule d’adhésion E‑cadherine qui aide normalement les cellules à rester groupées. À l’inverse, augmenter les niveaux de PRKACB rendait les cellules moins migratoires et moins invasives. Fait important, ces changements n’affectaient pas la vitesse de prolifération cellulaire, ce qui indique un rôle spécifique de PRKACB dans la dissémination plutôt que dans la croissance.
Zoom sur l’interrupteur de signalisation RhoA
Les chercheurs se sont ensuite demandé comment PRKACB exerce cet effet anti‑métastatique. À l’aide de méthodes d’interaction protéine–protéine et de modélisation structurelle, ils ont montré que PRKACB se lie directement à RhoA, un interrupteur moléculaire qui bascule entre des formes inactives et actives pour contrôler la forme et le mouvement cellulaire. PRKACB ajoute un groupe phosphate à une position spécifique de RhoA (sérine 188), ce qui inhibe RhoA et atténue les voies en aval ROCK et FAK qui pilotent les réarrangements du cytosquelette et la motilité cellulaire. Lorsque PRKACB était supprimé, RhoA était moins phosphorylé, plus actif, et la signalisation ROCK/FAK s’intensifiait, entraînant des mouvements cellulaires plus agressifs. Dans des modèles murins où des tumeurs proches de celles humaines étaient implantées dans la paroi gastrique, la diminution de PRKACB a provoqué davantage de nodules métastatiques abdominaux plus volumineux et une apparition plus précoce de la dissémination visible, là encore sans modifier la vitesse de croissance des métastases établies.
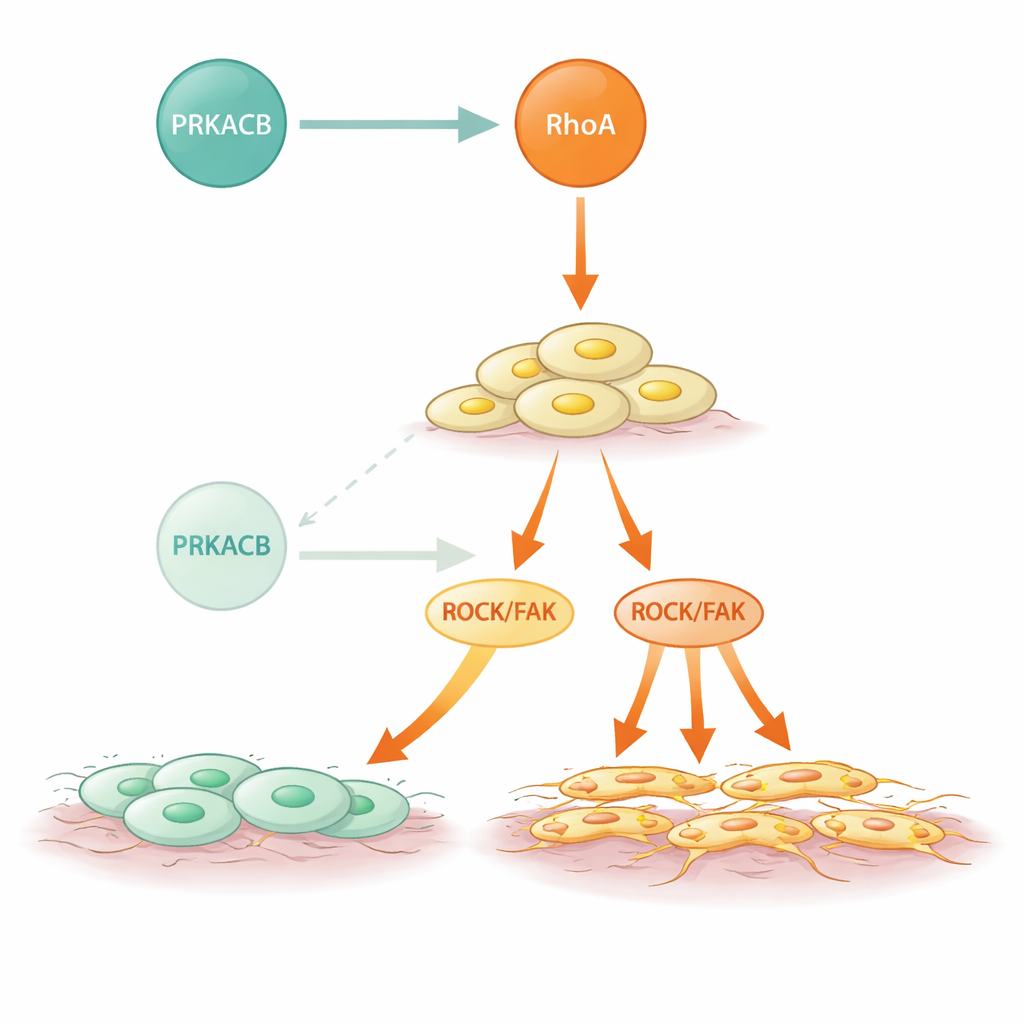
Signalisation mutante et une voie d’intervention possible
Les cancers gastriques de type diffus portent souvent des mutations de RHOA, et cette étude montre comment certaines de ces altérations aggravent le problème. Plusieurs mutations fréquentes associées au CGD affaiblissaient ou abolissaient la liaison de RhoA à PRKACB sans compromettre la capacité de RhoA à activer ses partenaires en aval. En conséquence, ces formes mutantes échappaient à la phosphorylation inhibitrice par PRKACB et présentaient une activité ROCK accrue et un comportement invasif renforcé. De façon remarquable, lorsque les chercheurs ont traité les cellules et les souris avec un composé bloquant RhoA, l’excès de métastases induit par la faible expression de PRKACB a été en grande partie inversé. Cela suggère que, même dans les tumeurs où le frein naturel est faible ou absent, cibler directement la voie RhoA hyperactive pourrait freiner la dissémination.
Ce que cela signifie pour les patients et les thérapies futures
En termes simples, ce travail identifie PRKACB comme un élément clé d’un circuit interne « anti‑migration » dans le cancer gastrique de type diffus. Lorsque les niveaux de PRKACB diminuent, ou lorsque RhoA est muté de sorte que PRKACB ne peut plus s’y lier et le modifier, la signalisation RhoA s’emballe et les cellules cancéreuses deviennent plus aptes à se détacher et à coloniser la cavité abdominale. Mesurer PRKACB et le statut de RhoA dans les tumeurs pourrait aider les médecins à évaluer la probabilité de métastase pour un patient et à identifier ceux qui bénéficieraient le plus de médicaments inhibant la voie RhoA–ROCK–FAK. Bien que de tels traitements nécessitent un développement et des essais cliniques supplémentaires, l’étude cartographie une route moléculaire claire allant d’un frein manquant à une propagation mortelle — et indique de nouvelles façons de ralentir ce processus.
Citation: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Mots-clés: cancer gastrique de type diffus, métastase, PRKACB, signalisation RhoA, voie ROCK FAK