Clear Sky Science · fr
La signalisation leptine-LEPR de la moelle osseuse reprogramme le métabolisme oxydatif mitochondrial pour conférer une chimiorésistance dans la leucémie myéloïde aiguë
Pourquoi la graisse de la moelle osseuse compte pour le traitement de la leucémie
Beaucoup savent que la graisse corporelle peut influencer des maladies comme le diabète et les troubles cardiovasculaires, mais peu réalisent que la graisse cachée à l’intérieur de nos os peut aussi affecter la réponse des cancers du sang aux traitements. Cette étude examine comment une hormone produite par les adipocytes, la leptine, aide à protéger les cellules de la leucémie myéloïde aiguë (LMA) contre la chimiothérapie standard. Comprendre ce système de protection caché pourrait indiquer de nouvelles voies pour améliorer l’efficacité des médicaments existants pour les patients.
Une hormone qui fait pencher la balance contre la chimiothérapie
Les chercheurs ont commencé par étudier des échantillons de moelle osseuse d’adultes récemment diagnostiqués de LMA. Ils ont mesuré les niveaux de leptine dans la moelle et évalué la capacité des patients à éliminer les cellules leucémiques après administration d’un traitement courant, la cytarabine. Les patients présentant des taux plus élevés de leptine dans la moelle et une expression plus importante de son récepteur sur les cellules leucémiques répondaient moins bien au traitement et avaient une survie plus courte. Même après ajustement sur d’autres facteurs de risque, la leptine restait un indicateur fort d’une mauvaise réponse à la chimiothérapie. Cela suggère que l’hormone d’origine graisseuse fait plus que refléter la sévérité de la maladie ; elle est activement liée à la résistance.
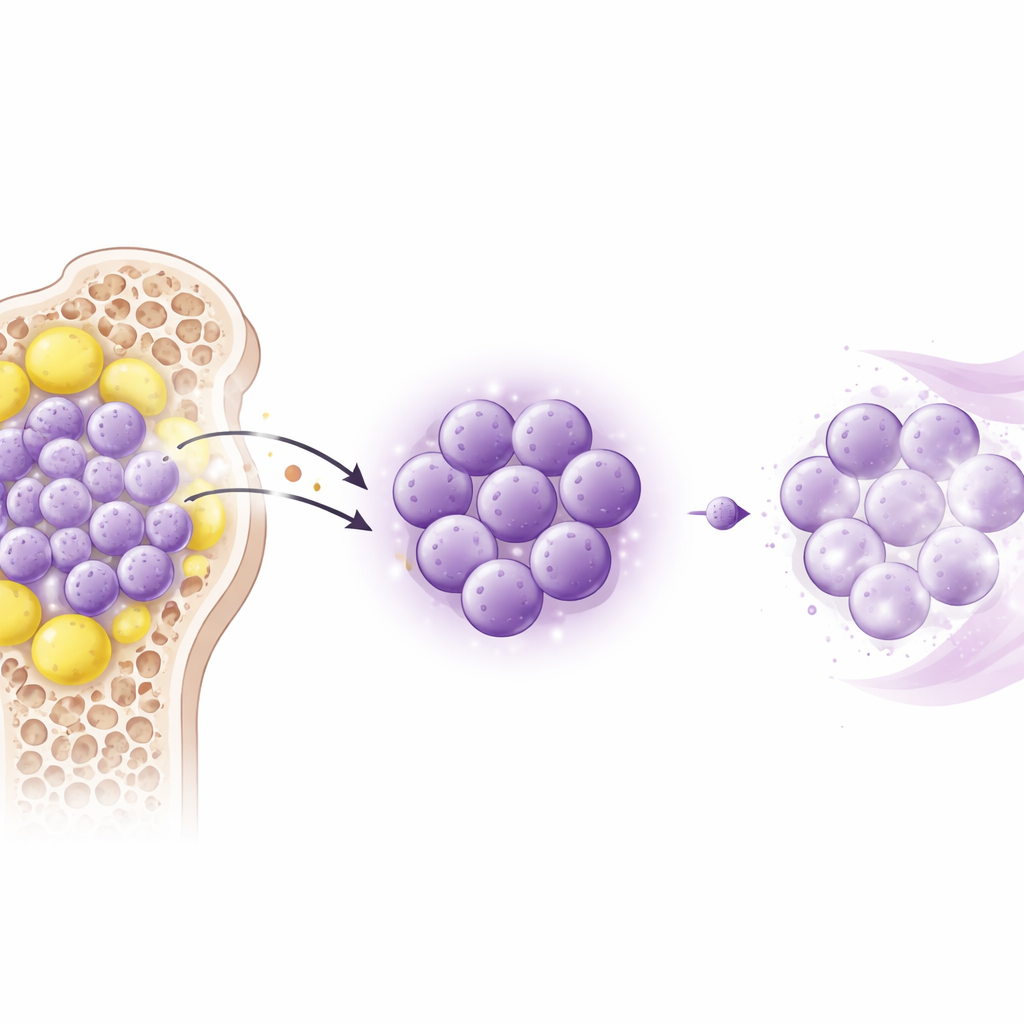
Des modèles animaux révèlent un bouclier caché
Pour tester si la leptine cause réellement la résistance aux médicaments, l’équipe a utilisé deux modèles murins de LMA qui reproduisent fidèlement la maladie humaine. Les souris ont reçu soit la cytarabine seule, soit la cytarabine avec un apport supplémentaire de leptine, soit la cytarabine associée à un petit peptide bloquant le récepteur de la leptine. L’ajout de leptine a raccourci la survie, hypertrophié la rate et le foie, et permis aux cellules leucémiques d’envahir ces organes malgré la chimiothérapie. En revanche, le blocage du récepteur n’a pas ralenti la progression de la leucémie par lui-même mais a significativement renforcé l’effet de la cytarabine, réduisant la taille des organes atteints et la charge leucémique. Ces résultats montrent que l’effet principal de la leptine n’est pas d’accélérer directement la croissance cancéreuse, mais de rendre les cellules leucémiques plus difficiles à éliminer lors de la chimiothérapie.
Booster les centrales énergétiques de la cellule
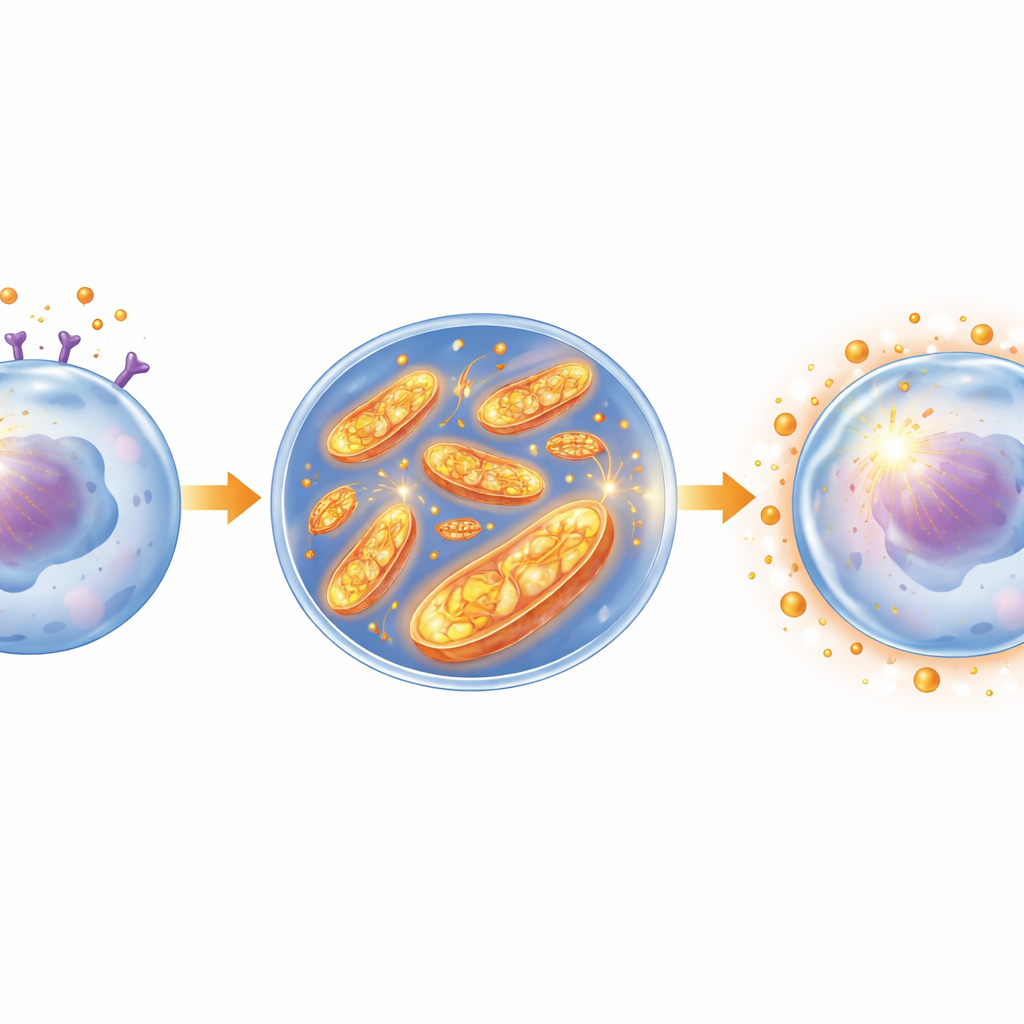
En approfondissant, les scientifiques ont examiné comment la leptine modifie le métabolisme des cellules leucémiques. Ils ont découvert que la leptine active une cascade de signalisation intracellulaire, connue sous le nom JAK2/STAT3, qui à son tour stimule les mitochondries — les petites centrales qui génèrent l’énergie. Chez des cellules leucémiques murines et des lignées de LMA humaines, la leptine a augmenté l’activité d’un composant clé mitochondrial, le complexe I, et a accru le métabolisme oxydatif global. Ce changement a généré davantage d’espèces réactives de l’oxygène à l’intérieur des mitochondries. Paradoxalement, au lieu d’endommager les cellules, cette élévation progressive des molécules réactives a déclenché une réponse adaptative : les cellules leucémiques ont renforcé leurs défenses antioxydantes, comme le glutathion et les enzymes détoxifiantes, créant une puissante protection interne.
Quand le stress devient une armure
L’équipe a montré que cette protection est centrale dans la chimiorésistance. Les cellules leucémiques traitées par la leptine présentaient une capacité antioxydante totale plus élevée et étaient moins affectées par la cytarabine et un autre médicament, la daunorubicine. La suppression du récepteur de la leptine par édition génomique a affaibli ce réseau antioxydant, diminué les niveaux de molécules protectrices et rendu les cellules beaucoup plus sensibles au traitement, même en l’absence de leptine. Des expériences supplémentaires ont confirmé qu’une brusque augmentation du stress mitochondrial peut aussi déclencher un programme protecteur similaire, tandis que l’élimination de ces molécules réactives détruit la protection et restaure la sensibilité aux médicaments. De manière importante, le blocage de la voie JAK2/STAT3 ou du récepteur de la leptine a empêché l’activation du complexe I, réduit les signaux de stress mitochondrial, effondré la barrière antioxydante et rendu la chimiothérapie de nouveau efficace.
Transformer une faiblesse en nouvelle piste thérapeutique
Pour les patients, le message de l’étude est que les cellules leucémiques peuvent exploiter une hormone produite par les cellules graisseuses voisines pour survivre à la chimiothérapie. La leptine provenant de la graisse de la moelle se lie à son récepteur sur les cellules leucémiques, reprogramme leurs mitochondries en générateurs d’énergie à haut régime, et utilise le stress de faible intensité qui en résulte pour activer un filet antioxydant protecteur. Ce filet protège les cellules des dommages plus sévères causés par les médicaments anticancéreux. En bloquant le récepteur de la leptine ou sa signalisation en aval, il pourrait un jour être possible de priver les cellules de cette protection et de permettre aux chimiothérapies existantes d’agir comme prévu, sans nécessairement augmenter les doses. Ainsi, une meilleure compréhension de la communication entre la graisse de la moelle et les cellules leucémiques pourrait se traduire directement par des rémissions plus durables pour les personnes vivant avec une LMA.
Citation: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
Mots-clés: leucémie myéloïde aiguë, leptine, chimiorésistance, mitochondries, stress oxydatif