Clear Sky Science · fr
La myosine nucléaire 1 relie l’architecture génomique au remodelage du tissu adipeux, à l’inflammation métabolique et à l’obésité chez la souris
Pourquoi le squelette cellulaire compte pour la masse grasse
On attribue souvent l’obésité à notre alimentation et à notre activité physique, mais au cœur des cellules, la manière dont l’ADN est empaqueté et lu peut aussi faire pencher la balance. Cette étude révèle qu’une petite protéine motrice, la myosine nucléaire 1 (NM1), qui aide à organiser l’ADN dans le noyau, joue un rôle surprenant dans la formation des adipocytes, le stockage de l’énergie et le déclenchement de l’inflammation. En étudiant des souris dépourvues de cette protéine, les chercheurs ont mis au jour un lien direct entre l’architecture physique de nos gènes et le développement d’une graisse viscérale délétère et de troubles métaboliques.
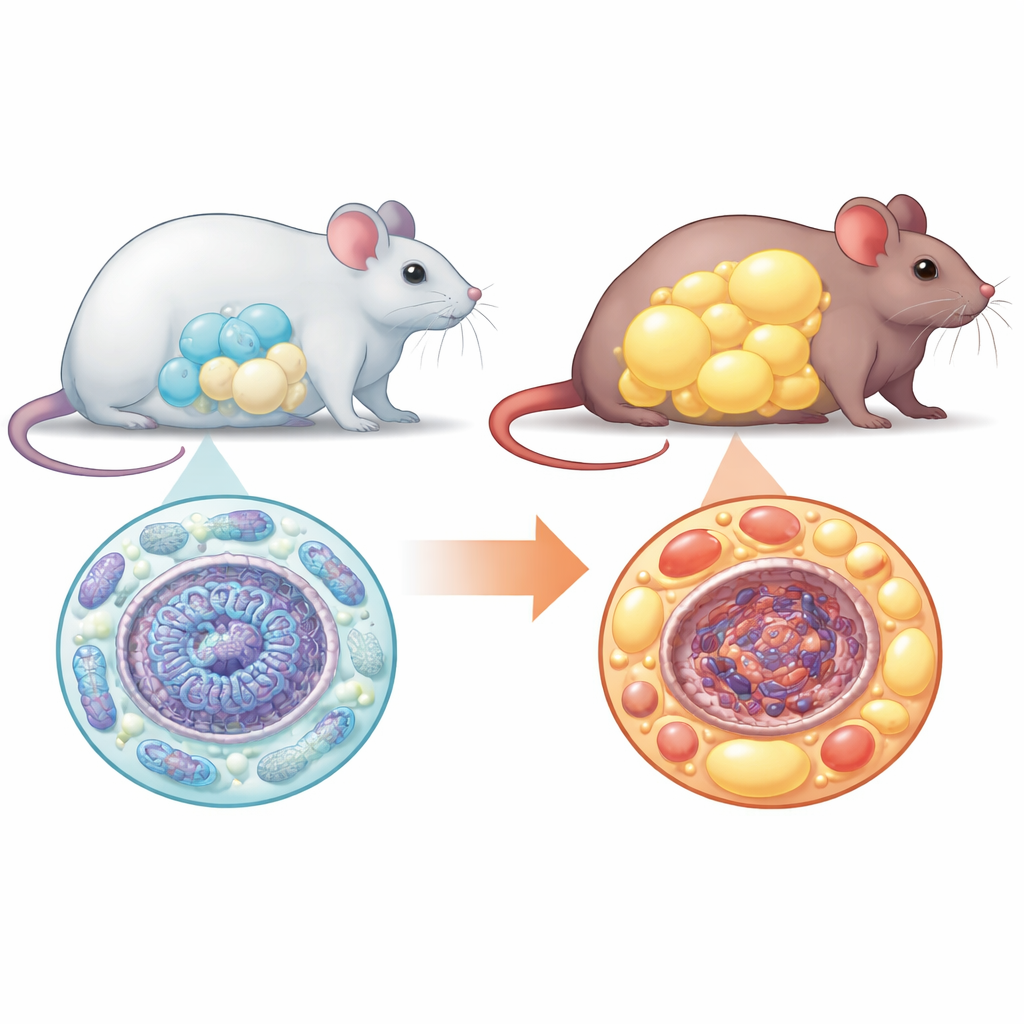
Des cellules souches aux adipocytes
Les adipocytes se développent à partir de précurseurs polyvalents appelés cellules souches mésenchymateuses. Normalement, ces précurseurs se multiplient, modifient leur usage énergétique et mûrissent en de nombreuses petites cellules graisseuses saines qui stockent les calories excédentaires en sécurité. L’équipe a constaté qu’en l’absence de NM1, ce processus ordonné se dérègle. Lorsqu’ils ont cultivé en laboratoire des cellules souches provenant de souris normales et de souris déficientes en NM1 puis les ont incitées à devenir adipocytes, bien moins de cellules ont achevé la transition sans NM1. Les cellules qui ont mûri étaient nettement plus volumineuses que la normale, remplies de lipides mais sans le profil génique et protéique typique des adipocytes sains. Ce schéma — moins de cellules mais chacune hypertrophiée — est caractéristique d’un tissu adipeux pathologique.
Comment le compactage des gènes influe sur le comportement des adipocytes
NM1 agit dans le noyau, où il contribue à maintenir des régions d’ADN accessibles afin que des gènes importants puissent être activés. Pour comprendre comment sa perte modifie le comportement cellulaire, les chercheurs ont superposé des cartes des régions d’ADN ouvertes avec des mesures de l’activité génique dans des cellules avec ou sans NM1. Ils ont observé que de nombreux gènes nécessaires à la formation des adipocytes, à la gestion des gouttelettes lipidiques et à l’entretien des mitochondries perdaient à la fois accessibilité et activité en l’absence de NM1. Parallèlement, d’autres gènes liés à la croissance et aux voies de signalisation devenaient plus accessibles et plus actifs. Cela désigne NM1 comme un contrôleur du trafic : il aide à maintenir un paysage équilibré de régions d’ADN ouvertes et fermées pour que les réseaux géniques appropriés pilotent le développement et le métabolisme sains des adipocytes.
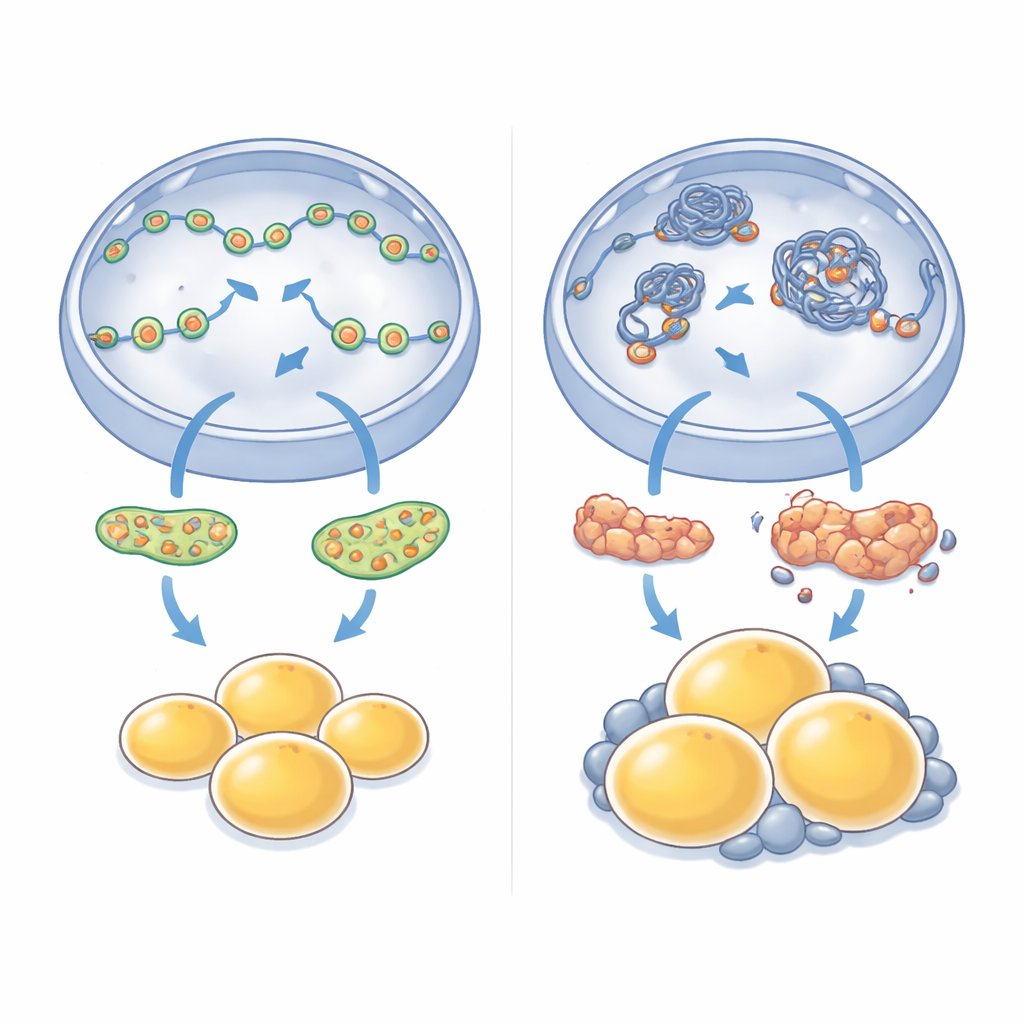
Quand des changements locaux se traduisent par une prise de poids généralisée
Les conséquences de la perte de ce moteur nucléaire unique ne sont pas restées confinées aux cellules en culture. Les souris déficientes en NM1 sont devenues progressivement plus lourdes que leurs congénères normales, alors même qu’elles ne consommaient pas plus de nourriture. Les explorations et l’analyse tissulaire ont montré une accumulation nette de graisse, en particulier autour des organes internes de l’abdomen, et les adipocytes individuels dans ces zones étaient remarquablement hypertrophiés. Lorsque les chercheurs ont mesuré les gènes sur- ou sous-exprimés dans cette graisse viscérale, ils ont trouvé des changements étendus : les voies impliquées dans l’utilisation de l’énergie, la signalisation de l’insuline et le remodelage tissulaire étaient reprogrammées. Les gènes associés à la croissance et à l’expansion des adipocytes étaient souvent stimulés, tandis que plusieurs régulateurs centraux de la formation d’adipocytes sains étaient atténués, reflétant les défauts observés dans les cellules souches cultivées.
Graisse enflammée et moteurs énergétiques perturbés
Au-delà de la taille, le tissu adipeux des souris déficientes en NM1 présentait des signes d’inflammation et de stress métabolique. Une analyse détaillée des voies a mis en évidence une forte activation des signaux immunitaires portés par des molécules comme l’interféron-gamma et le facteur de nécrose tumorale, connues pour contribuer à la résistance à l’insuline et aux maladies métaboliques. En parallèle, les régulateurs qui soutiennent un tissu adipeux calme et économe en énergie étaient supprimés. L’étude a aussi relié la perte de NM1 à des mitochondries perturbées — les moteurs énergétiques de la cellule. Les gènes qui contrôlent habituellement la qualité mitochondriale et la bascule entre production d’énergie efficace et métabolisme glycolytique rapide étaient déréglés, suggérant que sans NM1, les adipocytes adoptent une stratégie énergétique moins efficace et plus sujette au stress.
Signaux partagés entre souris et humains
Pour savoir si cette voie nucléaire pouvait aussi avoir de l’importance chez l’homme, les auteurs ont examiné de larges jeux de données génétiques provenant de graisse viscérale humaine. Ils se sont concentrés sur un homologue humain de NM1 appelé MYO1C et ont analysé des réseaux de variants qui modulent l’activité des gènes voisins. Ils ont trouvé que de nombreux thèmes observés chez la souris — contrôle du cytosquelette, signalisation immunitaire et régulation métabolique — apparaissaient aussi dans les réseaux géniques humains centrés sur MYO1C. Plusieurs gènes altérés dans la graisse des souris déficientes en NM1 figuraient également dans ces réseaux humains et ont été reliés au remodelage du tissu adipeux et au métabolisme. Ce recoupement inter-espèces suggère que des mécanismes nucléaires similaires pourraient influencer le risque d’obésité chez l’humain.
Ce que cela signifie pour l’obésité et la santé métabolique
En somme, ce travail montre que NM1 est bien plus qu’un auxiliaire nucléaire : c’est un hub central reliant l’organisation de l’ADN à la manière dont les adipocytes croissent, stockent l’énergie et communiquent avec le système immunitaire. Quand NM1 vient à manquer, les commutateurs géniques des précurseurs adipeux sont mal réglés, les mitochondries fonctionnent mal, les adipocytes s’hypertrophient au lieu de se multiplier, et la graisse viscérale s’enflamme — une combinaison qui ressemble à la graisse délétère observée dans l’obésité et la résistance à l’insuline. Pour le lecteur non spécialiste, le message est que l’agencement physique de l’ADN et de ses molécules associées à l’intérieur du noyau peut prédisposer les tissus à une expansion adipeuse saine ou nocive. Des protéines comme NM1 et son homologue humain MYO1C pourraient un jour devenir des cibles thérapeutiques pour remodeler le tissu adipeux de l’intérieur, offrant une approche plus précise pour lutter contre les maladies liées à l’obésité.
Citation: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Mots-clés: adipogenèse, chromatine, mitochondries, graisse viscérale, inflammation métabolique