Clear Sky Science · fr
Les macrophages M2 favorisent les métastases lymphatiques en régulant la translocation nucléaire de la PKM2 dans le cancer du sein triple négatif
Pourquoi cette recherche est importante
Pour les personnes diagnostiquées avec un cancer du sein triple négatif, l’une des plus grandes inquiétudes est que la tumeur se propage aux ganglions lymphatiques, une étape clé vers une dissémination généralisée. Cette étude examine comment certaines cellules immunitaires qui devraient nous protéger aident au contraire ce type de cancer du sein à envahir le système lymphatique, et identifie un « interrupteur » moléculaire qui pourrait être ciblé par des médicaments pour ralentir ou arrêter cette propagation.
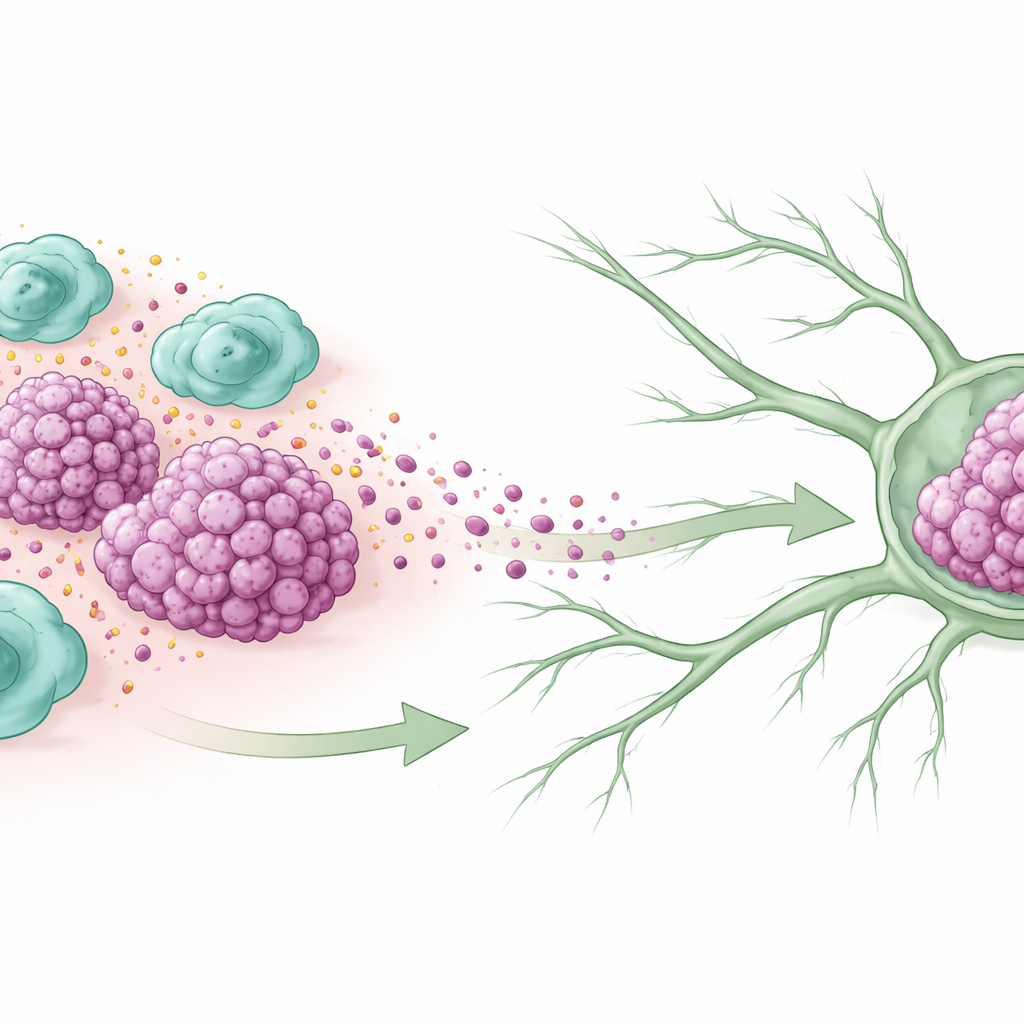
Des auxiliaires immunitaires devenus complices
Au sein de nombreuses tumeurs, des cellules immunitaires appelées macrophages s’accumulent en grand nombre. Certaines adoptent un état nourricier et réparateur, dit M2, qui dans le cancer finit souvent par aider les tumeurs plutôt que de les combattre. Les chercheurs ont analysé des tissus de femmes atteintes d’un cancer du sein triple négatif et ont constaté que les tumeurs ayant déjà envahi les ganglions lymphatiques contenaient beaucoup plus de macrophages de type M2. Les patientes dont les tumeurs étaient riches en ces cellules avaient tendance à présenter des cancers plus volumineux, des caractéristiques plus agressives et une survie plus courte, ce qui suggère que ces cellules immunitaires de « tir ami » sont étroitement liées à l’aggravation de la maladie.
Construire de nouvelles « autoroutes » lymphatiques pour les cellules cancéreuses
Les cellules cancéreuses n’atteignent généralement pas les ganglions lymphatiques par hasard ; elles empruntent souvent des vaisseaux lymphatiques nouvellement formés, des canaux minuscules qui drainent les fluides des tissus. Dans cette étude, les tumeurs riches en macrophages M2 présentaient également davantage de ces vaisseaux lymphatiques. In vitro, lorsque des cellules de cancer du sein étaient cultivées en présence de macrophages M2, elles libéraient des signaux qui incitaient les cellules lymphatiques humaines à former des réseaux tubulaires et à migrer plus rapidement, reproduisant la formation de nouveaux canaux lymphatiques. Chez la souris, des cellules cancéreuses pré-exposées aux macrophages M2 ont induit la formation de plus de vaisseaux lymphatiques au sein de la tumeur et des métastases plus fréquentes aux ganglions lymphatiques voisins, confirmant que ces cellules immunitaires aident activement à construire des voies d’évasion.
La chaîne de signaux cachée à l’intérieur des cellules cancéreuses
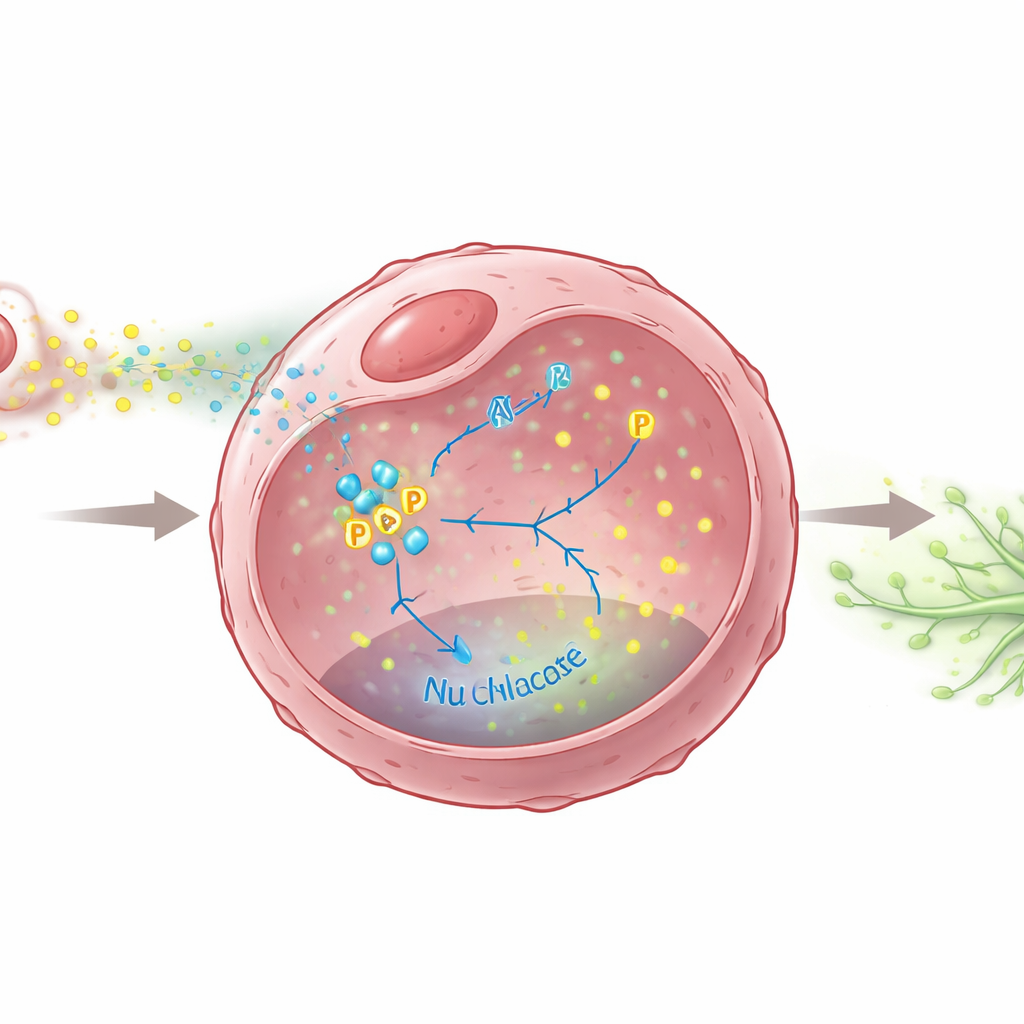
L’équipe a ensuite cherché quels messages chimiques les macrophages M2 envoient pour pousser les tumeurs vers la dissémination lymphatique. Ils ont identifié une molécule bien connue, le TGF-β, libérée en plus grande quantité par les macrophages M2. Ce signal provoquait chez les cellules cancéreuses une augmentation de la production de deux facteurs de croissance, VEGFC et VEGFD, qui sont des moteurs puissants de la croissance des vaisseaux lymphatiques. De façon cruciale, les chercheurs ont montré qu’une enzyme métabolique à l’intérieur des cellules cancéreuses, la PKM2, joue le rôle d’interrupteur central dans ce processus. Sous la stimulation par le TGF-β, la PKM2 non seulement accroît le métabolisme glucidique de la cellule, mais elle est aussi modifiée chimiquement et migre vers le noyau, où elle contribue à l’activation des gènes codant pour VEGFC et VEGFD. En l’absence de PKM2, ou lorsque sa translocation nucléaire était bloquée, les cellules cancéreuses produisaient beaucoup moins de ces signaux favorisant les vaisseaux lymphatiques et déclenchaient moins efficacement leur formation.
Tester un frein possible à la propagation
Parce que la PKM2 se situe à ce carrefour crucial entre métabolisme altéré et signalisation pro-métastatique, les scientifiques ont testé si la bloquer pouvait ralentir la dissémination lymphatique. Ils ont utilisé la shikonine, un composé qui interfère avec l’activation de la PKM2 et son entrée dans le noyau. En culture cellulaire, la shikonine a fortement réduit les niveaux de VEGFC et VEGFD et affaibli la capacité des sécrétions des cellules cancéreuses à induire la croissance et la migration des vaisseaux lymphatiques. Dans des modèles murins, le traitement par la shikonine a diminué le nombre et la taille des métastases ganglionnaires et réduit la densité des vaisseaux lymphatiques dans les tumeurs, sans effets toxiques évidents chez les animaux. Ces résultats suggèrent que bloquer la PKM2 pourrait à la fois priver les cellules cancéreuses de certains avantages métaboliques et réduire leur capacité à remodeler le réseau lymphatique à leur profit.
Ce que cela signifie pour les patientes et patients
Au total, l’étude propose une chaîne d’événements claire : les macrophages M2 dans les tumeurs triple négatif sécrètent du TGF-β, qui convertit la PKM2 dans les cellules cancéreuses en une double fonction — alimenter une consommation glucidique élevée et agir dans le noyau pour activer VEGFC et VEGFD. Ces facteurs stimulent ensuite la croissance de vaisseaux lymphatiques que les cellules cancéreuses utilisent pour atteindre les ganglions lymphatiques et au-delà. En identifiant la PKM2 comme un point central de cette chaîne, le travail suggère de nouvelles façons de prédire et potentiellement de traiter la dissémination lymphatique, en particulier chez les patientes dont les tumeurs affichent des niveaux élevés de macrophages M2, de PKM2 ou de VEGFC/D. Bien que des essais supplémentaires chez l’humain soient nécessaires, cibler cette voie pourrait contribuer à transformer le système lymphatique d’une autoroute pour le cancer en une barrière.»
Citation: Yang, Y., Ye, H., Zhong, D. et al. M2 macrophages promote lymphatic metastasis by regulating PKM2 nuclear translocation in triple-negative breast cancer. Cell Death Dis 17, 262 (2026). https://doi.org/10.1038/s41419-026-08524-4
Mots-clés: cancer du sein triple négatif, métastases ganglionnaires, macrophages associés à la tumeur, PKM2, lymphangiogenèse