Clear Sky Science · fr
La triméthylation de la lysine 36 de l’histone H3 par SETD2 façonne un paysage épigénétique dans les cellules souches intestinales pour orchestrer le métabolisme des lipides et atténuer la sénescence cellulaire
Pourquoi les cellules souches intestinales comptent à mesure que nous vieillissons
Au cœur de la muqueuse intestinale, de petites cellules souches travaillent sans relâche pour renouveler le tissu qui nous permet de digérer les aliments et d’absorber les nutriments. En vieillissant, ces cellules s’épuisent, rendant l’intestin plus vulnérable aux maladies et plus lent à réparer les lésions. Cette étude examine comment de subtiles marques chimiques sur les protéines qui emballent l’ADN aident à conserver la jeunesse des cellules souches intestinales, comment leur perte perturbe la combustion des graisses à l’intérieur des cellules, et comment des médicaments bien choisis pourraient un jour ralentir ce déclin.
Des cellules vieillissantes dans un environnement exigeant
La surface interne de l’intestin est l’un des tissus qui se renouvellent le plus rapidement dans l’organisme. Les cellules souches nichées à la base de petites cavités, appelées cryptes, se divisent pour remplacer des milliards de cellules tous les quelques jours. Ce travail constant exige un apport énergétique stable, en grande partie fourni par la dégradation des graisses. Parallèlement, ces cellules souches sont contrôlées par un code « épigénétique » — des marques chimiques sur les histones qui déterminent en partie quels gènes sont actifs ou silencieux. Les auteurs se sont concentrés sur l’une de ces marques, connue sous le nom de triméthylation de H3K36, catalysée par une enzyme appelée SETD2, et ont cherché à savoir si les modifications de cette marque pouvaient expliquer pourquoi les cellules souches intestinales perdent de leur vigueur avec l’âge.
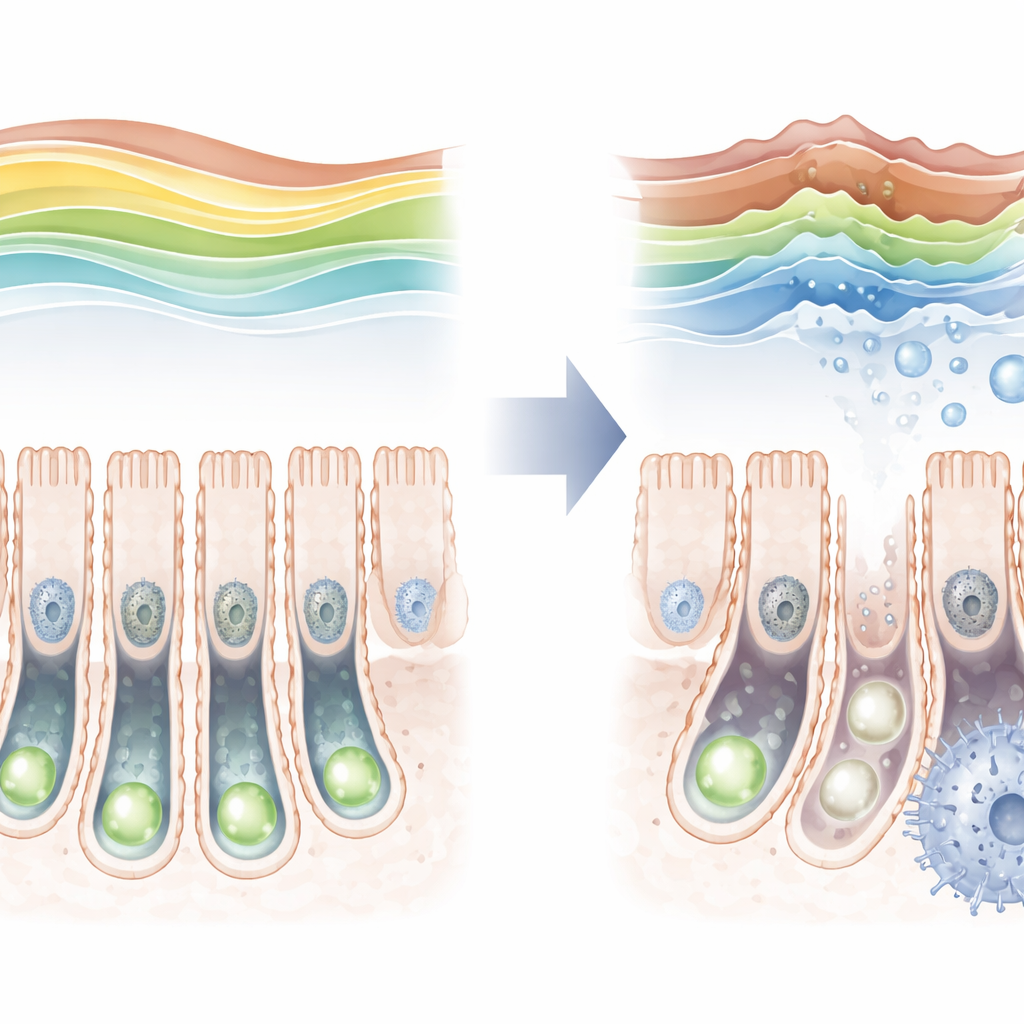
Une marque protectrice qui s’estompe avec l’âge
En examinant des intestins de souris tout au long de leur vie, les chercheurs ont constaté que la triméthylation de H3K36 n’est pas statique. Elle est relativement faible juste après la naissance, augmente pour atteindre un pic chez les jeunes adultes, puis décline chez les animaux âgés. À mesure que cette marque diminuait chez les animaux plus vieux, des marqueurs de vieillissement cellulaire augmentaient dans les cellules souches, suggérant un lien entre les deux. Pour tester cela plus directement, l’équipe a génétiquement conçu des souris où SETD2 pouvait être supprimée uniquement dans les cellules souches intestinales. Lorsque cette enzyme était éliminée, la marque protectrice disparaissait presque, les cellules souches se divisaient moins fréquemment et peinaient à produire l’éventail complet des types cellulaires spécialisés de l’intestin.
Comment les changements épigénétiques perturbent la combustion des graisses
La perte de cette unique marque histone a déclenché une cascade de modifications au sein des cellules souches. Les mesures d’activité génique ont montré que de nombreux gènes impliqués dans le cycle cellulaire et la réplication de l’ADN étaient réprimés, tandis que des gènes associés au stress et au vieillissement étaient stimulés. De façon marquante, le signal le plus fort indiquait une altération du métabolisme des lipides : les gènes qui soutiennent normalement l’oxydation des acides gras — la combustion contrôlée des graisses pour produire de l’énergie — étaient atténués, et des lipides se sont mis à s’accumuler dans les cryptes. Le profilage des métabolites a confirmé l’accumulation d’acides gras à longue chaîne, signe que les voies habituelles de traitement des lipides défaillaient. Parallèlement, l’organisation physique de l’ADN dans le noyau a changé, avec de nombreuses régions devenant plus exposées ou plus compactes, remodelant l’ensemble des gènes que la cellule peut facilement utiliser.
Réarrangeurs de chromatine et marche vers la sénescence
Pour comprendre comment ces modifications de l’emballage de l’ADN apparaissent, les auteurs ont cartographié à la fois les régions de chromatine ouverte et un ensemble d’autres marques d’histones à l’échelle du génome. Lorsque la triméthylation de H3K36 était perdue, de vastes segments d’ADN ont gagné des marques « actives » et sont devenus plus accessibles, en particulier près de gènes liés au métabolisme et au vieillissement. Un acteur clé de cette transition était le complexe remodelant de la chromatine SWI/SNF, animé par une sous-unité centrale appelée SMARCA4. Dans les cellules souches dépourvues de SETD2, les niveaux de SMARCA4 augmentaient, et le complexe semblait contribuer à ouvrir des régions qui activent des programmes de sénescence. Lorsque les chercheurs ont réduit l’activité de SMARCA4 génétiquement ou à l’aide d’un inhibiteur ciblé, les cellules souches ont récupéré une partie de leur capacité à former de mini-intestins sains en culture, et les marqueurs de vieillissement ont diminué — suggérant qu’un remodelage excessif pousse ces cellules vers un état fatigué et sénescent.
Réanimer les voies énergétiques pour sauver les cellules souches
Parce que la perturbation de l’oxydation des graisses est apparue comme un problème central, l’équipe a testé si stimuler cette voie pouvait contrer le vieillissement des cellules souches. Ils ont utilisé un médicament qui active PPARα, un régulateur majeur de l’oxydation des acides gras. Dans des organoïdes issus de cellules souches déficientes en SETD2, ce traitement a augmenté la croissance, restauré les bourgeonnements caractéristiques de cellules souches vigoureuses et réduit l’accumulation de lipides. Chez des souris vivantes, la même intervention a partiellement reconstitué le réservoir de cellules souches, diminué les marqueurs de sénescence et normalisé l’accumulation lipidique dans les cryptes intestinales. Ces résultats placent l’oxydation des acides gras comme un lien cruciale entre le contrôle épigénétique et la santé des cellules souches.
Ce que cela signifie pour un vieillissement en bonne santé
Dans l’ensemble, le travail montre qu’une marque histone spécifique, déposée par SETD2, aide à maintenir un paysage épigénétique équilibré dans les cellules souches intestinales. Lorsque cette marque s’estompe, la chromatine est anormalement remodelée, les voies de combustion des graisses faiblissent, les lipides s’accumulent et les cellules dérivent vers la sénescence, affaiblissant le système de réparation de l’intestin. En réduisant l’activité excessive des machines de remodelage ou en restaurant le métabolisme lipidique avec des médicaments ciblés, il pourrait être possible de préserver la fonction des cellules souches et la santé intestinale à un âge avancé. Bien que ces résultats proviennent de souris, ils font écho à des schémas observés dans des affections intestinales humaines, ce qui ouvre la possibilité que des thérapies métaboliques finement réglées puissent un jour aider à contrer le déclin lié à l’âge dans nos propres cellules souches intestinales.
Citation: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Mots-clés: cellules souches intestinales, épigénétique, oxydation des acides gras, sénescence cellulaire, SETD2