Clear Sky Science · fr
Un ARN lié à Lamp2a sécrété par des CSEAd empêche la rétroaction ENO1–lactylation–glycolyse et le comportement malin des cellules dans le cancer du sein triple négatif
Pourquoi c’est important pour les patient·e·s
Le cancer du sein triple négatif est l’une des formes les plus agressives de cancer du sein et il est dépourvu des cibles hormonales ou de facteurs de croissance qui rendent d’autres sous-types plus faciles à traiter. Cette étude révèle comment ces tumeurs réorganisent leur utilisation de l’énergie pour survivre en milieu pauvre en oxygène et décrit une façon ingénieuse d’attaquer ce rééquipement. Pour les lecteur·rice·s, elle offre un aperçu de la façon dont la compréhension du métabolisme du cancer peut conduire à de nouvelles thérapies très ciblées, distinctes de la chimiothérapie traditionnelle.
Comment ces tumeurs s’alimentent
Beaucoup de cancers comptent fortement sur une voie de production d’énergie rapide mais inefficace appelée glycolyse, qui transforme le sucre en sous-produit lactate. En examinant des échantillons de patient·e·s, des bases de données génétiques publiques et plusieurs lignées cellulaires du sein, les chercheur·se·s montrent que les tumeurs triple négatif s’appuient encore davantage sur la glycolyse que les autres cancers du sein. Une enzyme clé de cette voie, ENO1, est présente à des niveaux particulièrement élevés dans ces tumeurs et est associée à une survie plus mauvaise. Lorsque les niveaux d’ENO1 étaient réduits dans des cellules triple négatif cultivées en laboratoire, les cellules se détournaient de la glycolyse au profit d’une production d’énergie plus normale dans les mitochondries, croissaient plus lentement et étaient moins capables d’envahir ou de former des colonies.
Une boucle de rétroaction dangereuse à l’intérieur des cellules cancéreuses
En creusant davantage, l’équipe a découvert que le lactate lui-même renforce ENO1 et enferme les cellules cancéreuses dans un cercle vicieux. Le lactate peut modifier chimiquement des protéines dans un processus appelé lactylation. Dans les cellules triple négatif, un excès de lactate augmentait la lactylation d’ENO1, ce qui à son tour renforçait l’activité et la stabilité de l’enzyme, accélérant encore la glycolyse et produisant encore plus de lactate. En conditions de faible oxygène — typiques des tumeurs solides — cette boucle se renforçait, aidant les cellules cancéreuses à résister à la mort cellulaire et à continuer de proliférer. Bloquer l’activité d’ENO1 avec un inhibiteur de petite molécule, ou réduire la production de lactate, affaiblissait cette boucle, limitait la glycolyse et ralentissait la croissance tumorale chez la souris.
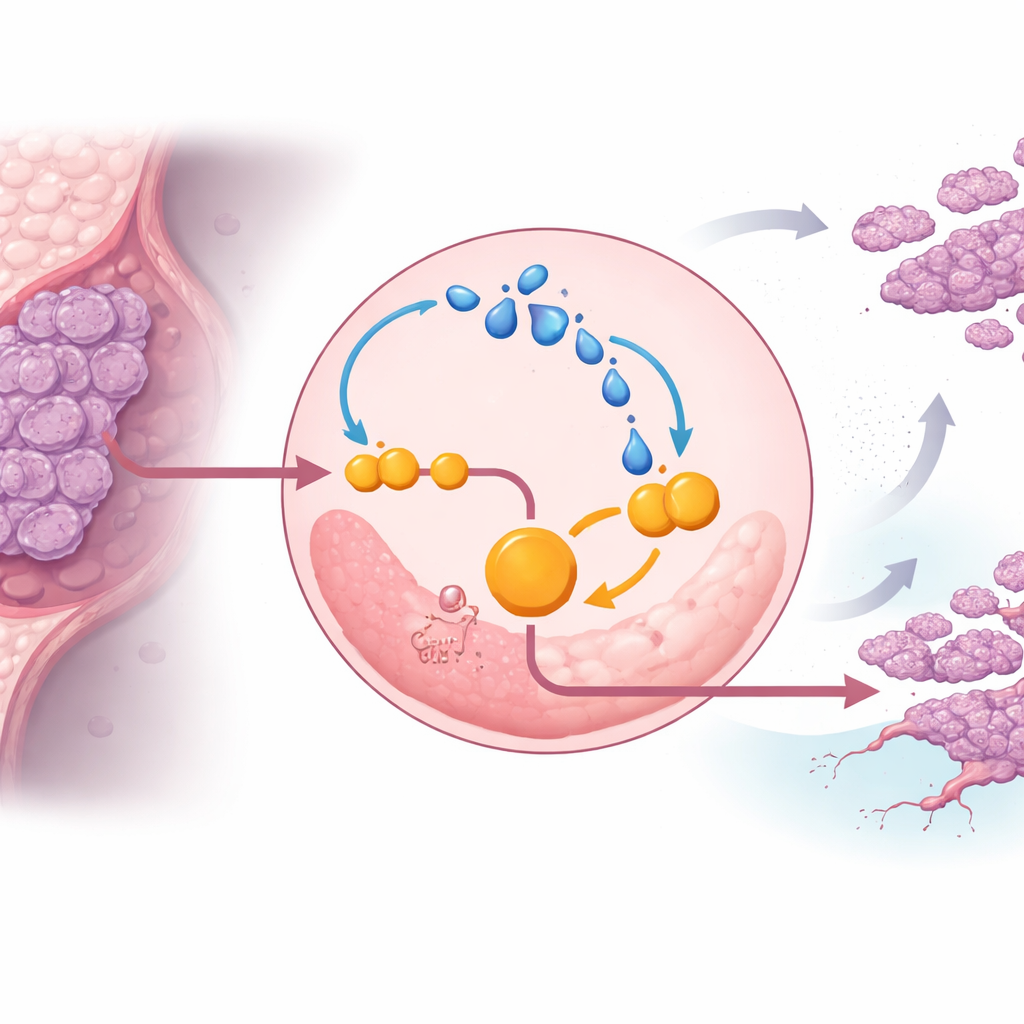
Le commutateur moléculaire qui protège ENO1
L’étude a identifié un point de contrôle spécifique sur ENO1 qui rend cette boucle possible. Une protéine connue sous le nom d’EP300 ajoute des marques à base de lactate sur plusieurs résidus lysine d’ENO1, un site en particulier, appelé K262, s’avérant crucial. Lorsque ce site était muté de sorte qu’il ne pouvait plus être lactylé, ENO1 était rapidement dirigé vers les centres de recyclage de la cellule, les lysosomes, et dégradé. Sans cette marque protectrice, les cellules triple négatif perdaient une grande partie de leur élan glycolytique et de leur capacité à former des tumeurs et des métastases dans des modèles animaux. Cela désigne la lactylation d’ENO1 en K262 comme un commutateur moléculaire qui protège l’enzyme de la destruction et soutient le métabolisme altéré du cancer.
Une nouvelle manière de marquer ENO1 pour la destruction
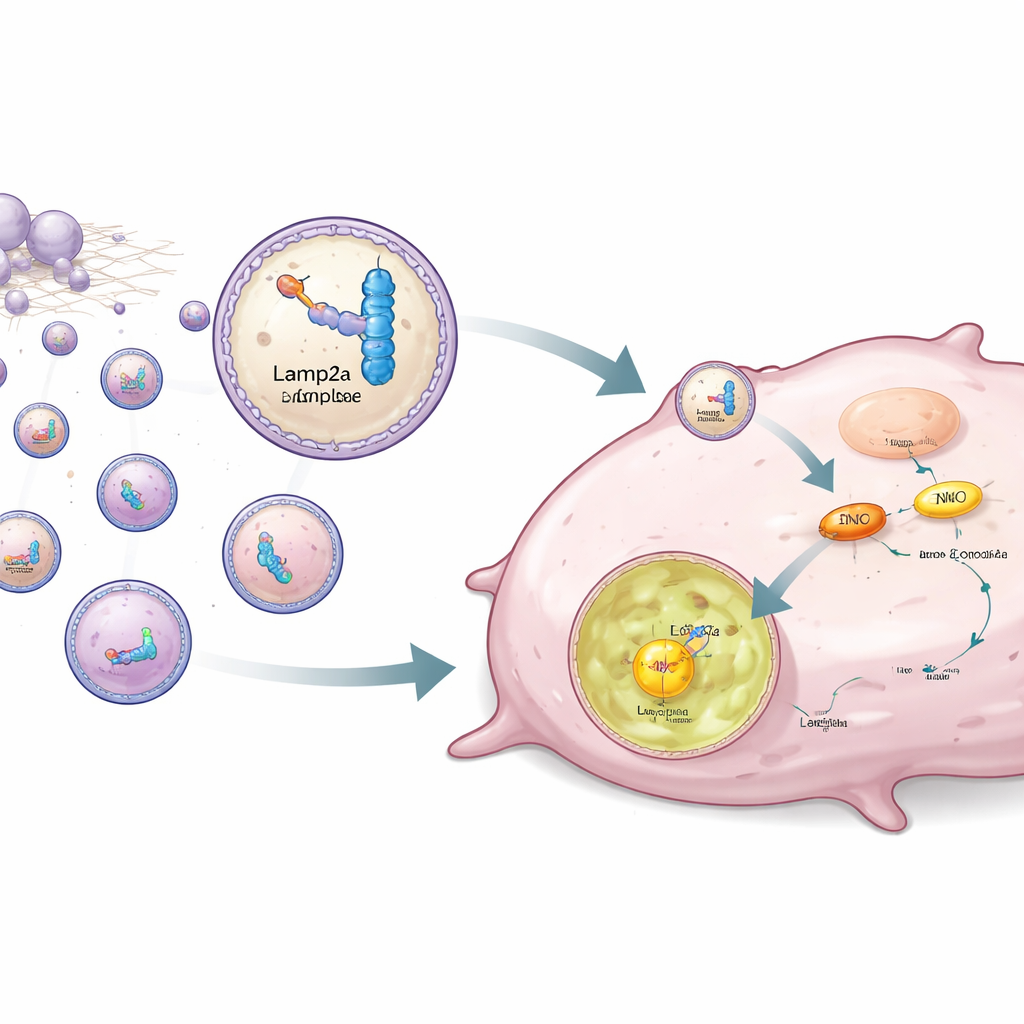
Plutôt que de se contenter de bloquer ENO1, les auteur·rice·s ont conçu une stratégie pour l’éliminer sélectivement des cellules cancéreuses. ENO1 agit aussi comme une protéine liant l’ARN, reconnaissant des courtes séquences ARN spécifiques. L’équipe a conçu des fragments d’ARN synthétiques qui se lient fortement à ENO1, puis les a liés à Lamp2a, une protéine de la membrane lysosomale impliquée dans la dégradation ciblée des protéines. Des cellules souches dérivées de tissu adipeux humain ont été génétiquement modifiées pour produire cette paire ARN–Lamp2a et pour l’emballer dans de petites vésicules appelées exosomes. Lorsque ces exosomes modifiés étaient ajoutés à des cellules triple négatif, la portion ARN s’accrochait à ENO1, tandis que la partie Lamp2a guidait l’ensemble du complexe vers les lysosomes, où ENO1 était dégradé même s’il portait la marque lactylation stabilisante.
Tester l’approche de dégradation ciblée chez l’animal
Pour rapprocher cette idée d’une thérapie pratique, les chercheur·se·s ont cultivé les cellules souches modifiées sur un échafaudage biodégradable et implanté ce dispositif sous la peau de souris, à proximité de tumeurs triple négatif. Depuis cet emplacement, les cellules souches libéraient en continu des exosomes portant les complexes ciblant ENO1. Les tumeurs de ces souris présentaient des niveaux d’ENO1 protéique nettement plus bas, une glycolyse réduite, moins de cellules en division et davantage de signes de mort cellulaire comparé aux animaux témoins. Les tumeurs croissaient plus lentement et leur comportement malin était clairement atténué, démontrant que diriger ENO1 vers les lysosomes peut effectivement priver le cancer de sa voie énergétique préférentielle.
Ce que cela pourrait signifier pour les traitements futurs
Pour un public non spécialiste, le message clé est que ce travail révèle à la fois une faiblesse et un nouvel angle thérapeutique potentiel pour le cancer du sein triple négatif. La faiblesse est la dépendance de la tumeur à une boucle énergétique auto-renforçante centrée sur ENO1 et le lactate, notamment dans les régions hypoxiques. L’angle thérapeutique est un système de dégradation ciblée des protéines qui utilise de l’ARN sur mesure et des exosomes dérivés de cellules souches pour traîner ENO1 vers la machinerie d’élimination de la cellule. Bien que loin d’une utilisation clinique, cette approche illustre comment une compréhension approfondie des astuces métaboliques du cancer peut inspirer des thérapies précises visant à neutraliser, plutôt qu’à empoisonner simplement, les cellules malignes.
Citation: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Mots-clés: cancer du sein triple négatif, métabolisme du cancer, signalisation par le lactate, dégradation ciblée des protéines, enzyme ENO1