Clear Sky Science · fr
La phosphatase Shp1 régule la stabilité de la protéine CXCR2 et l’invasivité médiée par IL8 dans le cancer du sein
Pourquoi cette recherche est importante pour le cancer du sein
Le cancer du sein reste l’une des principales causes de mortalité par cancer chez les femmes, en grande partie parce que certains tumeurs deviennent invasives et se propagent à des organes distants. Cette étude décrypte comment un signal inflammatoire fréquent dans les tumeurs, appelé IL8, communique avec les cellules du cancer du sein et comment un « frein » moléculaire nommé Shp1 contribue à décider si ces cellules restent en place ou deviennent plus agressives. Comprendre ce bras de fer moléculaire pourrait ouvrir de nouvelles voies pour ralentir ou empêcher la propagation de cancers du sein difficiles à traiter, en particulier les formes triple négatives.
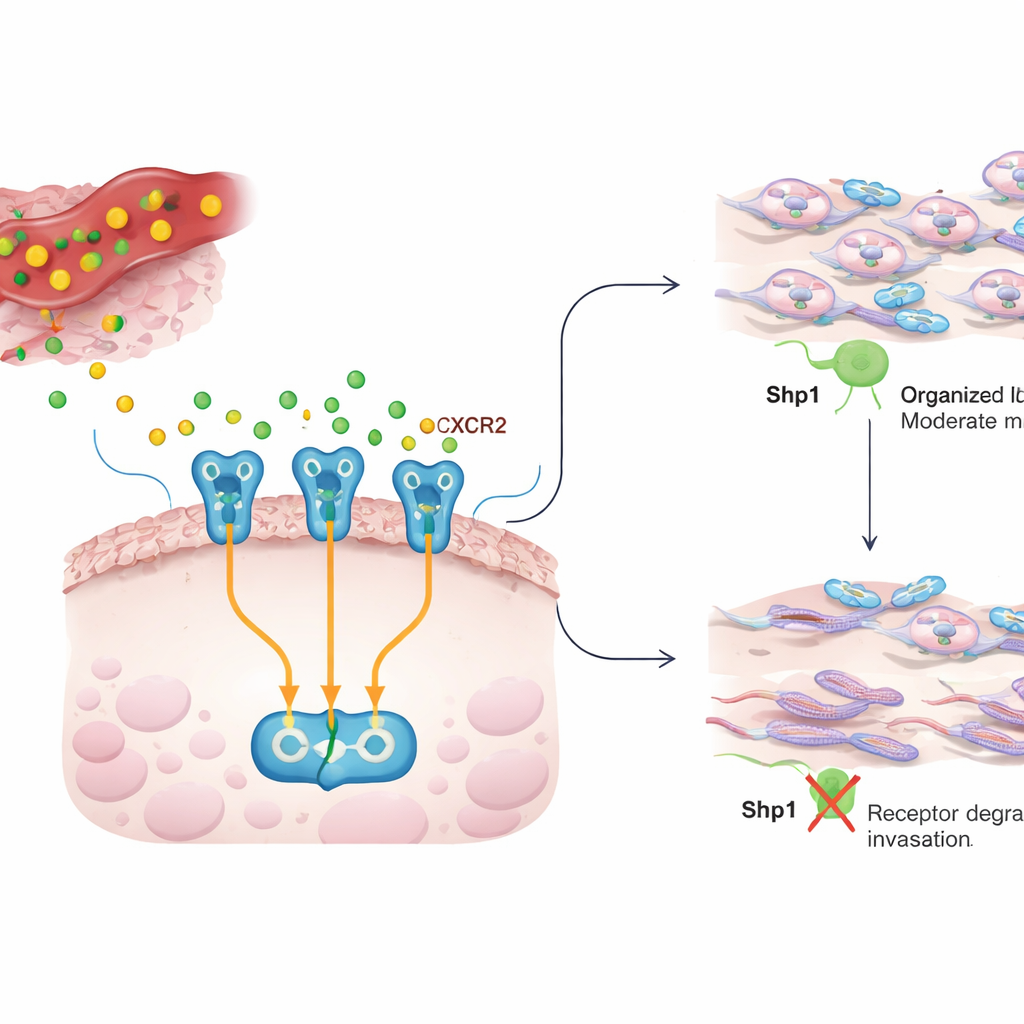
Une conversation entre inflammation et cellules cancéreuses
Au sein d’une tumeur, les cellules cancéreuses sont entourées de cellules immunitaires et de soutien qui libèrent des messagers chimiques, ou cytokines. IL8 est l’un de ces messagers et se trouve souvent à des niveaux élevés dans de nombreux cancers, où il alimente la croissance, la formation de vaisseaux sanguins et la capacité des cellules cancéreuses à se déplacer et à envahir. IL8 agit via un récepteur à la surface des cellules cancéreuses appelé CXCR2. Lorsque IL8 se lie à CXCR2, il active plusieurs circuits internes qui réorganisent le cytosquelette cellulaire, aidant les cellules à ramper à travers les tissus et à se disséminer. Le travail actuel s’interroge sur la façon dont cette conversation IL8–CXCR2 est contenue, et si Shp1, une enzyme généralement considérée comme un frein suppresseur de tumeur sur les signaux de croissance, module aussi ce comportement invasif.
Le rôle caché de Shp1 dans le mouvement cellulaire
Les chercheurs ont d’abord supprimé ou bloqué chimiquement Shp1 dans une lignée cellulaire du cancer du sein luminal largement utilisée (MCF7) et ont mesuré la capacité des cellules à migrer et à envahir à travers un gel imitant le tissu. En l’absence de Shp1, les cellules cancéreuses refermaient les blessures plus rapidement et traversaient le gel deux à trois fois plus efficacement, ce qui révèle que Shp1 limite normalement le mouvement. À partir de données de patientes, ils ont aussi constaté que les femmes dont les tumeurs exprimaient moins de Shp1 avaient une survie plus mauvaise et un délai avant rechute plus court. Ensemble, ces résultats suggèrent que Shp1 restreint le comportement agressif des cellules du cancer du sein et que la perte de ce frein est associée à des issues cliniques défavorables.
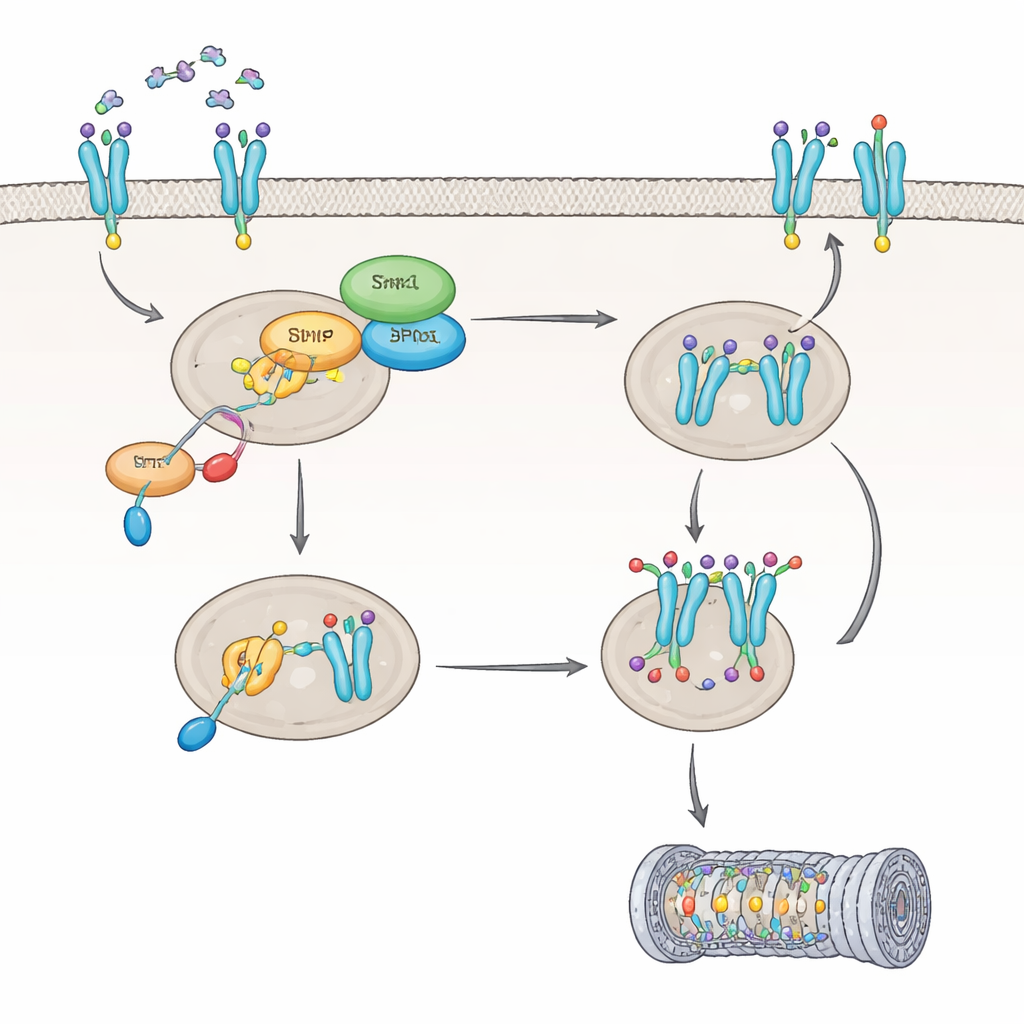
Comment IL8 désactive Shp1 et reprogramme un récepteur clé
Ensuite, l’équipe a étudié comment IL8 affecte Shp1 lui-même. Ils ont découvert qu’IL8 active une protéine appelée PKC, qui marque Shp1 en un site spécifique, réduisant son activité enzymatique d’environ 60 %. Lorsque Shp1 est ainsi atténué, une autre enzyme, PP2A, devient moins active, et le récepteur CXCR2 reste dans un état fortement modifié qui change son devenir à l’intérieur de la cellule. Au lieu d’être nettoyé et recyclé à la surface cellulaire, CXCR2 est étiqueté pour destruction, principalement via la machinerie d’élimination des protéines de la cellule, le protéasome. Une modification particulière de CXCR2, à un acide aminé appelé Ser347, s’est révélée cruciale pour l’attachement de ces étiquettes de dégradation. Dans les cellules dépourvues de Shp1, CXCR2 était davantage marqué et dégradé plus rapidement, entraînant moins de récepteurs à la surface cellulaire et une réponse atténuée à IL8 au fil du temps.
Différents types de cancer du sein, différents branchements
Le cancer du sein n’est pas une maladie unique ; les tumeurs sont regroupées en sous‑types luminal, HER2‑positif et triple négatif en fonction de leurs profils de récepteurs. Les chercheurs ont testé le circuit IL8–CXCR2–Shp1 dans plusieurs lignées cellulaires représentant chaque sous‑type. Dans les cellules luminales et triple négatives, IL8 activait la cascade Shp1–PP2A–CXCR2, et le blocage de Shp1 augmentait à la fois l’invasivité de base et supprimait l’effet pro‑invasif habituel d’IL8. En revanche, les cellules HER2‑positives répondaient toujours à IL8, mais le blocage de Shp1 modifiait peu leur comportement, ce qui suggère que dans ces tumeurs Shp1 est pris dans d’autres signaux, tels que HER2, et moins disponible pour réguler CXCR2. Des analyses d’expression génique à grande échelle soutiennent ce tableau : les lignées triple négatives avaient tendance à présenter moins de Shp1, une signalisation liée aux GPCR altérée et des niveaux d’IL8 plus élevés, cohérents avec un profil plus agressif et conduit par l’inflammation.
Ce que cela signifie pour les traitements futurs
Pour un public non spécialiste, le message central est que l’enzyme Shp1 fonctionne comme un contrôleur du trafic pour le récepteur IL8, CXCR2, déterminant si le récepteur est réutilisé ou détruit et, par conséquent, à quel point les cellules du cancer du sein peuvent répondre aux signaux inflammatoires. Dans les cancers du sein luminal et triple négatif, ce point de contrôle paraît particulièrement important : lorsque les niveaux de Shp1 sont faibles ou que son activité est bloquée, les cellules deviennent plus invasives et le pronostic des patientes se détériore. Parce que Shp1 peut être augmenté ou modulé par certains médicaments existants, cibler l’axe Shp1–CXCR2, éventuellement en association avec des bloqueurs d’IL8 ou de CXCR2, pourrait offrir une nouvelle stratégie pour limiter l’invasion et les métastases dans les sous‑types de cancer du sein agressifs.
Citation: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Mots-clés: invasion du cancer du sein, signalisation IL8, récepteur CXCR2, phosphatase Shp1, cancer du sein triple négatif