Clear Sky Science · fr
CRMP2 inhibe la formation de métastases en altérant la stabilisation dépendante d’ILF3 de l’ARNm de CXCL10 dans le cancer du sein
Pourquoi il est crucial d’arrêter la propagation du cancer
La plupart des décès liés au cancer du sein ne sont pas causés par la tumeur primaire, mais par des cellules cancéreuses qui migrent vers des organes vitaux comme les poumons et y forment de nouvelles lésions. Cette étude met en lumière une protéine protectrice intrinsèque aux cellules du cancer du sein capable de ralentir voire d’empêcher cette dissémination en modifiant le « tapis d’accueil » que les organes distants préparent pour ces cellules errantes. Comprendre cet interrupteur de sécurité caché pourrait ouvrir la voie à de nouveaux traitements qui empêchent le cancer de s’implanter ailleurs dans l’organisme.
Un défenseur discret à l’intérieur des cellules cancéreuses
Les chercheurs se sont intéressés à une protéine appelée CRMP2, surtout connue pour aider les neurones à croître et à maintenir leur cytosquelette. En analysant de larges bases de données publiques sur le cancer et des échantillons tumoraux de patients, ils ont constaté que les niveaux de CRMP2 étaient anormalement faibles dans les tumeurs mammaires, en particulier dans les cancers ayant déjà métastasé. Les patientes dont les tumeurs conservaient des quantités plus élevées de CRMP2 vivaient en moyenne plus longtemps et développaient moins fréquemment des métastases à distance. Ce schéma suggère que CRMP2 agit plutôt comme un frein que comme un accélérateur dans le cancer du sein, se comportant comme un défenseur interne plutôt que comme un moteur de la maladie.
Comment les poumons sont préparés pour l’invasion
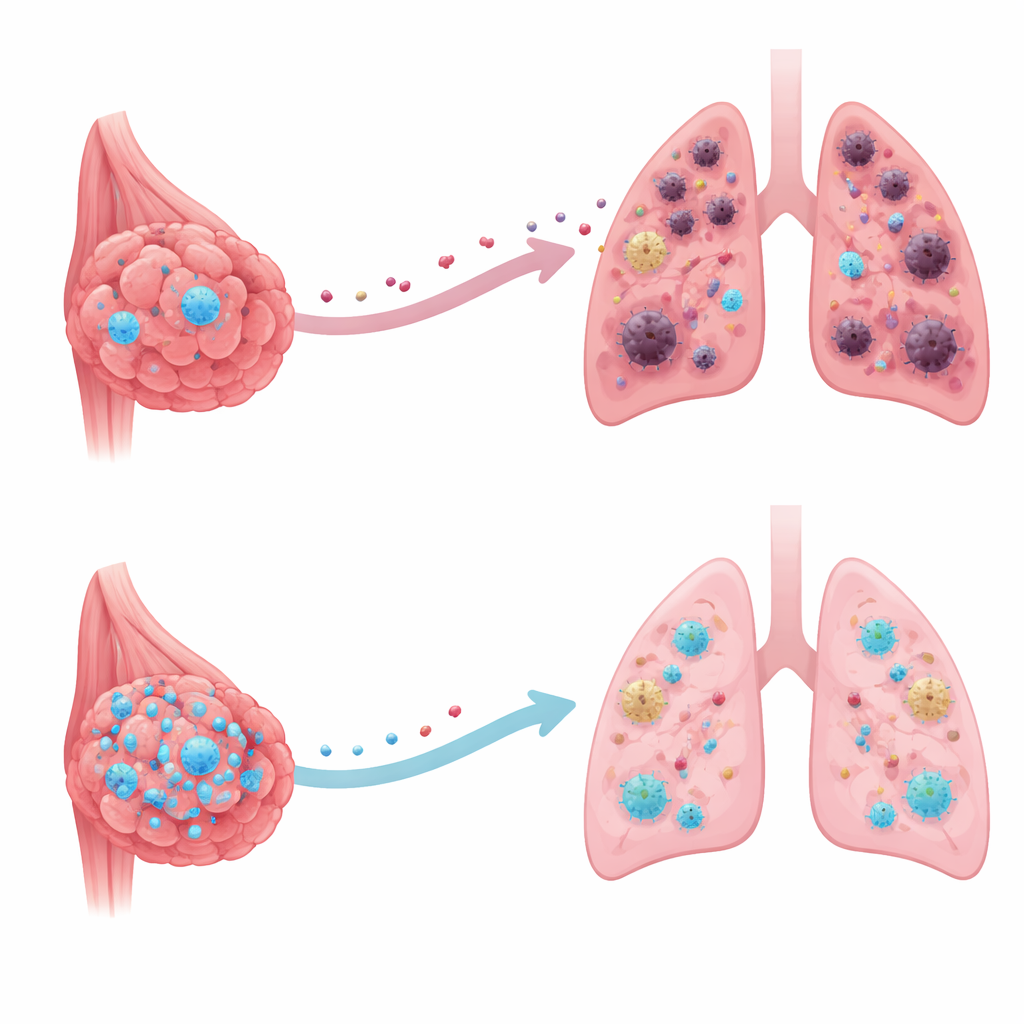
Les cellules cancéreuses n’arrivent que rarement par surprise dans un organe distant. Bien avant leur arrivée, la tumeur primaire libère des molécules qui reconfigurent cet organe en ce que les scientifiques appellent une « niche pré‑métastatique » — un microenvironnement favorable à la survie des cellules cancéreuses. À l’aide d’un modèle murin bien établi qui reproduit fidèlement le cancer du sein humain, l’équipe a montré que lorsque les cellules tumorales mammaires étaient modifiées pour produire du CRMP2 en excès, les tumeurs primaires croissaient à la même vitesse, mais les poumons devenaient beaucoup moins hospitaliers. Les marqueurs d’inflammation et de remodelage tissulaire dans les poumons diminuaient, et moins de cellules immunitaires habituellement impliquées dans la suppression des défenses antitumorales étaient recrutées. En conséquence, après ablation de la tumeur principale, beaucoup moins de nodules métastatiques se formaient dans les poumons.
Une chaîne de signalisation qui déclenche les ennuis
Pour creuser davantage, les scientifiques ont cherché quels signaux sécrétés par la tumeur préparaient les poumons. Ils ont ciblé CXCL10, une petite protéine messagère (chimiokine) connue pour attirer certaines cellules immunitaires et réveiller des cellules cancéreuses dormantes. Dans des cellules de cancer du sein humaines et murines cultivées en laboratoire, l’augmentation de CRMP2 réduisait fortement la quantité de CXCL10 produite et libérée. Chez la souris, les poumons exposés à du matériel tumoral riche en CRMP2 présentaient beaucoup moins de CXCL10 et moins de cellules immunitaires entrant en provenance qui freinent habituellement l’activité protectrice des cellules T. Lorsque les chercheurs bloquaient CXCL10 avec un anticorps, la colonisation pulmonaire par les cellules cancéreuses diminuait ; lorsque qu’ils réintroduisaient du CXCL10, l’effet protecteur de CRMP2 était annulé. CXCL10 se situe donc clairement en aval de CRMP2 en tant que principal instigateur d’une niche favorable aux métastases.
Le médiateur caché qui stabilise les signaux néfastes
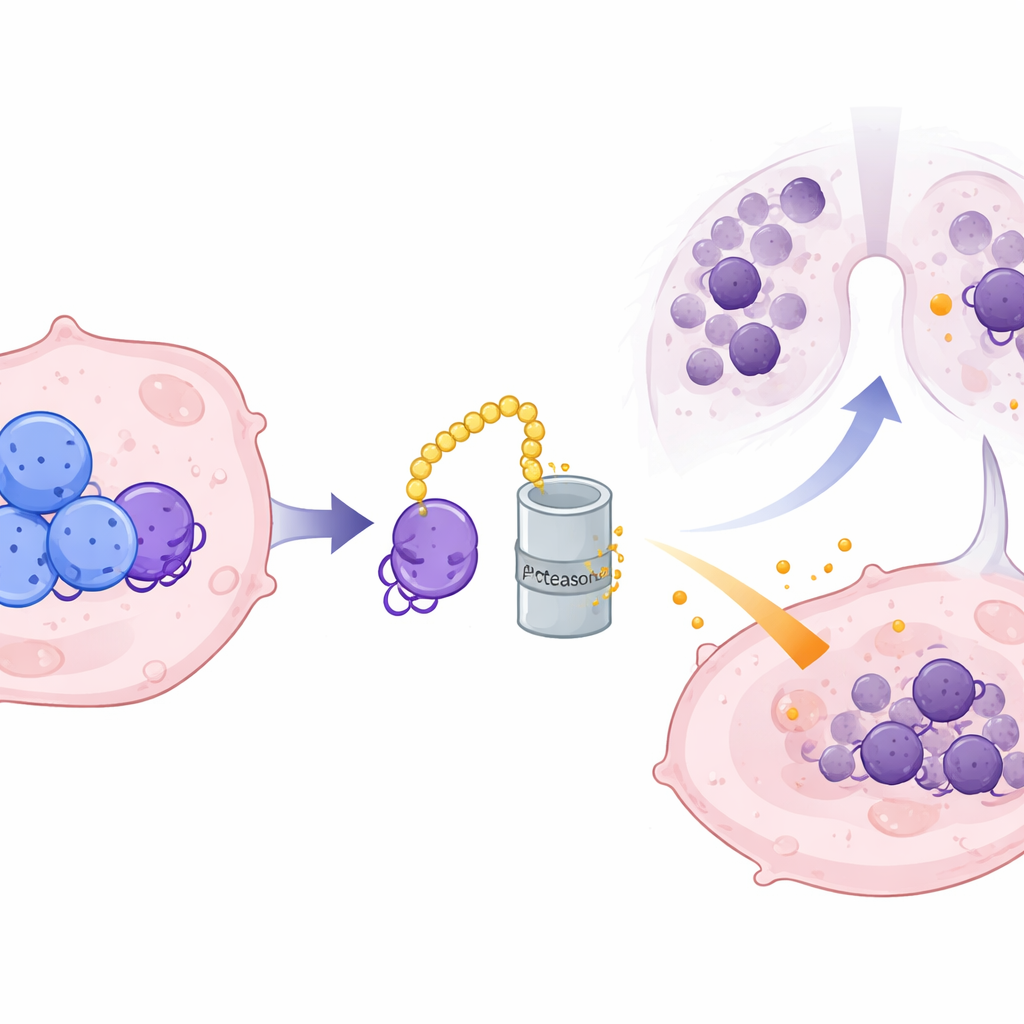
Étant donné que CRMP2 est intracellulaire tandis que CXCL10 est sécrétée, l’équipe a suspecté un médiateur moléculaire. Ils ont identifié ILF3, une protéine liant l’ARN, comme un partenaire direct de CRMP2. ILF3 se fixe à l’ARN codant CXCL10 et le protège normalement de la dégradation, permettant la production d’une plus grande quantité de protéine CXCL10. CRMP2 se lie à ILF3 à des points de contact spécifiques et le marque pour destruction via la machinerie de recyclage des protéines de la cellule, raccourcissant la durée de vie d’ILF3 et rompant son emprise sur l’ARN de CXCL10. Lorsque les niveaux de CRMP2 sont élevés, ILF3 est dégradé plus rapidement, l’ARN de CXCL10 devient instable et moins de chimiokine inflammatoire est sécrétée. Lorsque ILF3 était rétabli artificiellement, il pouvait outrepasser la suppression de CXCL10 par CRMP2, confirmant son rôle de lien crucial dans cette chaîne.
Transformer un composé végétal en allié potentiel
Pour tester si cette voie pouvait être exploitée thérapeutiquement, les chercheurs ont criblé une bibliothèque de composés naturels et découvert que la psoralène — une molécule d’origine végétale utilisée depuis longtemps dans des traitements cutanés — se lie directement à CRMP2 et le rend plus stable. Dans des expériences cellulaires, la psoralène augmentait les niveaux de CRMP2, abaissait ILF3 et CXCL10, et réduisait le comportement invasif des cellules du cancer du sein sans nuire à leur viabilité générale. Dans plusieurs modèles murins, la psoralène ne réduisait pas la taille des tumeurs mammaires primaires, mais elle diminuait fortement les métastases pulmonaires et atténuait la formation de la niche pré‑métastatique, encore une fois d’une manière dépendante de CRMP2. Bien que la psoralène elle‑même puisse provoquer une toxicité hépatique et nécessite des améliorations, ces résultats montrent que de petites molécules peuvent renforcer le rôle protecteur de CRMP2.
Ce que cela signifie pour les patientes
Dans l’ensemble, ce travail révèle un axe protecteur au sein des cellules du cancer du sein dans lequel CRMP2 déstabilise ILF3, ce qui à son tour diminue CXCL10 et empêche les poumons de devenir un terreau fertile pour les métastases. Plutôt que d’attaquer directement les cellules cancéreuses, cette stratégie vise à désarmer les niches distantes dont elles dépendent, faisant pencher la balance en faveur des défenses naturelles de l’organisme. Bien qu’il reste beaucoup à faire avant qu’une telle approche n’atteigne la clinique, cibler la voie CRMP2–ILF3–CXCL10 — éventuellement avec des médicaments de type psoralène plus sûrs — offre un nouvel angle prometteur pour empêcher la propagation du cancer du sein.
Citation: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Mots-clés: métastases du cancer du sein, niche pré-métastatique, signalisation des chimiokines, protéines liant l’ARN, thérapeutiques d’origine naturelle