Clear Sky Science · fr
Ubenimex potentialise le blocage de PD-L1 dans le cancer gastrique en se liant de façon compétitive à LAP3 avec UBE3A
Pourquoi cette recherche est importante
Pour de nombreuses personnes atteintes d’un cancer de l’estomac avancé, les médicaments d’immunothérapie modernes qui « enlèvent les freins » du système immunitaire ont apporté un nouvel espoir — mais ils ne bénéficient toujours qu’à une minorité de patients. Cette étude pose une question pratique à fort impact clinique : un médicament immunostimulant ancien, l’Ubenimex, peut-il être réutilisé pour améliorer l’efficacité de ces traitements, et pourquoi cela fonctionnerait-il ? Les chercheurs dévoilent une astuce moléculaire cachée utilisée par les tumeurs pour échapper à l’attaque immunitaire et montrent comment l’Ubenimex peut l’inverser, ouvrant la voie à des traitements combinés plus efficaces.
Un nouvel allié pour l’immunothérapie anticancéreuse
Les travaux se concentrent sur le cancer gastrique, une maladie qui reste fréquente et mortelle, en particulier en Chine. Les médicaments bloquant PD-1 ou PD-L1 — des protéines qui atténuent les réponses immunitaires — constituent désormais une colonne vertébrale du traitement. Pourtant, la plupart des patients ne répondent jamais ou rechutent finalement. Les auteurs se sont intéressés à l’Ubenimex, un médicament anciennement approuvé et utilisé en complément de la chimiothérapie et de la radiothérapie, connu pour stimuler les cellules immunitaires. Ils ont voulu savoir si l’association de l’Ubenimex avec des anticorps anti–PD-L1 pourrait rendre les tumeurs plus vulnérables aux lymphocytes T cytotoxiques, les cellules immunitaires qui détruisent directement les cellules cancéreuses.
Tester la combinaison médicamenteuse
En utilisant un modèle murin de cancer gastrique dans lequel les tumeurs étaient génétiquement modifiées pour surproduire une protéine appelée LAP3, l’équipe a traité les animaux par Ubenimex, anti–PD-L1, les deux ou aucun des deux. Chaque traitement pris isolément a réduit la taille des tumeurs, mais la combinaison s’est distinguée : les tumeurs ont régressé complètement chez tous les animaux traités et la survie s’est améliorée davantage que sous blocage de PD-L1 seul. Les analyses immunitaires ont montré que la combinaison augmentait fortement le nombre et l’activité des lymphocytes T CD8 « tueurs », qui libéraient davantage de molécules toxiques et de médiateurs inflammatoires. Fait important, le traitement n’a pas provoqué de dommages hépatiques évidents ni de perte de poids, suggérant que l’approche pourrait être puissante sans être excessivement toxique.
Un interrupteur caché qui protège les tumeurs
Pour comprendre pourquoi l’Ubenimex aidait, les chercheurs se sont concentrés sur LAP3, une enzyme qu’il inhibe. Ils ont constaté que les niveaux de LAP3 étaient plus élevés dans les tumeurs gastriques humaines que dans le tissu gastrique normal et que les patients présentant davantage de LAP3 avaient tendance à avoir une survie plus faible. Dans des échantillons de patients et des tumeurs murines, un LAP3 élevé coïncidait avec un nombre réduit de lymphocytes T CD8 à l’intérieur du cancer, alors que d’autres types cellulaires immunitaires restaient inchangés. Lorsque LAP3 était diminué expérimentalement dans les cellules tumorales, les tumeurs croissaient plus lentement, attiraient davantage de lymphocytes T CD8 et devenaient plus faciles à éliminer par ces cellules dans des tests en laboratoire. Ensemble, les données suggèrent que LAP3 n’est pas un simple témoin mais un promoteur actif de l’échappement immunitaire.
Comment les tumeurs utilisent LAP3 pour maintenir les freins
En creusant plus avant, l’équipe a découvert comment LAP3 protège les cellules tumorales contre l’attaque immunitaire. Ils ont montré que LAP3 aide à stabiliser PD-L1, la protéine « frein » clé à la surface des cellules cancéreuses qui met hors service les lymphocytes T. Normalement, PD-L1 peut être marquée par de petites étiquettes protéiques qui l’orientent vers les mécanismes d’élimination de la cellule. Une enzyme appelée UBE3A ajoute ces marques, conduisant à la dégradation de PD-L1. LAP3 se lie physiquement à UBE3A et, ce faisant, empêche UBE3A de marquer PD-L1. Par conséquent, PD-L1 s’accumule à la surface tumorale, formant un bouclier protecteur contre les lymphocytes T CD8. Lorsque les niveaux de LAP3 diminuent, ou lorsque son action est bloquée, PD-L1 est davantage marqué, dégradé plus rapidement et ses niveaux de surface chutent — permettant aux T de s’approcher et d’attaquer.
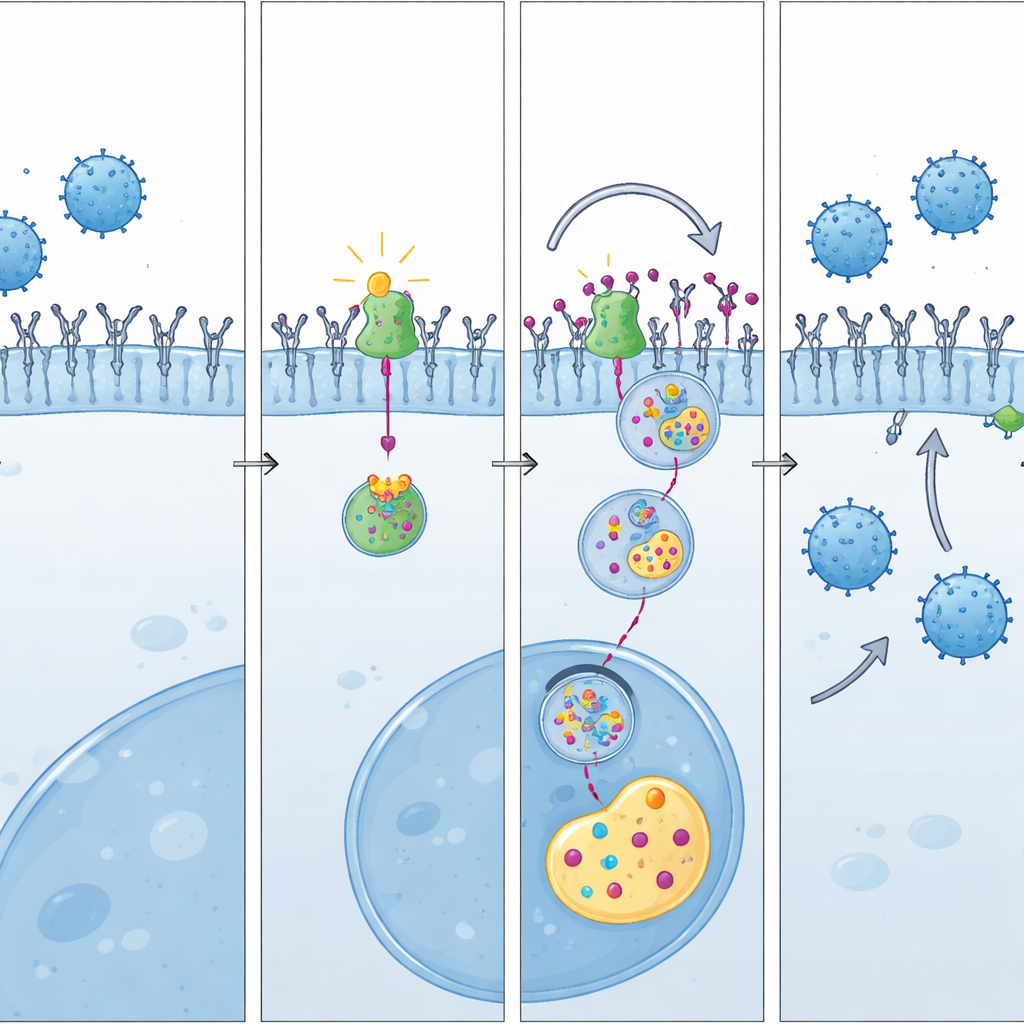
Comment l’Ubenimex renverse l’équilibre
L’étude montre ensuite que l’Ubenimex agit en perturbant le partenariat LAP3–UBE3A. La modélisation informatique et des expériences biochimiques indiquent que l’Ubenimex se loge dans LAP3 au même endroit où LAP3 interagit normalement avec UBE3A. Cette liaison compétitive éloigne UBE3A de LAP3, le libérant pour marquer PD-L1 en vue de sa destruction. Dans des expériences cellulaires, l’Ubenimex a réduit PD-L1 à la surface tumorale, augmenté le marquage de PD-L1 pour son élimination et inversé les effets d’élévation de PD-L1 induits par un excès de LAP3. Chez la souris vivante, ce changement moléculaire s’est traduit par davantage de lymphocytes T CD8 actifs et un contrôle tumoral spectaculaire lorsque l’Ubenimex était associé au blocage de PD-L1.
Ce que cela signifie pour les patients
Au total, l’étude dresse un tableau clair : de nombreuses tumeurs gastriques surproduisent LAP3, ce qui les aide à maintenir des niveaux élevés de PD-L1 et donc à se cacher du système immunitaire. L’Ubenimex brise cette protection en bloquant l’emprise de LAP3 sur UBE3A, permettant ainsi l’élimination de PD-L1. Avec moins de freins à la surface des cellules cancéreuses, les médicaments bloquant PD-L1 et les lymphocytes T tueurs peuvent agir ensemble beaucoup plus efficacement. Parce que l’Ubenimex est déjà utilisé en clinique et que LAP3 peut être mesuré dans des échantillons tumoraux, cette recherche fournit une stratégie concrète et testable pour améliorer l’immunothérapie dans le cancer de l’estomac et potentiellement dans d’autres cancers présentant une élévation de LAP3.
Citation: Zhao, C., Li, J., Zheng, J. et al. Ubenimex synergizes with the PD-L1 blockade in gastric cancer by competitively binding LAP3 with UBE3A. Cell Death Dis 17, 241 (2026). https://doi.org/10.1038/s41419-026-08509-3
Mots-clés: cancer gastrique, immunothérapie, PD-L1, Ubenimex, LAP3