Clear Sky Science · fr
CCL11 favorise la récidive du carcinome hépatocellulaire après chirurgie en potentialisant des macrophages de type M2 immunosuppresseurs CCR5+ CD206+ et en promouvant l’invasivité tumorale
Pourquoi le cancer du foie peut revenir après une intervention
La chirurgie hépatique est souvent le meilleur espoir pour les personnes atteintes d’un cancer du foie à un stade précoce, mais de nombreux patients voient leur cancer réapparaître quelques années après. Cette étude pose une question simple mais cruciale : la réponse inflammatoire déclenchée par la chirurgie aide‑t‑elle involontairement les cellules cancéreuses résiduelles à croître et à se disséminer ? Les chercheurs se concentrent sur une molécule de signalisation appelée CCL11 et montrent comment une poussée de cette molécule après l’opération peut à la fois affaiblir l’immunité anti‑cancer et rendre les cellules tumorales survivantes plus agressives.
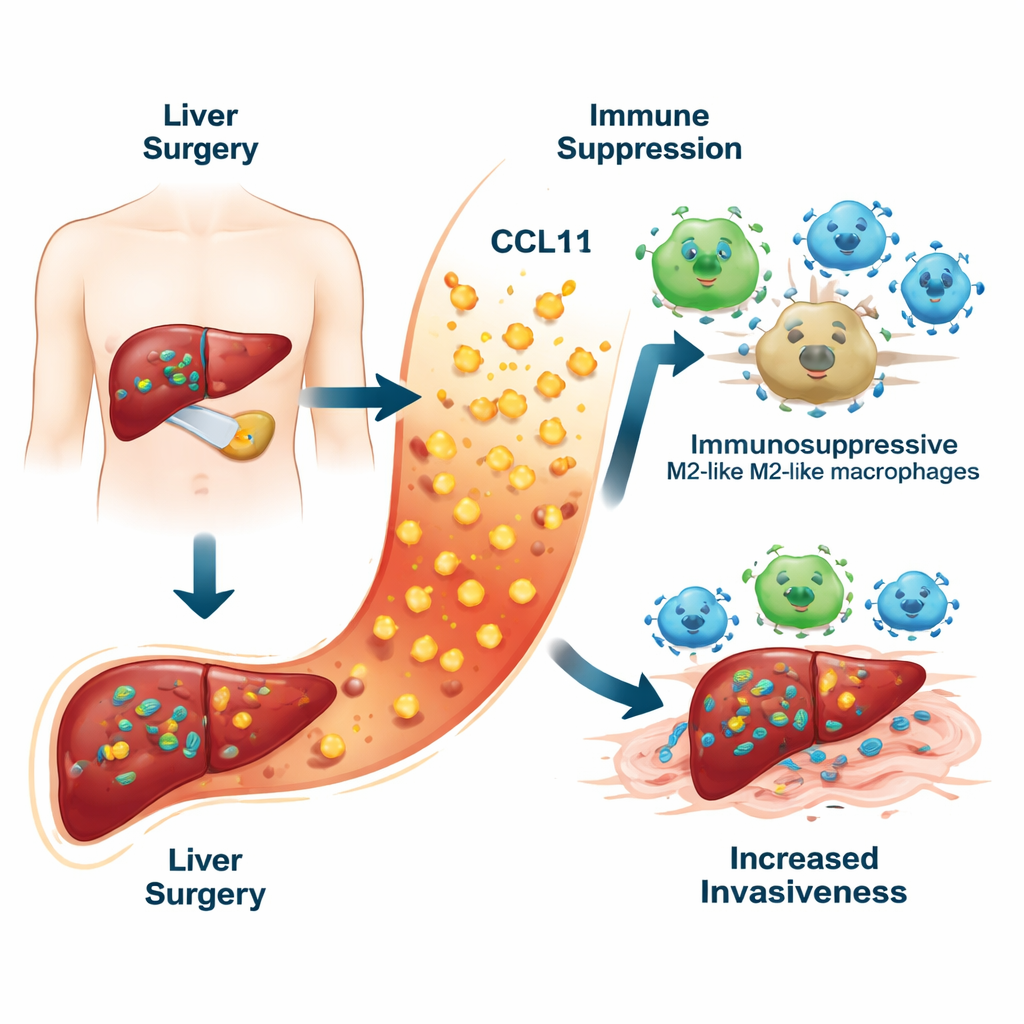
Un danger caché dans la réponse de cicatrisation
Quand les chirurgiens retirent une tumeur hépatique, ils doivent comprimer des vaisseaux sanguins et blesser les tissus environnants. Ces lésions déclenchent une vague d’inflammation qui aide le foie à guérir. En mesurant dix molécules inflammatoires différentes dans le sang des patients une semaine après la chirurgie, l’équipe a constaté qu’une chimiokine, CCL11, se distinguait. Les patients dont le cancer du foie a ensuite récidivé présentaient des niveaux de CCL11 significativement plus élevés que ceux restés indemnes. Des niveaux élevés de CCL11 étaient également associés à une survie plus mauvaise. En combinant CCL11 avec des données cliniques de routine telles que des analyses sanguines et des caractéristiques tumorales, les chercheurs ont construit une « fiche de score » de risque qui prédit la récidive à cinq ans de manière plus précise que les modèles traditionnels.
Le tissu hépatique d’apparence normale compte toujours
La plupart des recherches sur le cancer se concentrent sur la tumeur elle‑même, mais cette étude montre que le tissu hépatique « normal » environnant peut être tout aussi important. Dans des échantillons issus de plus de 100 patients, CCL11 était en réalité plus élevé dans le foie non tumoral que dans les nodules cancéreux ou que dans des foies de donneurs sains. Les patients dont le tissu hépatique adjacent produisait davantage de CCL11 avaient plus de risques d’avoir une maladie avancée, des disséminations à distance et une récidive après chirurgie. Dans des modèles murins reproduisant la brève perte puis le retour du flux sanguin pendant une opération, la lésion hépatique a rapidement fait augmenter les niveaux de CCL11. En conditions de faible oxygénation in vitro, des cellules de soutien du foie comme les myofibroblastes et les cellules endothéliales vasculaires produisaient aussi plus de CCL11, ce qui suggère que le stress chirurgical prépare le reliquat hépatique à devenir un environnement pro‑cancer.
Comment CCL11 transforme des défenseurs immunitaires en spectateurs
Pour comprendre comment CCL11 façonne l’immunité, les auteurs se sont intéressés aux macrophages, des globules blancs polyvalents qui peuvent soit attaquer les tumeurs soit les protéger. Ils ont constaté que, dans le foie non tumoral, des niveaux plus élevés de CCL11 allaient de pair avec une augmentation d’un sous‑type de macrophages exprimant le marqueur CCR5 et présentant un profil dit de type M2, favorable à la tumeur. Chez les patients, des foies riches en ces macrophages CCR5+ de type M2 étaient associés à une survie plus mauvaise. En culture cellulaire, l’ajout de CCL11 poussait les monocytes à devenir ce type de macrophage immunosuppresseur, augmentant des molécules telles que PD‑L1 et IL‑10 et libérant d’autres signaux qui recrutent et orientent davantage les cellules immunitaires. Ces macrophages conditionnés par CCL11 encourageaient ensuite les lymphocytes T auxiliaires naïfs à se convertir en cellules T régulatrices, une population connue pour atténuer les réponses anti‑tumorales. Des expériences mécanistiques ont montré que CCL11 active une chaîne de signaux à l’intérieur des macrophages qui aboutit à la voie NF‑κB et à la production de PD‑L1, contribuant à protéger les cellules cancéreuses des attaques immunitaires.
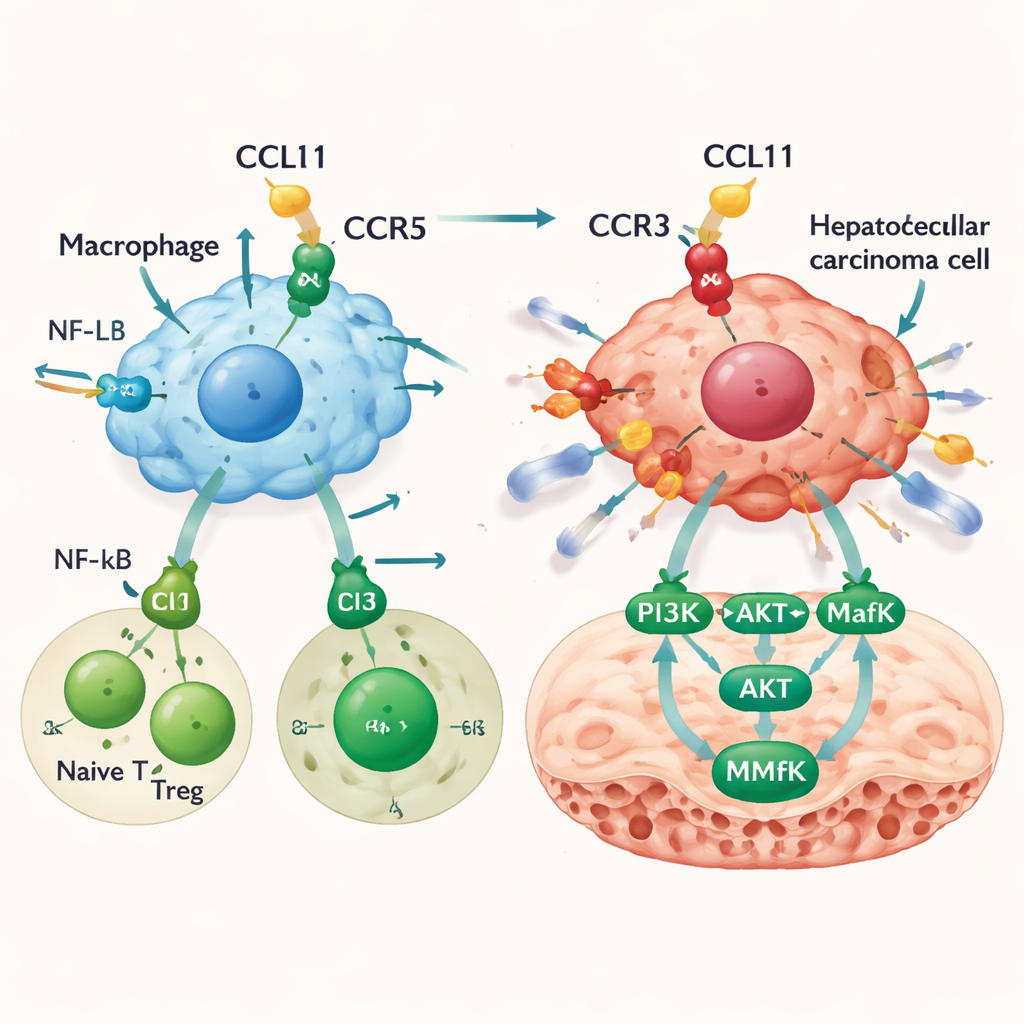
Comment CCL11 rend les cellules tumorales résiduelles plus invasives
CCL11 ne se contente pas de remodeler le paysage immunitaire ; elle agit aussi directement sur les cellules du cancer du foie. Bien que les cellules cancéreuses elles‑mêmes produisent peu de CCL11, elles expriment l’un de ses récepteurs, CCR3. Dans des essais en laboratoire, CCL11 n’accélérait pas la prolifération des cellules hépatiques cancéreuses mais augmentait leur migration et leur capacité d’invasion à travers des barrières, un signe de potentiel métastatique. Le blocage du récepteur CCR3 annulait en grande partie cet effet. Des analyses génomiques ont mis en évidence une voie dans laquelle le signal CCL11–CCR3 active PI3K et AKT, puis un facteur de transcription appelé MafK. MafK accroît à son tour la production de MMP13, une enzyme qui dégrade le tissu environnant et ouvre des voies pour la dissémination tumorale. Dans des modèles murins, l’infusion de CCL11 dans le foie augmentait la charge tumorale et entraînait davantage de métastases, ainsi que des niveaux plus élevés de la voie PI3K–AKT–MafK–MMP13 au sein des tumeurs.
Transformer un signal à risque en opportunité thérapeutique
Parce que CCL11 semble à la fois museler les défenses immunitaires et renforcer les cellules cancéreuses résiduelles, les chercheurs ont testé si le bloquer après chirurgie pouvait modifier les résultats. Chez des souris porteuses de tumeurs hépatiques opérées, un traitement par un anticorps neutralisant CCL11 a réduit de façon spectaculaire le taux de récidive hépatique et amélioré la survie, sans effets secondaires évidents tels que la perte de poids. Pris dans leur ensemble, ces résultats présentent CCL11 comme un interrupteur majeur reliant la lésion chirurgicale à un environnement hépatique immunosuppresseur et propice à l’invasion. Pour les patients, ce travail suggère que la mesure de CCL11 après chirurgie pourrait aider à identifier ceux à plus haut risque de rechute, et que des médicaments ciblant l’axe CCL11–CCR5/CCR3 pourraient un jour faire partie des stratégies pour empêcher la réapparition du cancer du foie.
Citation: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Mots-clés: récidive du cancer du foie, chimiokine CCL11, microenvironnement tumoral, suppression immunitaire, métastase cancéreuse