Clear Sky Science · fr
Le facteur de transcription ZMYM3 favorise la métastase du carcinome hépatocellulaire en régulant à la hausse CTTN et en induisant la formation d’invadopodes
Pourquoi cette étude sur le cancer du foie est importante
Le cancer du foie figure parmi les cancers les plus meurtriers dans le monde, principalement parce qu’il est souvent détecté tardivement et qu’il a une forte propension à se disséminer. Cette étude examine à la fois les tissus et le noyau cellulaire pour poser une question cruciale : qu’est-ce qui rend certains tumeurs hépatiques si efficaces pour se détacher et envahir d’autres parties du corps ? En mettant au jour un moteur moléculaire clé de cette dissémination, les chercheurs ouvrent la voie à de nouvelles approches pour, un jour, mieux prédire les patients à haut risque et concevoir des traitements capables de ralentir ou d’empêcher les métastases.
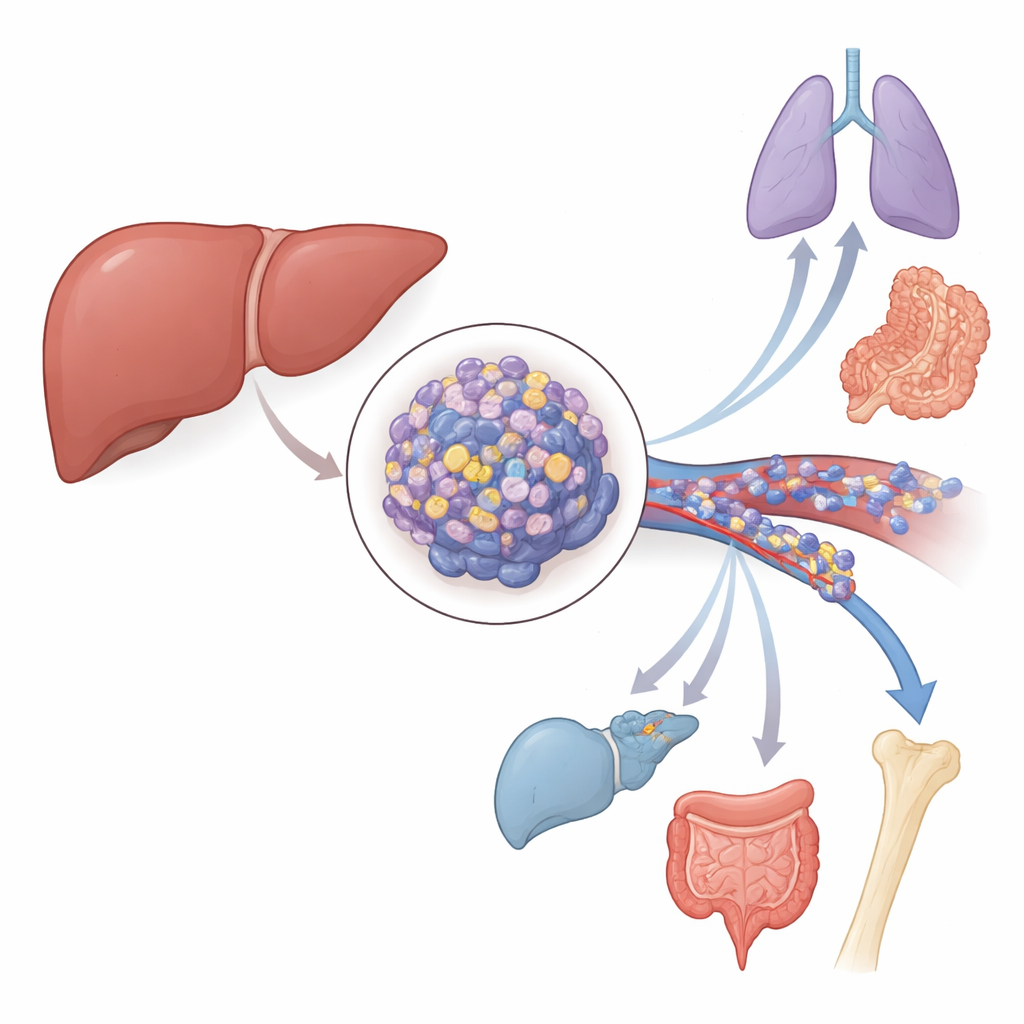
Un interrupteur caché à l’intérieur des tumeurs hépatiques
Les auteurs se sont concentrés sur le carcinome hépatocellulaire, le type le plus fréquent de cancer primitif du foie. En exploitant de grandes bases de données publiques sur le cancer et en analysant des échantillons de tissus de patients, ils ont montré qu’un gène appelé ZMYM3 est beaucoup plus fortement activé dans les tumeurs hépatiques que dans le tissu hépatique sain voisin. Les patients dont les tumeurs présentaient des niveaux élevés de ZMYM3 avaient tendance à avoir une survie globale plus mauvaise et des périodes sans récidive plus courtes. L’équipe a aussi examiné des caillots tumoraux spéciaux formés par des cellules cancéreuses dans la veine porte, un vaisseau majeur qui draine le foie. Dans ces thrombus très invasifs, les niveaux de ZMYM3 étaient encore plus élevés que dans les tumeurs hépatiques d’origine, ce qui relie fortement ce gène à la capacité du cancer d’envahir les vaisseaux sanguins et de se disséminer.
Comment ZMYM3 rend les cellules cancéreuses plus agressives
Pour dépasser les simples corrélations, les scientifiques ont manipulé les niveaux de ZMYM3 dans des lignées cellulaires de cancer du foie. Lorsqu’ils ont réduit ZMYM3, les cellules proliféraient plus lentement, formaient moins de colonies et étaient plus susceptibles de subir la mort cellulaire programmée. À l’inverse, en augmentant ZMYM3, les cellules se divisaient plus rapidement, résistaient davantage à la mort et montraient une meilleure migration et capacité d’invasion à travers des barrières artificielles en laboratoire. Dans des modèles murins, les tumeurs génétiquement modifiées pour surexprimer ZMYM3 étaient plus volumineuses sous la peau et formaient davantage de nodules métastatiques dans les poumons après injection dans la circulation sanguine. Ensemble, ces expériences montrent que ZMYM3 n’est pas seulement un marqueur mais un promoteur actif de la croissance et de la dissémination du cancer du foie.
Envahir en développant de minuscules « pieds »
Une caractéristique frappante des cellules cancéreuses agressives est leur capacité à développer de petites protrusions riches en actine qui creusent et dissolvent les tissus environnants. Ces structures, appelées invadopodes, agissent comme des marteaux-piqueurs cellulaires, aidant les cellules tumorales à percer le réseau de soutien autour des organes et à pénétrer dans les vaisseaux sanguins. Par profilage de l’expression génique, imagerie du cytosquelette et essais fonctionnels, les chercheurs ont montré que ZMYM3 augmente l’expression de nombreux gènes liés aux invadopodes et à un programme plus large de plasticité appelé transition épithélio–mésenchymateuse, qui rend les cellules plus mobiles. Lorsque ZMYM3 est élevé, les cellules du carcinome hépatocellulaire forment davantage d’invadopodes et relâchent leurs attaches aux cellules voisines ; lorsque ZMYM3 est réduit, ces structures et comportements invasifs diminuent.
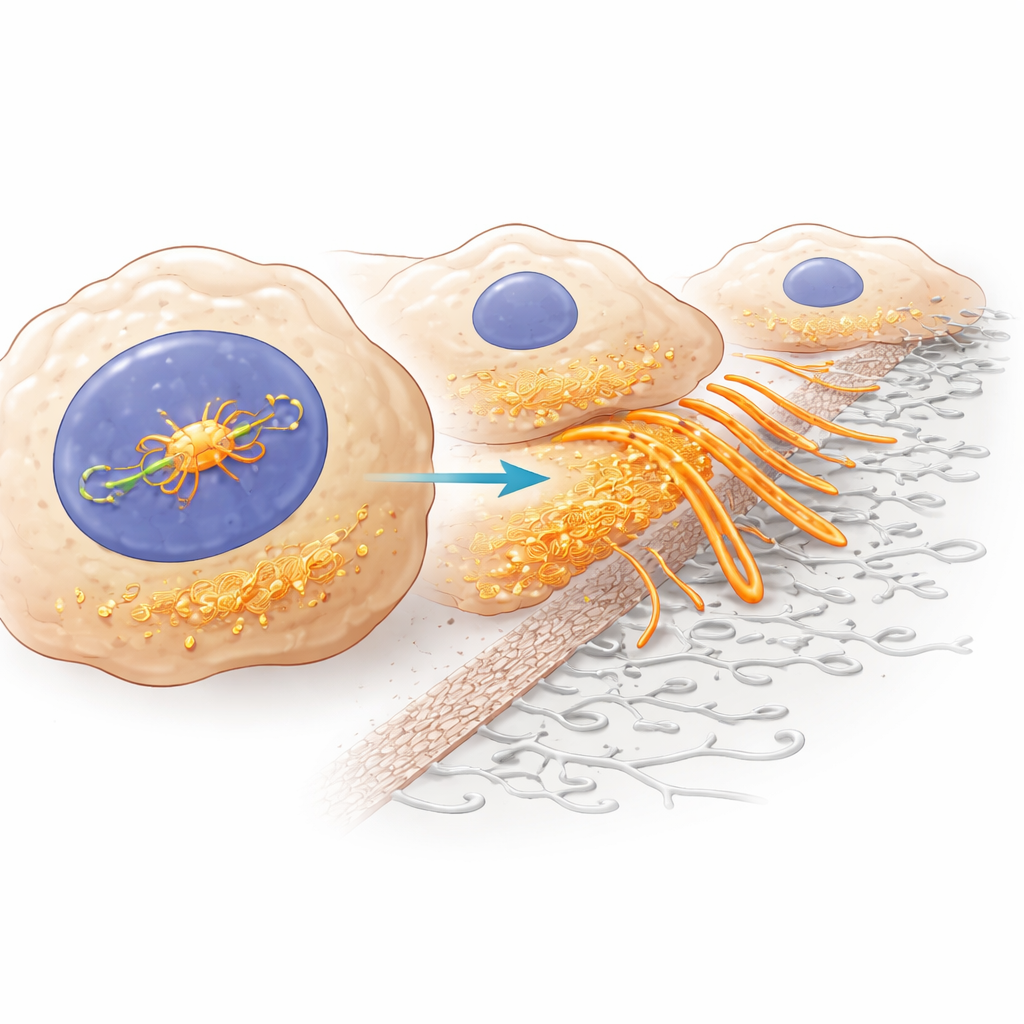
Le partenaire clé : une protéine d’échafaudage appelée cortactine
Pour approfondir le mécanisme, l’équipe a utilisé une technique qui cartographie l’adhésion des protéines à l’ADN à l’échelle du génome. Ils ont découvert que ZMYM3 se lie directement à la région de contrôle d’un autre gène, CTTN, qui code pour la cortactine—un organisateur central des invadopodes. L’activation de cette région augmente la production de cortactine. Dans les données cliniques, la cortactine était également élevée dans les tumeurs hépatiques et associée à de moins bons pronostics, et ses niveaux suivaient ceux de ZMYM3. Lorsque les chercheurs ont diminué la cortactine dans des cellules surexprimant ZMYM3, les cellules cancéreuses perdaient une grande partie de leur surcroît de croissance, de survie, de migration et d’invasion. Cela indique qu’une large part de l’effet de ZMYM3 passe par l’augmentation de la cortactine et, par conséquent, par le renforcement des invadopodes.
Ce que cela signifie pour les patients
Pour un non-spécialiste, le message est que cette étude identifie un « accélérateur » moléculaire—ZMYM3—qui aide les cellules du cancer du foie à croître, à résister à la mort et à forer physiquement leur chemin dans les vaisseaux sanguins et les organes distants. Il agit en grande partie en activant un autre gène, CTTN, qui fournit aux cellules cancéreuses des « pieds » invasifs plus puissants. Parce que des niveaux élevés de ZMYM3 et de cortactine sont associés à la récidive et à une survie plus mauvaise, ils pourraient servir de signaux d’alerte pour identifier les patients à risque élevé de métastases. À plus long terme, des médicaments ciblant cette voie ZMYM3–cortactine, ou la formation d’invadopodes elle-même, pourraient offrir de nouvelles stratégies pour ralentir la propagation du carcinome hépatocellulaire et améliorer les résultats cliniques.
Citation: Zeng, F., Zhang, Z., Hu, T. et al. Transcriptional factor ZMYM3 promotes hepatocellular carcinoma metastasis by upregulating CTTN and inducing invadopodia formation. Cell Death Dis 17, 294 (2026). https://doi.org/10.1038/s41419-026-08506-6
Mots-clés: carcinome hépatocellulaire, métastase, ZMYM3, cortactine, invadopodes