Clear Sky Science · fr
Les fibroblastes associés aux tumeurs favorisent la résistance à l’osimertinib dans les cellules de cancer du poumon non à petites cellules via la modification m7G de NET1 médiée par METTL1
Pourquoi certains cancers du poumon cessent de répondre à un médicament « intelligent »
Les médicaments ciblés comme l’osimertinib ont transformé le traitement de nombreuses personnes atteintes d’un type courant de cancer du poumon, offrant une survie prolongée avec moins d’effets indésirables que la chimiothérapie conventionnelle. Pourtant, pour la plupart des patients, ces bénéfices sont temporaires : les tumeurs finissent par trouver des moyens de déjouer le médicament. Cette étude pose une question apparemment simple mais aux grandes implications : le tissu de soutien de la tumeur — en particulier des cellules appelées fibroblastes associés au cancer — aide‑t‑il discrètement les cellules cancéreuses à échapper aux effets de l’osimertinib ?
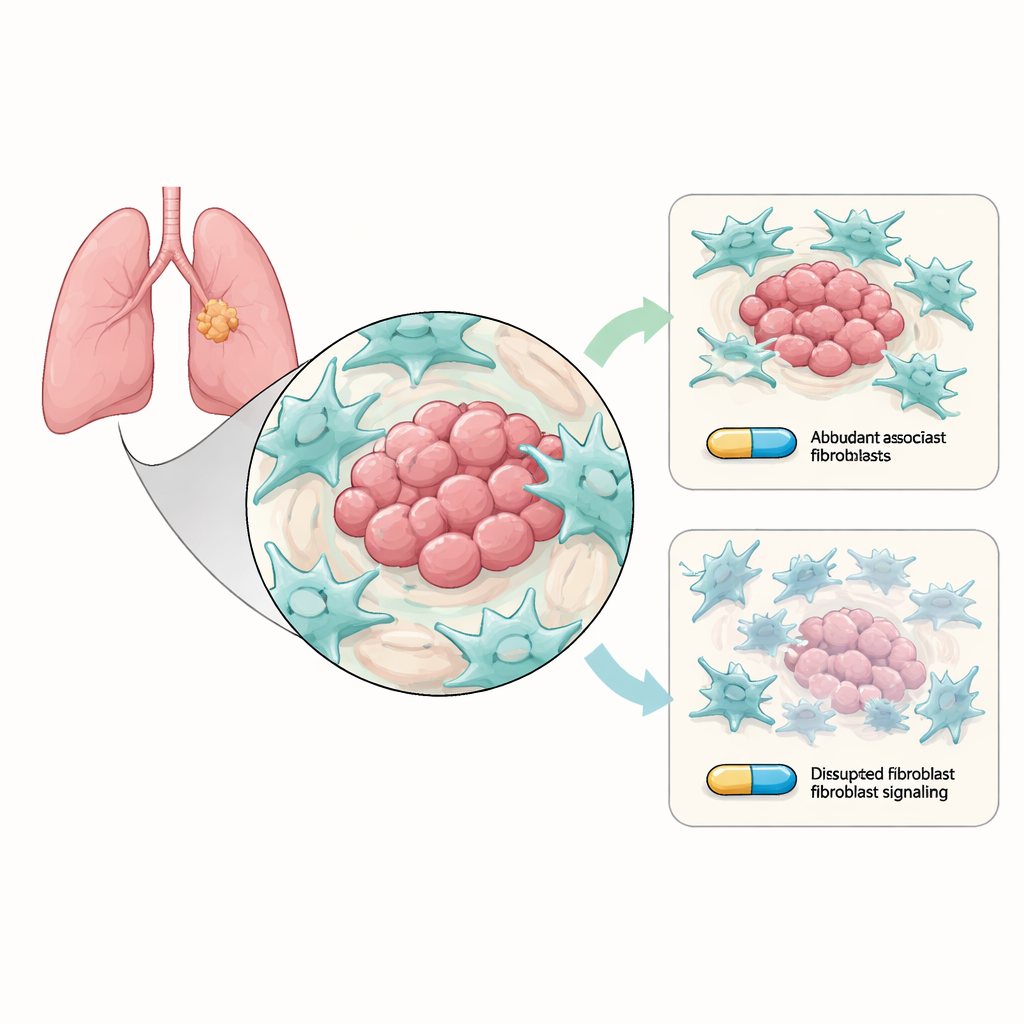
Des cellules aidantes qui protègent secrètement la tumeur
Le cancer du poumon non à petites cellules se développe au sein d’un micro‑environnement tumoral animé, composé de cellules non cancéreuses. Parmi les résidents les plus abondants figurent les fibroblastes associés au cancer (CAF), des cellules du tissu conjonctif qui remodèlent la zone entourant la tumeur. Les chercheurs ont cultivé des cellules de cancer du poumon porteuses des mutations EGFR habituellement sensibles à l’osimertinib avec des CAF en laboratoire. Ils ont constaté que, en présence de CAF, les cellules cancéreuses étaient plus difficiles à éliminer par l’osimertinib : elles formaient davantage de colonies, s’autodétruisaient moins fréquemment et présentaient des traits « de type souche » plus marqués, associés à une survie à long terme et à une rechute. En d’autres termes, bien que le médicament ciblât toujours les cellules cancéreuses, les fibroblastes environnants les aidaient discrètement à durer.
Une étiquette chimique sur l’ARN qui change les règles
L’équipe s’est ensuite intéressée au‑delà des gènes eux‑mêmes, aux marques chimiques qui décorent l’ARN — les copies de travail de l’information génétique à l’intérieur des cellules. Une de ces marques, appelée m7G, peut influencer la stabilité d’un ARN et l’efficacité de sa traduction en protéine. Grâce à des tests biochimiques et un cartographie à l’échelle du génome, les chercheurs ont montré que les CAF augmentent le marquage m7G global sur les ARN à l’intérieur des cellules de cancer du poumon. Cette augmentation était principalement portée par une enzyme méthyltransférase nommée METTL1, qui place les marques m7G sur les ARN messagers. Les niveaux de METTL1 étaient plus élevés dans les tumeurs pulmonaires que dans le tissu normal adjacent et étaient associés à une maladie plus avancée et à une survie des patients plus faible, suggérant que cette enzyme fait plus que peaufiner des fonctions cellulaires de routine.
Un signal sécrété et une chaîne moléculaire vulnérable
Comment les CAF augmentent‑ils METTL1 dans les cellules cancéreuses ? L’étude pointe vers une protéine appelée HMGB1, que les CAF libèrent dans leur environnement. Comparativement aux cellules cancéreuses, les CAF sécrétaient des quantités bien supérieures de HMGB1. Lorsque les chercheurs ont ajouté du HMGB1 aux cellules de cancer du poumon, les niveaux de METTL1 et les marques m7G augmentaient ; lorsqu’ils ont bloqué le HMGB1 dans le milieu conditionné par les CAF, cet effet s’est estompé. En examinant plus précisément, ils ont identifié une cible clé de METTL1 : NET1, un gène qui favorise la croissance et la migration cellulaires. Les CAF augmentaient à la fois le marquage m7G et l’abondance de l’ARN et de la protéine NET1, et METTL1 se liait physiquement à l’ARN de NET1 pour le stabiliser. Moins de METTL1 signifiait moins de NET1 modifié, des signaux de survie des cellules cancéreuses affaiblis et une sensibilité accrue à l’osimertinib.
Activation de voies de survie à l’intérieur des cellules cancéreuses
Le signal NET1 renforcé n’agissait pas seul. En combinant des données d’ARN à grande échelle avec une analyse de voies, les scientifiques ont montré que les CAF activent une voie majeure de croissance et de survie intracellulaire connue sous le nom de voie AKT/NF‑κB. Le blocage d’AKT ou de NF‑κB avec des inhibiteurs spécifiques rendait les cellules de cancer du poumon plus vulnérables à l’osimertinib, même en présence de CAF. La modulation des niveaux de NET1 produisait des effets similaires : réduire NET1 affaiblissait la protection fournie par les CAF, tandis qu’augmenter NET1 renforçait la résistance. Chez des souris implantées avec des cellules humaines de cancer du poumon, l’ajout de CAF rendait les tumeurs plus rapides à croître et moins sensibles à l’osimertinib. L’extinction de METTL1 dans les cellules cancéreuses diminuait les marques m7G, abaissait NET1 et l’activation des voies, et réduisait fortement la croissance tumorale induite par les CAF.
Ce que cela signifie pour le traitement futur du cancer du poumon
Pour les personnes atteintes d’un cancer du poumon mutant EGFR, ce travail propose une nouvelle façon d’envisager pourquoi des médicaments puissants comme l’osimertinib finissent par échouer. Plutôt que d’imputer uniquement la résistance à de nouvelles mutations dans les cellules cancéreuses, il met en lumière une chaîne moléculaire qui commence en dehors de la cellule tumorale — avec des CAF libérant du HMGB1 — et qui passe par METTL1, les marques m7G sur NET1 et l’activation de voies de survie qui atténuent l’impact du médicament. Interrompre cette chaîne à n’importe quel point pourrait, en principe, restaurer ou prolonger la sensibilité au traitement. Bien que les médicaments ciblant directement METTL1, HMGB1 ou des ARN spécifiquement marqués par la m7G soient encore à des stades précoces, l’étude suggère que combiner l’osimertinib avec des thérapies ciblant les cellules de soutien de la tumeur ou leurs signaux de modification de l’ARN pourrait aider à contrôler plus durablement cette forme de cancer du poumon.
Citation: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Mots-clés: résistance à l’osimertinib, cancer du poumon non à petites cellules, fibroblastes associés au cancer, méthylation de l’ARN, voie METTL1 NET1