Clear Sky Science · fr
miR-424(322)~503 entrave la progression du cancer du côlon liée à une déficience en PTEN
Pourquoi cette étude compte pour le cancer du côlon
Le cancer du côlon reste l’un des cancers les plus fréquents et les plus meurtriers dans le monde, et de nombreux patients évoluent vers une maladie avancée malgré la chirurgie, la chimiothérapie et les thérapies ciblées. Cette étude explore un petit ensemble d’« interrupteurs » génétiques appelés microARNs qui peuvent ralentir ou accélérer la croissance tumorale. En révélant comment un cluster précis de microARNs interagit avec un gène suppresseur de tumeurs bien connu, PTEN, ce travail aide à expliquer pourquoi certains cancers du côlon deviennent plus agressifs et suggère de nouvelles pistes pour prédire le risque et concevoir des traitements.
De minuscules interrupteurs ARN au grand impact
Les microARNs sont de courtes molécules d’ARN qui ne codent pas de protéines mais ajustent finement l’utilisation de centaines de gènes dans une cellule. Le cluster miR-424(322)~503, composé de deux microARNs apparentés, a intrigué les chercheurs car il peut agir comme frein ou comme accélérateur selon les cancers. Dans le cancer du côlon, son rôle était jusqu’ici flou. Les auteurs se sont concentrés sur les tumeurs poussées par la perte de PTEN, un gène qui contrôle normalement les signaux de croissance et est fréquemment altéré dans les tumeurs colorectales. Ils ont posé une question simple mais puissante : que se passe-t-il dans le développement du cancer du côlon lorsque PTEN et ce cluster de microARNs sont tous deux absents ?
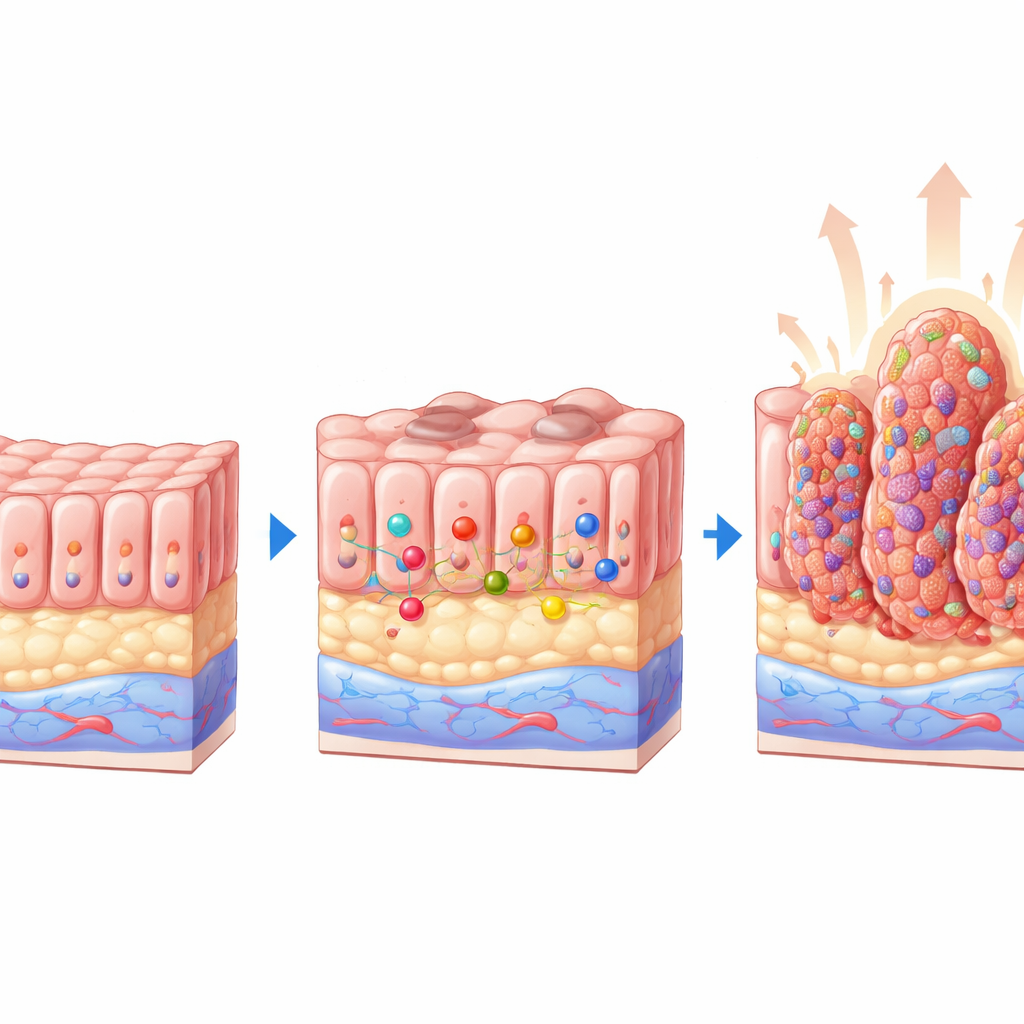
Des modèles murins révèlent un rôle protecteur
Pour répondre à cette question, l’équipe a utilisé des souris génétiquement modifiées où PTEN peut être inactivé dans l’épithélium intestinal, et les a croisées avec des souris dépourvues du cluster miR-424(322)~503. Quatre groupes en ont résulté : animaux normaux, souris dépourvues uniquement des microARNs, souris dépourvues uniquement de PTEN, et souris double knockout dépourvues des deux. Après induction de la perte de PTEN, ils ont examiné attentivement les côlons. Les animaux ne présentant que la perte de PTEN ont développé de multiples petits polypes, dont beaucoup montraient des anomalies tissulaires précoces. Par contraste frappant, les souris dépourvues à la fois de PTEN et du cluster de microARNs présentaient bien plus de lésions, des polypes plus volumineux et une proportion plus élevée de signes avancés, incluant une dysplasie de haut grade et de véritables adénocarcinomes. Le cluster de microARNs seul n’a pas provoqué de maladie, montrant que sa perte est particulièrement délétère en présence d’une déficience en PTEN.
La voie classique inchangée, des coupables nouveaux en jeu
Le cancer du côlon est souvent entraîné par une activation excessive de la voie Wnt/β-caténine, une route clé régulant les cellules souches intestinales. Parce que ce cluster de microARNs peut influencer cette voie dans le tissu mammaire, les auteurs ont testé si c’était aussi le cas ici. De manière surprenante, les niveaux et la localisation de la β-caténine et de son corécepteur LRP6 dans le côlon n’ont pas changé lorsque le cluster de microARNs a été supprimé, même chez les animaux double knockout. À la place, une analyse à grande échelle de l’expression génique a pointé ailleurs : les tumeurs dépourvues à la fois de PTEN et des microARNs montraient de fortes signatures de remodelage tissulaire, de réponse à la blessure et de transition épithélio-mésenchymateuse, un programme associé à l’invasion et aux métastases. Les voies de signalisation portées par les kinases MAP (ERK1/2 et p38) et par le facteur de croissance TGFβ étaient particulièrement enrichies.
Comment les signaux de croissance se dérèglent
En approfondissant, les chercheurs ont examiné les protéines dans le tissu colique. Ils ont constaté que si la perte de PTEN seule stimulait la voie PI3K/AKT, l’ajout de la perte du cluster de microARNs provoquait une poussée supplémentaire de l’activité MAPK : davantage de JNK, p38, MKK4 activés et surtout d’ERK1/2. Ces signaux très actifs coïncidaient avec des niveaux accrus de cycline D1, un moteur clé de la division cellulaire. Parallèlement, des composants de la voie TGFβ favorisant son activité (SMAD3 et SMAD4) augmentaient, tandis qu’un frein interne (SMAD7) diminuait, et les cellules cancéreuses présentaient une plus forte coloration nucléaire de SMAD2/3, cohérente avec l’activation de la voie. En comparant les gènes des tumeurs murines avec les cibles prédictes des microARNs, l’équipe a identifié IGF1, un puissant facteur de croissance qui alimente les cascades MAPK, comme une cible directe du cluster miR-424(322)~503. Lorsque les microARNs étaient absents, IGF1 échappait à la répression, poussant encore plus l’activation de la signalisation MAPK. Les analyses des jeux de données de cancers colorectaux humains reflétaient ces observations : IGF1 était plus élevé dans les tumeurs avec de faibles niveaux de miR-424 ou miR-503, et le long ARN non codant qui héberge ces microARNs, MIR503HG, ainsi que les microARNs eux-mêmes, étaient coordonnés et altérés dans les tumeurs de patients.
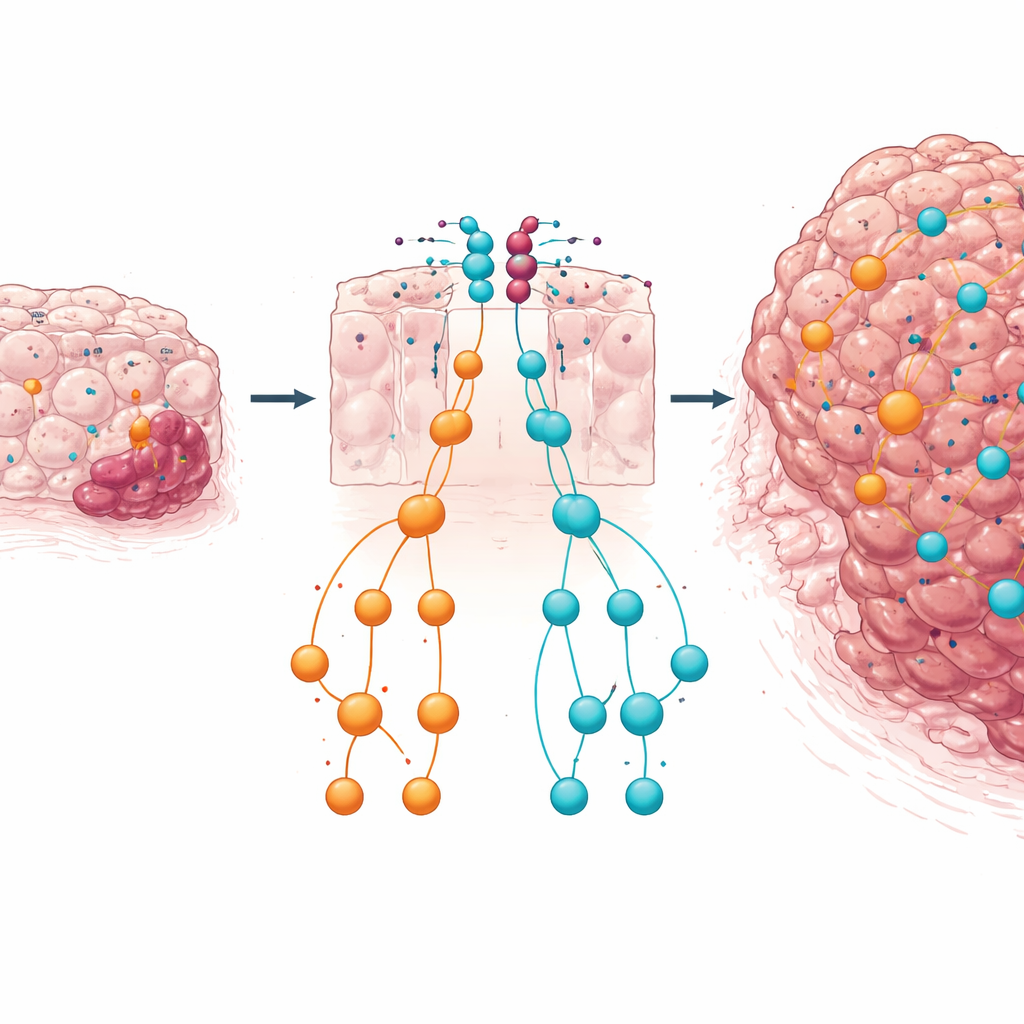
Un double filet de sécurité et ce que cela signifie pour les patients
Dans l’ensemble, les résultats suggèrent que dans le tissu colique déficient en PTEN, le cluster miR-424(322)~503 fonctionne comme un second filet de sécurité. Quand PTEN est perdu, ces microARNs sont upregulés, en partie via des signaux tels que TGFβ, et travaillent à freiner des voies de croissance puissantes comme IGF1–MAPK et TGFβ–SMAD. Si ce frein microARN est supprimé, les signaux de croissance et de remodelage tournent sans contrôle, accélérant la transition de polypes bénins à un cancer invasif. Pour un lecteur non specialisté, le message clé est que toutes les altérations génétiques dans une tumeur ne vont pas dans le même sens : certaines constituent des défenses intégrées. Comprendre comment PTEN et ce cluster de microARNs coopèrent pour maintenir l’équilibre de la croissance cellulaire pourrait aider à identifier les patients à haut risque et inspirer des traitements combinés ciblant à la fois les axes PI3K/AKT et MAPK/TGFβ dans le cancer colorectal.
Citation: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Mots-clés: cancer colorectal, PTEN, microARN, signalisation MAPK, TGF-bêta