Clear Sky Science · fr
ERRα-KDM5C limite l’activité de l’enhancer STING pour moduler la signalisation des interférons de type I dans la progression du cancer du sein
Empêcher les cellules cancéreuses de se cacher
Les cellules cancéreuses ne se contentent pas de croître de manière incontrôlée — elles apprennent aussi à se dissimuler face au système immunitaire de l’organisme. Cette étude révèle comment certaines cellules du cancer du sein abaissent un important système d’alarme interne, appelé voie STING, qui alerte normalement le système immunitaire en cas de danger. En comprenant ce « bouton d’arrêt », les scientifiques espèrent trouver de nouvelles façons de rendre les tumeurs plus visibles pour le système immunitaire et d’améliorer l’efficacité des traitements existants, y compris la chimiothérapie.
Un système d’alarme cellulaire sous pression
La voie STING agit comme un système de sécurité intégré au sein de nos cellules. Lorsqu’une atteinte à l’ADN ou des signaux de type viral sont détectés, STING aide à déclencher les interférons de type I — des messagers immunitaires puissants qui mobilisent des défenses telles que les lymphocytes T cytotoxiques. De nombreuses tumeurs trouvent des moyens d’éteindre cette alarme, ce qui leur facilite la croissance sans contrôle. Les auteurs de ce travail se sont concentrés sur les cellules du cancer du sein et ont cherché à savoir : quelles molécules maintiennent STING au repos, et comment ce contrôle est-il intégré au « tableau de bord » génétique des enhancers — de courtes régions d’ADN qui augmentent l’activité des gènes voisins ?
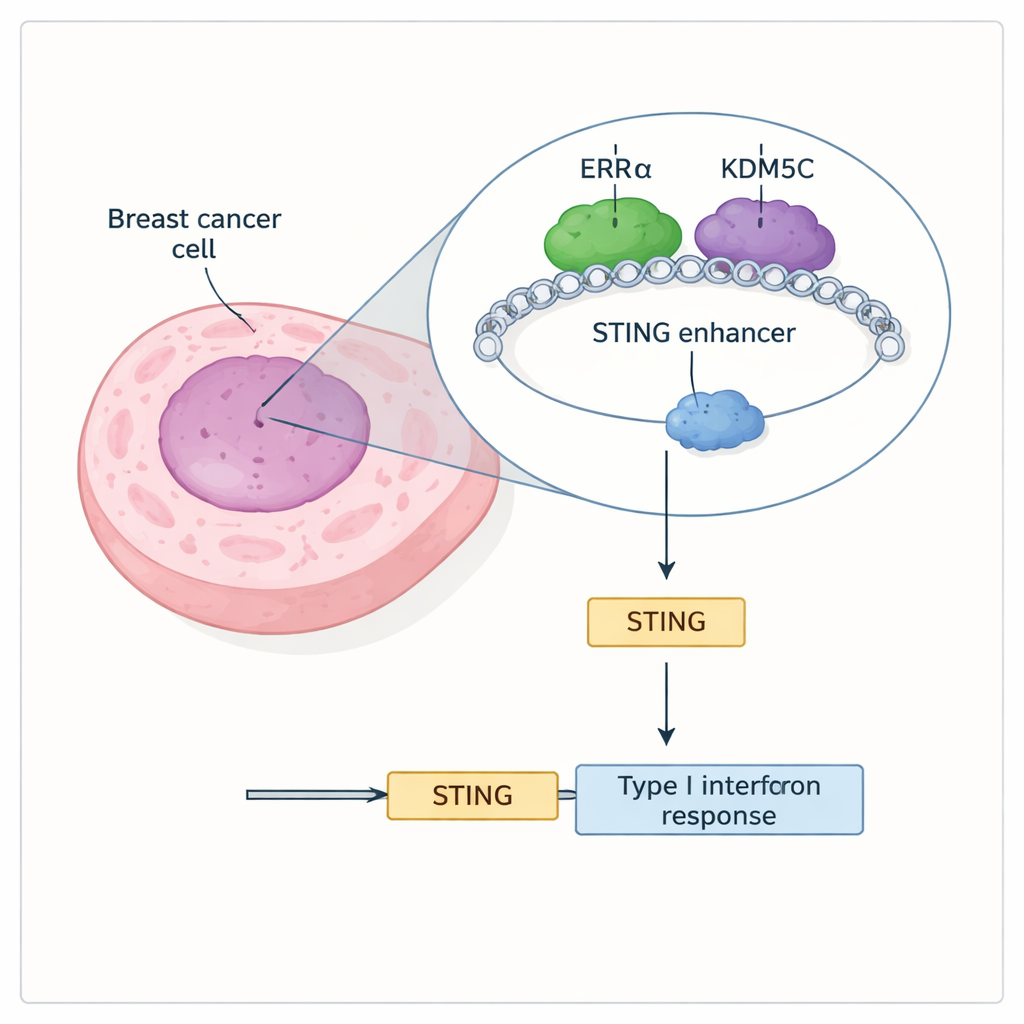
Deux protéines s’associent pour étouffer STING
Les chercheurs ont découvert qu’un récepteur nucléaire nommé ERRα et une enzyme appelée KDM5C interagissent physiquement et se localisent ensemble sur de nombreux enhancers actifs, y compris un enhancer contrôlant le gène STING. ERRα est connu pour aider les cellules cancéreuses à reprogrammer leur métabolisme et à résister à la mort cellulaire, tandis que KDM5C est un « éditeur de chromatine » qui efface une marque chimique (H3K4me3) associée à une forte activation génique. À l’aide de cartes d’occupation du génome, l’équipe a montré qu’ERRα et KDM5C co-occupent souvent des sites d’enhancer portant des marques d’activité élevée et produisant des ARN d’enhancer, signe que ces commutateurs sont activés. À l’enhancer de STING en particulier, les deux protéines sont présentes, et leur présence coïncide avec une production de STING limitée.
Relâcher le frein sur les signaux immunitaires
Lorsque les scientifiques ont réduit les niveaux d’ERRα ou de KDM5C dans des cellules de cancer du sein, l’enhancer de STING est devenu hyperactif. Les marques chimiques associées à une forte activation ont augmenté, celles liées à un état plus faible ont diminué, et la production d’ARN d’enhancer a augmenté. Cela a été suivi par une hausse des niveaux du gène et de la protéine STING et par une activation plus forte de sa voie en aval, y compris TBK1 et IRF3 — des relais clés qui stimulent la production d’interférons de type I. En conséquence, les cellules ont commencé à exprimer des niveaux plus élevés d’interférons et de gènes stimulés par les interférons, centraux pour la défense antivirale et l’immunité antitumorale. Autrement dit, la suppression d’ERRα ou de KDM5C a transformé une alarme étouffée en une sirène bruyante au sein des cellules cancéreuses.
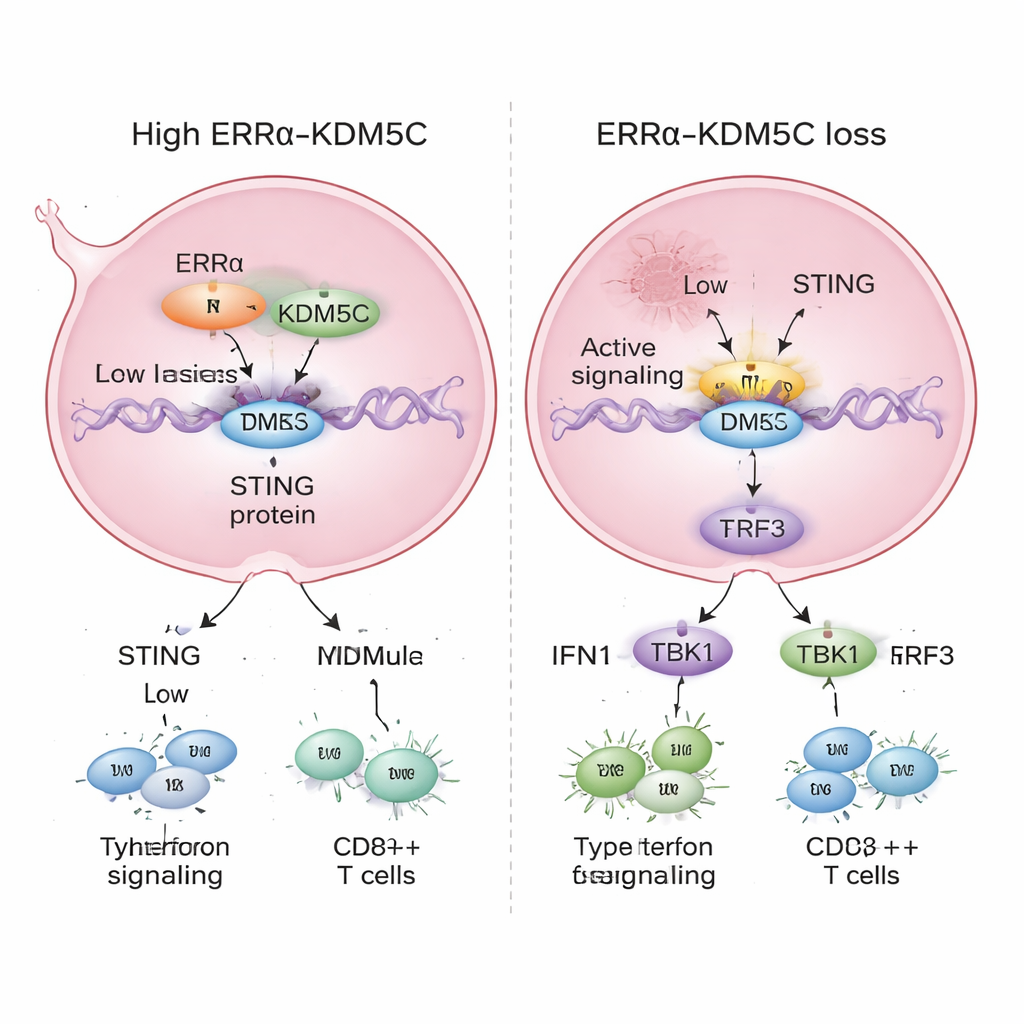
Ralentir la croissance tumorale et renforcer la thérapie
Ces changements moléculaires ont eu des effets visibles sur le comportement des cellules cancéreuses. Les cellules de cancer du sein avec des niveaux réduits d’ERRα ou de KDM5C se sont développées plus lentement et ont formé moins de colonies en culture. Chez la souris, les tumeurs issues de cellules appauvries en ERRα étaient plus petites et plus légères, indiquant une croissance moindre in vivo. Fait important, lorsque STING était également éteint, une grande partie de cette inhibition de croissance était annulée, montrant que l’activation de STING est une composante clé de la façon dont la perte d’ERRα et de KDM5C limite les tumeurs. L’équipe a aussi testé un médicament de chimiothérapie, l’étoposide, qui provoque des dommages à l’ADN connus pour activer STING. Le blocage d’ERRα rendait l’étoposide plus efficace pour réduire les tumeurs, suggérant que desserrer ce frein améliore les traitements standard en amplifiant les signaux stimulant l’immunité.
Ce que cela signifie pour les patientes
En analysant des données de patientes, les chercheurs ont constaté que les niveaux d’ERRα sont plus élevés dans les cancers du sein humains que dans le tissu mammaire normal, et qu’une expression élevée d’ERRα est associée à une survie plus faible et à une moindre présence de lymphocytes T CD8+ antitumoraux dans les tumeurs. Pris ensemble, les résultats dessinent une image claire : ERRα et KDM5C forment un module de contrôle qui maintient l’alarme STING silencieuse, aidant les tumeurs mammaires à croître et à échapper à l’attaque immunitaire. Pour un public non spécialiste, le message clé est que certains cancers du sein utilisent ce duo pour se cacher des défenses de l’organisme. Cibler ERRα, KDM5C ou leur emprise sur l’enhancer de STING pourrait aider à « démasquer » les tumeurs, renforcer la réponse immunitaire et accroître l’efficacité des thérapies existantes.
Citation: Xu, ZH., Chen, J., He, Y. et al. ERRα-KDM5C restrains STING enhancer activity to modulate type I interferon signaling in breast cancer progression. Cell Death Dis 17, 228 (2026). https://doi.org/10.1038/s41419-026-08499-2
Mots-clés: cancer du sein, voie STING, interféron de type I, régulation épigénétique, immunité tumorale