Clear Sky Science · fr
La suppression de l’autophagie pilotée par mTOR définit une vulnérabilité métabolique dans les cancers du sein HR+/HER2− résistants aux inhibiteurs de CDK4/6
Pourquoi cela compte pour les patientes atteintes de cancer du sein
De nombreuses femmes atteintes de cancer du sein avancé vivent aujourd’hui plus longtemps grâce à des médicaments appelés inhibiteurs de CDK4/6, qui ralentissent la vitesse de division des cellules tumorales. Malheureusement, la plupart des tumeurs finissent par échapper à ces traitements. Cette étude pose une question porteuse d’espoir : lorsque le cancer du sein devient résistant aux inhibiteurs de CDK4/6, acquiert-il une nouvelle faiblesse que les cliniciens pourraient exploiter avec des médicaments métaboliques existants et relativement simples, comme la metformine ou le dichloroacétate (DCA) ?
Quand les médicaments du cycle cellulaire cessent de fonctionner
Les médecins traitent souvent le type le plus courant de cancer du sein — maladie hormonodépendante (récepteurs hormonaux positifs), HER2 négatif — par hormonothérapie associée à des inhibiteurs de CDK4/6 comme le palbociclib ou le ribociclib. Ces médicaments ciblent des protéines qui poussent les cellules à traverser le cycle de division. Avec le temps, cependant, certaines cellules cancéreuses s’adaptent et deviennent fortement résistantes, continuant de croître même en présence de fortes doses. Les chercheurs ont recréé ce problème en laboratoire en exposant des lignées de cellules de cancer du sein (T47D et MCF7) à des quantités progressivement croissantes d’inhibiteurs de CDK4/6. Ils ont obtenu deux types de survivantes : des cellules partiellement résistantes et un sous-groupe plus réduit de clones fortement résistants qui ne répondaient plus bien au traitement.
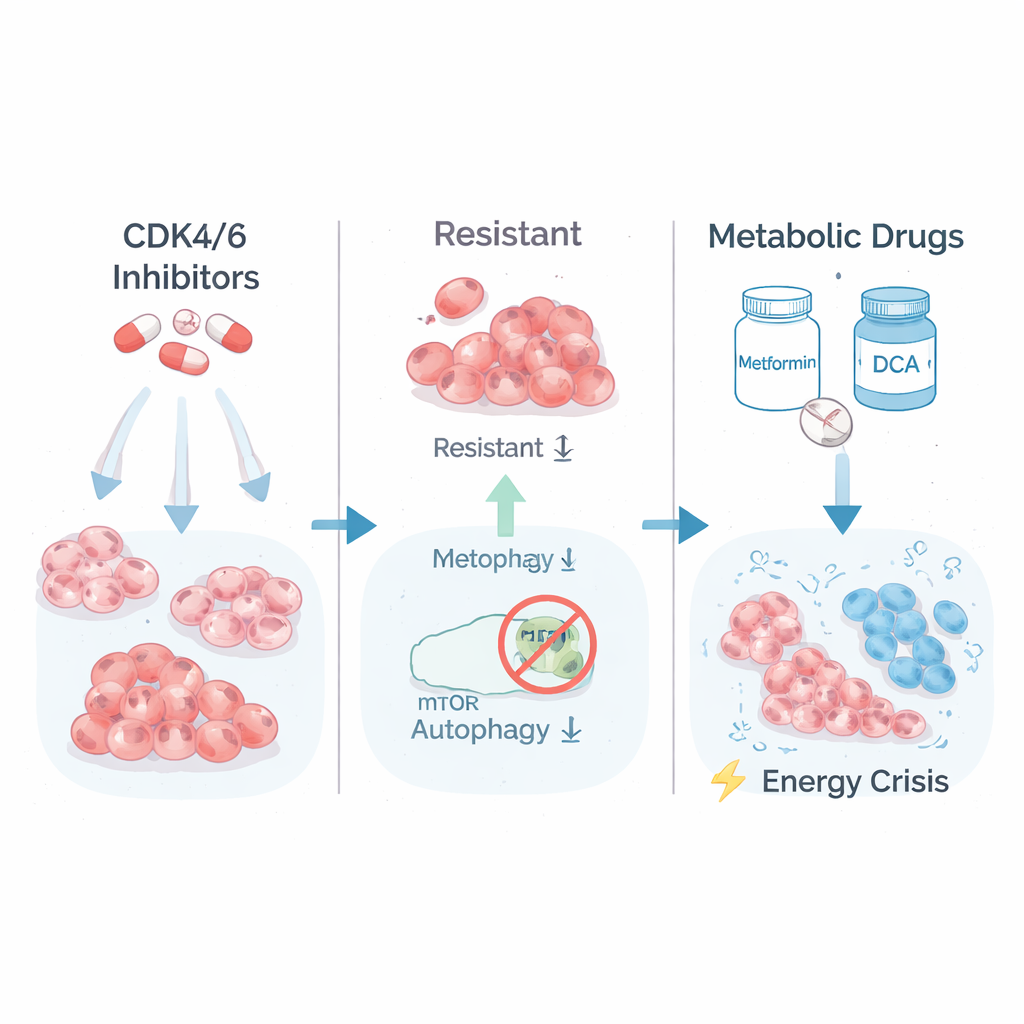
Une faiblesse cachée dans l’utilisation de l’énergie par la tumeur
Pour comprendre ce qui rendait les cellules fortement résistantes différentes, l’équipe a examiné quels gènes étaient activés ou réprimés. Ils ont constaté que les cellules les plus résistantes avaient fortement augmenté des voies impliquées dans la combustion du sucre (glycolyse) et dans la signalisation de croissance contrôlée par un complexe protéique appelé mTORC1. Autrement dit, ces cellules vivaient « à plein régime », consumant rapidement du carburant pour continuer de croître. Les scientifiques ont ensuite testé si ce métabolisme « en première » pouvait être retourné contre les cellules. Ils ont traité les cellules résistantes et parentales par la metformine, un médicament antidiabétique courant qui met à l’épreuve les « centrales énergétiques » cellulaires, et par le DCA, qui force les cellules à métaboliser le carburant plus efficacement. De façon frappante, les clones les plus résistants sont devenus les plus vulnérables : leur croissance à long terme en culture s’est effondrée sous traitement métabolique, alors que les cellules parentales et seulement partiellement résistantes étaient beaucoup moins affectées.
Autonettoyage bloqué et effondrement énergétique
Pourquoi ces cellules échappées du traitement seraient-elles si sensibles au stress énergétique ? La réponse réside dans un autre processus de survie fondamental : l’autophagie, le système cellulaire de « recyclage et nettoyage ». Normalement, lorsque l’énergie vient à manquer, les cellules dégradent et réutilisent leurs propres composants pour survivre. Les chercheurs ont montré que, chez les clones fortement résistants, mTORC1 était hyperactif et imposait un frein chimique sur ULK1, un acteur clé du démarrage de l’autophagie. À l’aide d’un test rapporteur sensible, ils ont démontré que ces cellules ne pouvaient plus activer ou augmenter correctement l’autophagie, même lorsqu’elles étaient exposées à des médicaments métaboliques. En conséquence, la metformine et le DCA ont provoqué une sévère crise énergétique : des senseurs du faible niveau d’énergie se sont activés, la synthèse des lipides a été coupée et des marqueurs de mort cellulaire irréversible sont apparus, spécifiquement dans les cellules fortement résistantes.
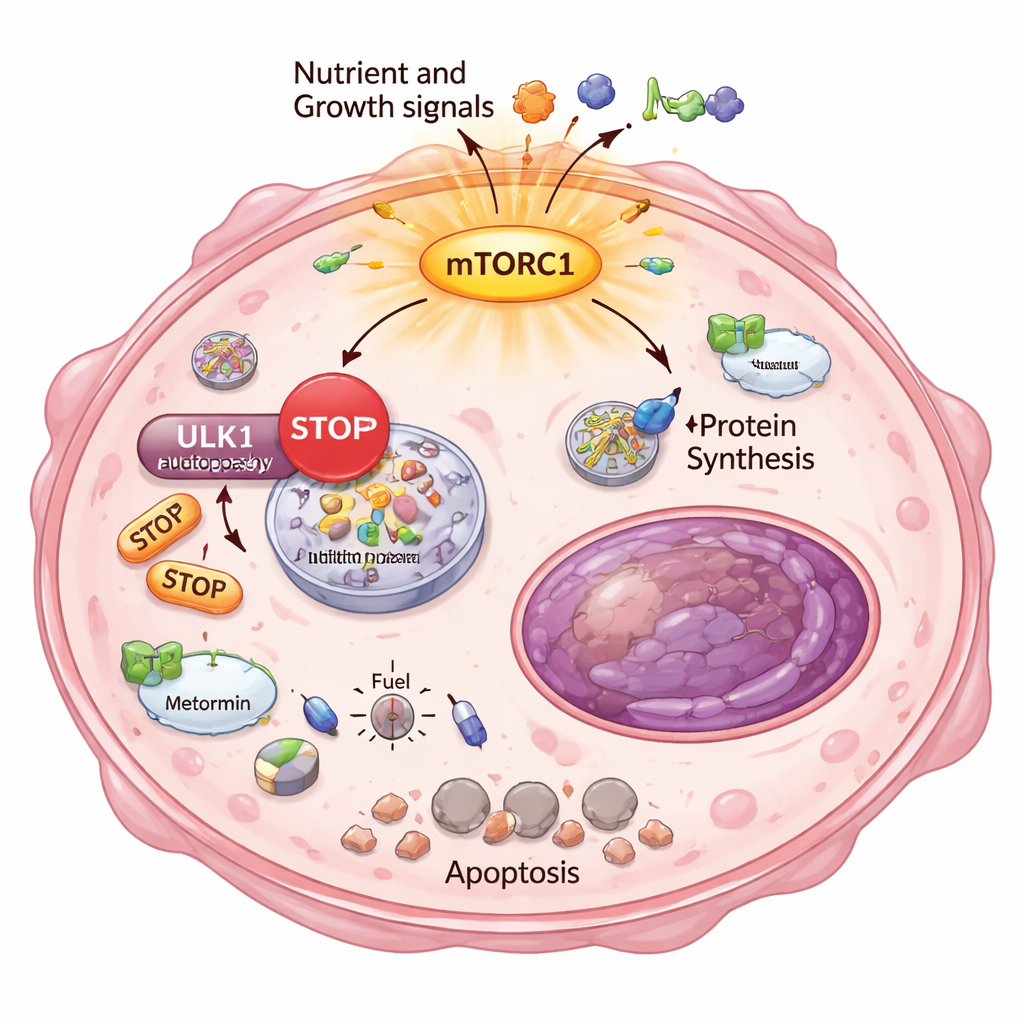
Preuves à partir de tumeurs humaines
Les modèles de laboratoire ne reflètent pas toujours ce qui se passe chez les patients, l’équipe s’est donc tournée vers des échantillons tumoraux humains. Ils ont coloré plus d’une centaine de cancers pour un marqueur d’activité de mTORC1 (4E-BP1 phosphorylé) et pour p62, une protéine qui s’accumule lorsque l’autophagie est bloquée. Les tumeurs avec une activité élevée de mTORC1 avaient tendance à présenter davantage de p62, ce qui soutient l’idée qu’un profil « signal de croissance suractivé plus recyclage déficient » existe dans de vrais cancers du sein, et pas seulement dans des lignées cellulaires. Cela suggère qu’un sous-ensemble de patientes pourrait porter des tumeurs présentant la même faiblesse métabolique observée en laboratoire.
Ce que cela pourrait signifier pour les traitements futurs
Pour un non-spécialiste, le message clé est que lorsque des cancers du sein évoluent pour échapper à des inhibiteurs de CDK4/6 puissants, ils peuvent aussi se retrouver piégés sur le plan métabolique. En activant en permanence les signaux de croissance et en désactivant le recyclage cellulaire, ces tumeurs deviennent fortement dépendantes d’un approvisionnement énergétique constant. L’étude montre que cette configuration peut être exploitée avec des médicaments métaboliques comme la metformine et le DCA, déjà bien connus dans d’autres pathologies. Les auteurs proposent en outre que de simples tests tissulaires pour l’activité de mTORC1 et les marqueurs d’autophagie pourraient aider à identifier les patientes dont les tumeurs résistantes sont prêtes pour ce type d’attaque métabolique, ouvrant la voie à des traitements de sauvetage plus personnalisés après l’échec des inhibiteurs de CDK4/6.
Citation: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Mots-clés: cancer du sein, résistance aux inhibiteurs de CDK4/6, mTOR, autophagie, thérapie métabolique