Clear Sky Science · fr
Le basculement d’épissage de l’isoforme oncogénique BCS1L supprime la progression du cancer de l’ovaire en perturbant la fonction mitochondriale
Des centrales énergétiques à l’intérieur des cellules cancéreuses
Toutes les cellules de notre organisme dépendent de petites centrales appelées mitochondries. Les cellules cancéreuses, qui prolifèrent et se disséminent rapidement, ont un appétit énergétique particulièrement élevé. Cette étude révèle comment le cancer de l’ovaire réorganise l’un de ses principaux assistants mitochondriaux, et montre que basculer en douceur un « interrupteur » moléculaire sur cet assistant peut affamer les tumeurs tout en épargnant largement les tissus sains.
Pourquoi les tumeurs s’appuient sur leurs moteurs
Les cellules du cancer de l’ovaire, comme de nombreux cancers, peuvent puiser de manière flexible différentes sources d’énergie. En passant au crible de grandes bases de données de patients et des profils unicellulaires, les chercheurs ont constaté que de nombreuses tumeurs ovariennes font fonctionner leurs mitochondries en mode suralimenté connu sous le nom de phosphorylation oxydative, ou OXPHOS. Les tumeurs présentant cette activité mitochondriale accrue étaient plus agressives et plus fréquentes dans les stades avancés. Parmi les nombreuses protéines qui composent la machinerie énergétique mitochondriale, une a retenu l’attention : BCS1L, une chaperonne qui aide à assembler le Complexe III, un hub central dans la chaîne énergétique cellulaire. Les tumeurs à forte OXPHOS et certains sous‑types cellulaires tumoraux montraient une activité BCS1L particulièrement élevée, suggérant que les cellules cancéreuses comptaient fortement sur cet assistant pour maintenir leurs moteurs en marche.
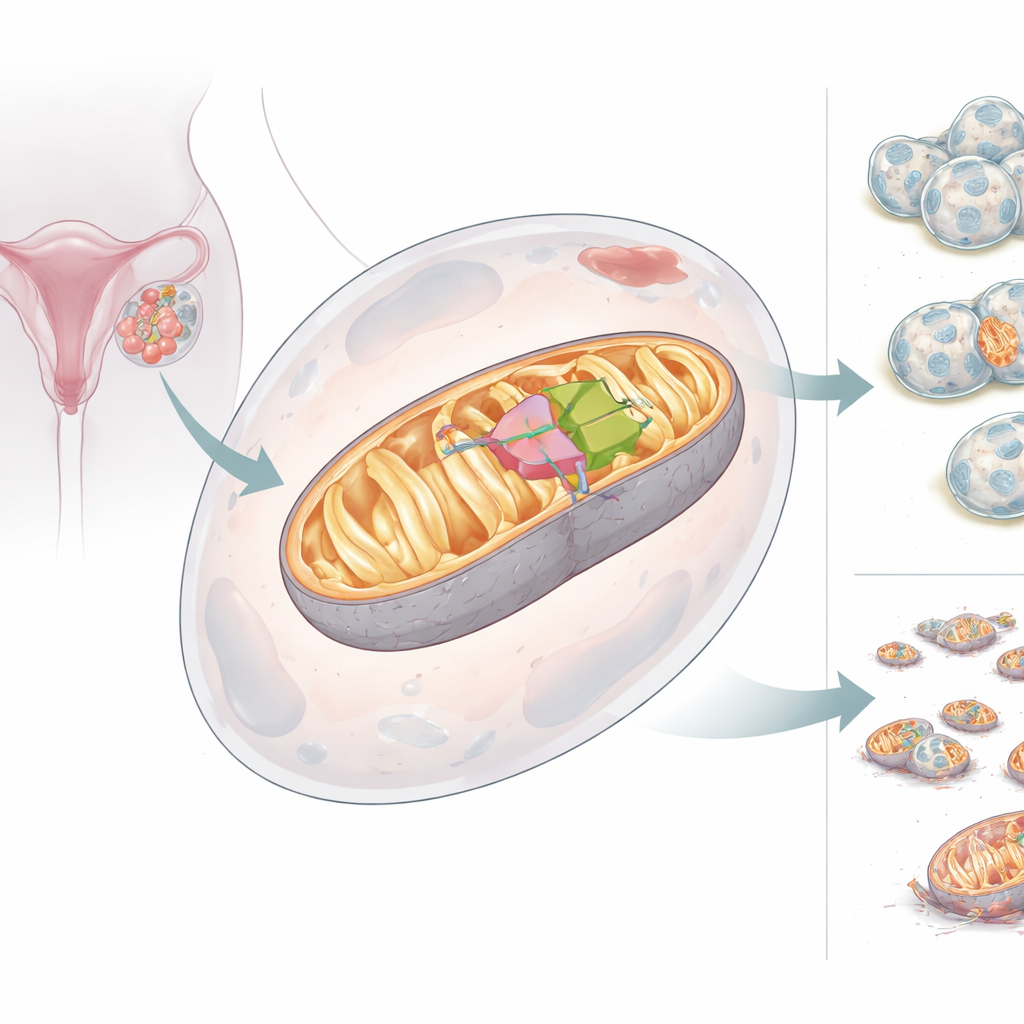
Deux visages d’un assistant mitochondrial
L’équipe a découvert que le gène BCS1L peut produire deux versions, ou isoformes, de sa protéine. La forme pleine longueur, BCS1L‑L, porte une étiquette d’adressage qui l’envoie dans les mitochondries, où elle soutient l’assemblage correct du Complexe III et une forte production d’énergie. La forme plus courte, BCS1L‑S, est dépourvue d’un segment clé et ne peut pas atteindre les mitochondries ; elle reste plutôt dans le cytosol et le noyau et ne soutient pas la production d’énergie. Dans les tissus sains, la version courte est courante, mais dans les cancers de l’ovaire l’équilibre bascule : la version longue, liée aux mitochondries, domine. Lorsque les cellules étaient forcées de produire davantage de BCS1L‑L, leurs mitochondries généraient plus d’énergie, maintenaient un potentiel de membrane plus élevé, produisaient moins de sous‑produits oxygénés nocifs et résistaient à la mort cellulaire. Lorsque BCS1L diminuait, les mitochondries se fragmentaient, la production d’énergie chutait, les molécules d’oxygène dommageables augmentaient et les cellules cancéreuses étaient plus susceptibles de mourir.
Comment le cancer réécrit le message
La production de la version longue ou courte de BCS1L dépend de la manière dont la cellule édite son message ARN, un processus appelé épissage. Les chercheurs ont cherché des protéines qui se lient à l’ARN de BCS1L et influencent ce choix. Ils ont ciblé USP39, un facteur d’épissage déjà associé à plusieurs cancers. Dans les cellules du cancer ovarien, USP39 se lie à proximité du segment d’ARN qui devient l’exon 2 de BCS1L et favorise son inclusion, privilégiant ainsi la version longue ciblée vers les mitochondries. Lorsque USP39 était silencieux, les cellules sautaient plus souvent ce segment, basculant vers la forme courte BCS1L‑S. Ce basculement affaiblissait le Complexe III, réduisait la respiration mitochondriale et la production d’ATP, augmentait le stress oxydatif et déclenchait la mort des cellules tumorales. Restaurer BCS1L‑L dans ces cellules sauvait une grande partie de leur fonction mitochondriale et de leur survie, montrant que USP39 commande un interrupteur mitochondrial critique essentiellement via BCS1L.
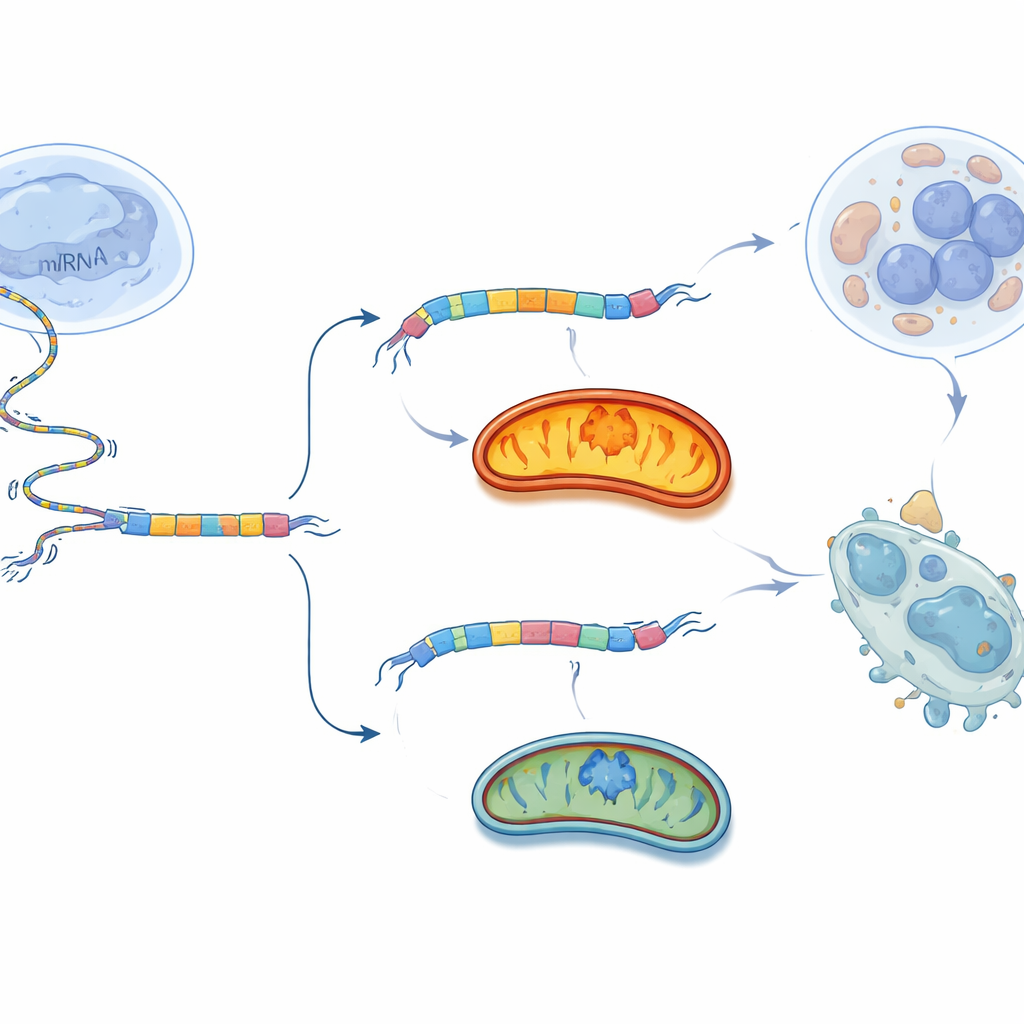
Activer l’interrupteur contre la tumeur
Plutôt que de bloquer les mitochondries de façon générale, ce qui pourrait nuire à de nombreux tissus, l’équipe a testé une tactique plus chirurgicale : influer sur le choix d’épissage de BCS1L lui‑même. Ils ont conçu de courtes séquences d’acide nucléique appelées oligonucléotides antisens (ASO) qui se lient juste autour de l’exon 2 de l’ARN de BCS1L. Ces ASO agissent comme de minuscules pinces, modifiant la lecture du message par la machinerie d’épissage et encourageant la cellule à sauter l’exon 2. Dans des cellules de cancer ovarien cultivées en laboratoire, le meilleur ASO a fortement réduit la forme longue BCS1L‑L et augmenté la forme courte BCS1L‑S. En conséquence, la respiration mitochondriale et la production d’ATP ont chuté, les niveaux d’espèces oxygénées nocives ont augmenté et beaucoup plus de cellules ont subi une mort programmée. Lorsque le même ASO a été injecté dans des tumeurs ovariennes chez la souris, la croissance tumorale a ralenti et les tumeurs pesaient moins, avec un effet bien plus marqué sur les cellules cancéreuses que sur les fibroblastes normaux.
Que cela pourrait signifier pour les patients
En termes simples, ce travail montre que de nombreux cancers de l’ovaire dépendent d’une version « turbo » d’une protéine d’aide mitochondriale pour alimenter leur croissance. Un facteur d’épissage, USP39, incline la machinerie d’édition de l’ARN de la cellule pour produire davantage cette version turbo, maintenant ainsi les centrales de la tumeur en pleine forme. En utilisant des ASO conçus de manière précise pour faire basculer le choix d’épissage vers la version plus faible, les chercheurs peuvent crippler sélectivement les mitochondries des cellules cancéreuses, déclenchant leur mort tout en laissant la plupart des cellules normales relativement épargnées. Bien que l’administration de ce type de médicament ASO aux tumeurs reste un défi majeur, cette étude identifie le commutateur d’épissage de BCS1L comme une cible nouvelle, prometteuse et très spécifique pour traiter le cancer de l’ovaire.
Citation: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Mots-clés: cancer de l’ovaire, mitochondries, épissage de l’ARN, BCS1L, oligonucléotides antisens