Clear Sky Science · fr
PGC-1α protège contre la MASH via l’inhibition dépendante de Tim23 de la ferroptose médiée par DRP1
Pourquoi cela compte pour la santé de tous les jours
Beaucoup de personnes atteintes d’obésité ou de diabète de type 2 développent silencieusement un problème hépatique sérieux appelé stéatohépatite associée à un dysfonctionnement métabolique (MASH). Dans cette affection, les cellules du foie engorgées de graisses s’enflamment et commencent à mourir, ouvrant la voie à la formation de cicatrices, à la cirrhose et au cancer du foie. Cette étude met au jour un système de protection interne des cellules hépatiques — centré sur de petites centrales énergétiques appelées mitochondries — qui peut soit protéger le foie des dommages, soit, lorsqu’il fait défaut, accélérer la maladie. Comprendre cet interrupteur de sécurité interne pourrait ouvrir des pistes pour de nouveaux traitements contre l’une des menaces hépatiques les plus courantes dans le monde.
Un examen approfondi d’une maladie hépatique silencieuse
La MASH se développe lorsqu’un simple foie gras bascule vers un état plus dangereux marqué par des cellules hépatiques enflées et lésées, de l’inflammation et, finalement, du tissu cicatriciel. Les auteurs ont examiné des échantillons hépatiques de patients atteints de MASH et de modèles murins nourris avec des régimes riches en graisses et en sucre ou déficients en nutriments imitant la condition humaine. Ils se sont concentrés sur un type particulier de mort cellulaire appelé ferroptose, dans lequel le fer et les lipides endommagés se combinent pour générer des molécules toxiques qui perforent les membranes cellulaires. Tant chez les patients que chez les souris atteints de MASH, les cellules hépatiques présentaient des signes caractéristiques de cette mort liée au fer et aux lipides : dépôts excessifs de fer, mitochondries déformées et niveaux élevés de protéines favorisant les dommages lipidiques, accompagnés de faibles niveaux de protéines qui detoxifient normalement les sous-produits nocifs.
Des preuves que bloquer la mort cellulaire induite par le fer aide
Pour tester si la ferroptose est un simple témoin ou un moteur de la maladie, les chercheurs ont traité des souris soumises à un régime riche en graisses avec la ferrostatine-1, un composé qui bloque spécifiquement la ferroptose. Les souris recevant ce bloqueur présentaient moins d’accumulation de graisses, moins de surcharge en fer et moins de signes d’inflammation et de cicatrisation du foie. Les analyses sanguines montraient une amélioration de la fonction hépatique et de la santé métabolique, y compris un taux de cholestérol plus bas et une meilleure sensibilité à l’insuline. Dans des cellules hépatiques de souris isolées exposées à l’acide palmitique — un lipide qui reproduit la surcharge observée dans la MASH — le même médicament a réduit l’accumulation de graisses, la charge en fer, les dommages oxydatifs et les signaux inflammatoires. Ensemble, ces résultats soutiennent que la ferroptose est un moteur clé des lésions dans la MASH et que l’interrompre peut atténuer de façon significative la maladie.
Le gardien intégré du foie dans les mitochondries
L’équipe s’est ensuite intéressée à PGC-1α, un régulateur maître qui aide les mitochondries à produire de l’énergie et à faire face au stress. Dans les foies humains atteints de MASH, ainsi que chez des souris malades et des cellules hépatiques stressées, les niveaux de PGC-1α étaient sensiblement plus bas, tandis qu’une protéine de scission mitochondriale appelée DRP1 et une enzyme activatrice de lipides nommée ACSL4 étaient plus élevées. En utilisant des souris génétiquement modifiées dépourvues de PGC-1α uniquement dans les cellules du foie, les auteurs ont montré que la perte de ce gardien rendait les régimes riches en graisses beaucoup plus délétères : les foies étaient plus gras, plus enflammés, plus chargés en fer et présentaient des signaux de ferroptose renforcés. Au niveau cellulaire, l’absence de PGC-1α augmentait l’activité de DRP1, l’expression d’ACSL4 et des protéines d’importation du fer, et affaiblissait les défenses antioxydantes qui limitent normalement la ferroptose.
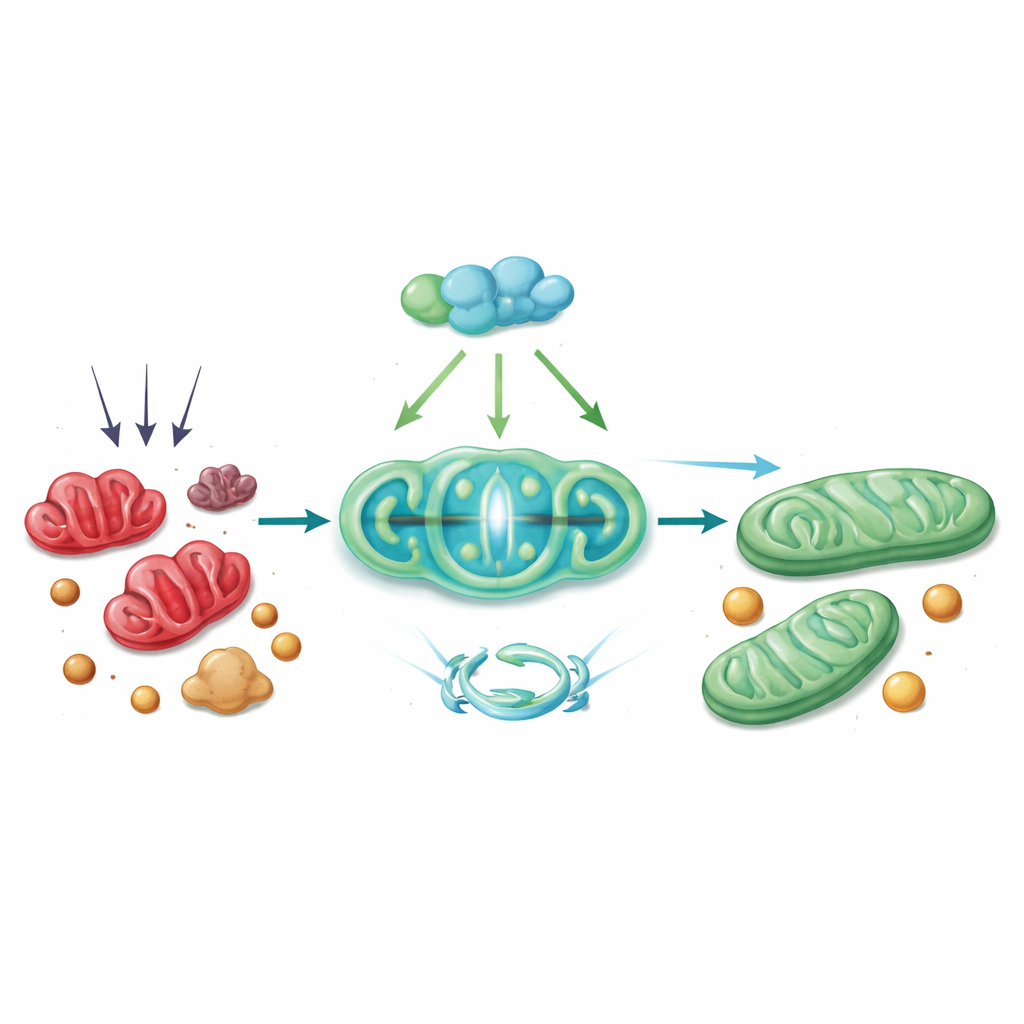
Une réaction en chaîne protectrice à l’intérieur de la cellule
Mécaniquement, PGC-1α agit via une chaîne de partenaires. Il coopère avec un facteur de transcription appelé Nrf1 pour augmenter la production de Tim23, un canal situé dans la membrane mitochondriale interne essentiel à l’importation des protéines et au maintien d’une structure saine. Lorsque les niveaux de Tim23 diminuent, le potentiel de membrane mitochondriale faiblit, ce qui déclenche DRP1 à fragmenter l’organite. L’étude montre qu’avec une baisse de Tim23, DRP1 est plus actif et plus susceptible de s’associer à ACSL4 à la surface mitochondriale, attirant cette enzyme de modification des lipides vers les mitochondries. Là, ACSL4 favorise les altérations lipidiques qui rendent les cellules vulnérables à la ferroptose. Restaurer PGC-1α — soit chez la souris par un vecteur viral de transfert de gène, soit dans des hépatocytes en culture avec un activateur basé sur CRISPR — a inversé plusieurs de ces étapes : Tim23 augmentait, l’activité de DRP1 et d’ACSL4 diminuait, les mitochondries semblaient plus saines et les marqueurs de ferroptose et de lésion hépatique déclinaient.
Comment cette découverte pourrait orienter des thérapies futures
Pour un non-spécialiste, la principale conclusion est que le foie possède un frein interne contre la mort cellulaire conduite par le fer et les lipides, et que ce frein est intégré aux mitochondries. La chaîne PGC-1α–Tim23–DRP1–ACSL4 fonctionne comme un circuit de sécurité : lorsque PGC-1α est robuste, Tim23 stabilise les mitochondries, DRP1 et ACSL4 sont contenus, et les cellules du foie sont moins susceptibles de s’autodétruire. Lorsque ce circuit faillit, la ferroptose s’accélère et la MASH s’aggrave. En identifiant cette voie dans des tissus humains et des modèles animaux, l’étude met en évidence deux stratégies complémentaires pour de futurs traitements — bloquer directement la ferroptose, et renforcer l’activité de PGC-1α ou de Tim23 pour stabiliser les mitochondries — offrant l’espoir d’interventions plus précoces et plus efficaces avant l’installation irréversible des cicatrices hépatiques.
Citation: Zhao, Y., Zhang, L., Li, B. et al. PGC-1α protects against MASH via Tim23-dependent inhibition of DRP1-mediated ferroptosis. Cell Death Dis 17, 246 (2026). https://doi.org/10.1038/s41419-026-08493-8
Mots-clés: maladie du foie gras, mitochondries, mort cellulaire, métabolisme du fer, inflammation hépatique