Clear Sky Science · fr
NSD2 inhibe l’expression de PD-L1 via la phosphorylation oxydative pour contrôler la surveillance immunitaire dans le carcinome hépatocellulaire
Pourquoi cette histoire sur le cancer du foie est importante
Le carcinome hépatocellulaire, la forme la plus fréquente de cancer du foie, est souvent diagnostiqué tard et résiste à de nombreux traitements. Les médicaments d’immunothérapie qui bloquent le « voile d’invisibilité » PD-L1 à la surface des cellules tumorales aident certains patients, mais pas la majorité. Cette étude met au jour un acteur inattendu, une protéine appelée NSD2, qui relie la façon dont les cellules cancéreuses hépatiques produisent de l’énergie à leur visibilité pour le système immunitaire. Comprendre ce lien pourrait indiquer de nouvelles voies pour renforcer les thérapies actuelles et identifier quels patients sont susceptibles d’en bénéficier.
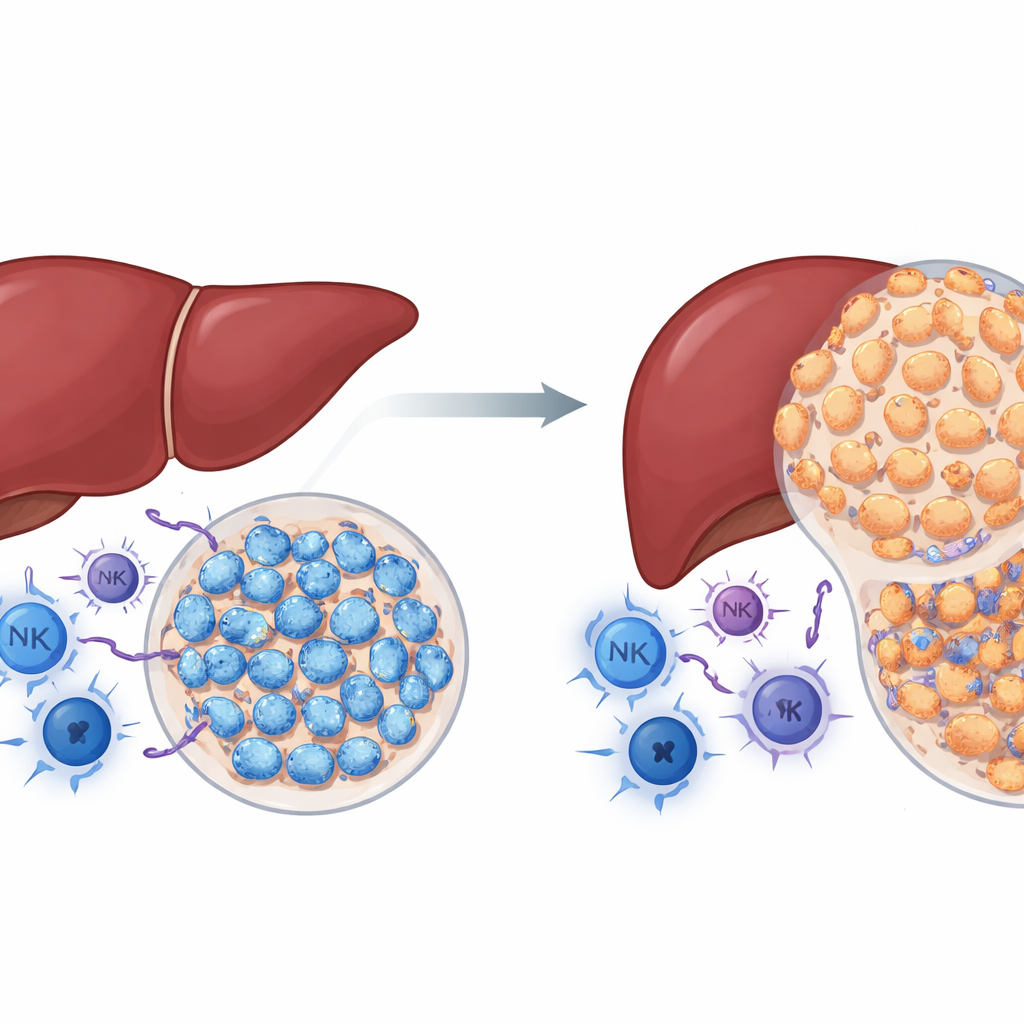
Un rôle surprenant pour une protéine cancéreuse connue
NSD2 est une enzyme qui modifie les histones, les protéines autour desquelles l’ADN est enroulé. Dans de nombreux cancers, NSD2 est considérée comme un moteur de la croissance tumorale. Les auteurs ont cherché à savoir si cela valait aussi pour le cancer du foie. À l’aide de souris génétiquement modifiées exprimant NSD2 spécifiquement dans les cellules hépatiques, ils ont traité les animaux avec un produit chimique qui induit de façon fiable des tumeurs hépatiques. Contrairement aux attentes, les souris surexprimant NSD2 ont développé bien moins de tumeurs et de plus petite taille que les souris normales, et leurs foies présentaient moins de lésions, de cicatrisation et de prolifération cellulaire. Parallèlement, les tumeurs des foies surexprimant NSD2 contenaient davantage de cellules immunitaires anti-cancer, y compris des lymphocytes T auxiliaires et cytotoxiques ainsi que des cellules NK. Ces résultats suggèrent que, en présence d’un système immunitaire intact, NSD2 agit moins comme un accélérateur et davantage comme un frein au cancer du foie.
Les usines d’énergie et l’utilisation du carburant dans les cellules tumorales
Pour comprendre comment NSD2 freine les tumeurs, l’équipe a profilé l’activité génique dans le tissu hépatique. Ils ont constaté que la surexpression de NSD2 réprimait fortement les gènes impliqués dans la phosphorylation oxydative, le processus par lequel les mitochondries — les « centrales électriques » de la cellule — génèrent de l’énergie en utilisant l’oxygène. Des expériences complémentaires sur des lignées de cellules de cancer du foie de souris et humaines ont montré qu’une augmentation de NSD2 diminuait l’expression de nombreux gènes de la phosphorylation oxydative, réduisait la consommation d’oxygène et la production d’ATP, et faisait chuter le potentiel de membrane mitochondrial, signe d’une activité mitochondriale affaiblie. En même temps, ces cellules consommaient moins de glucose mais ne basculaient pas vers une dépendance accrue à la glycolyse, indiquant une réduction nette de la production d’énergie. La perte de NSD2 avait l’effet inverse, renforçant la puissance mitochondriale et l’utilisation du carburant.
Comment NSD2 reconfigure l’énergie et la visibilité immunitaire
Approfondissant l’analyse, les chercheurs ont combiné une cartographie chromatinienne à l’échelle du génome avec des données d’expression génique et ont identifié un ensemble de gènes directement activés en présence de NSD2. Deux d’entre eux, Camk2d et Prkce, sont connus pour freiner l’activité mitochondriale. NSD2 augmentait une marque histone particulière (H3K36me2) à leurs promoteurs, stimulant leur expression. La réintroduction de ces gènes dans des cellules de cancer du foie déficientes en NSD2 réduisait la consommation d’oxygène mitochondriale et la production d’ATP, confirmant qu’ils agissent comme des freins en aval de NSD2 sur la phosphorylation oxydative. Fait important, des travaux antérieurs suggéraient que des mitochondries très actives favorisent une forte expression de PD-L1 sur les cellules tumorales. Conformément à cela, les auteurs ont observé que la surexpression de NSD2 réduisait les niveaux de PD-L1, tandis que la perte de NSD2 augmentait PD-L1 sur les cellules de cancer du foie et dans les tissus tumoraux.
Abaisser le bouclier et réveiller l’attaque immunitaire
L’impact fonctionnel de ces modifications moléculaires a été testé chez des souris recevant des injections hépatiques de cellules cancéreuses modifiées pour surexprimer ou perdre NSD2. Les cellules dépourvues de NSD2 formaient rapidement des tumeurs plus grosses, exprimaient davantage PD-L1 et étaient infiltrées par moins de lymphocytes T et de cellules NK, en particulier de lymphocytes T cytotoxiques activés. Lorsque les chercheurs bloquaient chimiquement le complexe V mitochondrial, un composant clé de la phosphorylation oxydative, les niveaux de PD-L1 dans les cellules déficientes en NSD2 retombaient vers la normale et les cellules immunitaires étaient mieux à même d’induire la mort des cellules tumorales. De même, la surexpression de Camk2d ou Prkce dans des cellules dépourvues de NSD2, ou le traitement des tumeurs par un anticorps bloquant PD-L1, réduisait la taille des tumeurs et rétablissait l’infiltration des cellules immunitaires. Dans des jeux de données de patients, une faible expression de NSD2 était associée à une survie plus faible mais, de façon intrigante, à une meilleure réponse aux thérapies ciblant PD-L1, suggérant que le statut de NSD2 pourrait aider à prédire qui bénéficie de ces médicaments.
Ce que cela signifie pour les soins futurs du cancer du foie
Pour le lecteur général, le message clé est que cette étude redéfinit NSD2 comme un facteur suppressif de tumeur dans le cancer du foie, du moins en présence d’un système immunitaire fonctionnel. En réduisant la production d’énergie cellulaire basée sur l’oxygène, NSD2 abaisse indirectement PD-L1 sur les cellules tumorales, retirant une partie de leur voile d’invisibilité et permettant aux cellules immunitaires de les reconnaître et de les attaquer. Cette chaîne NSD2–énergie–PD-L1 nouvellement décrite suggère deux idées pratiques : d’une part, les patients dont les tumeurs manquent de NSD2 pourraient être des candidats particulièrement adaptés aux médicaments bloquant PD-L1 ; d’autre part, associer des médicaments qui inhibent la production d’énergie mitochondriale à l’immunothérapie pourrait offrir un coup de grâce puissant contre le cancer du foie.
Citation: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Mots-clés: carcinome hépatocellulaire, NSD2, phosphorylation oxydative, PD-L1, immunothérapie tumorale