Clear Sky Science · fr
La régulation de l’épissage de DDX39B par SNRPD2 favorise la progression du cancer de l’endomètre en supprimant l’activation d’exons cryptiques de CTSC
Pourquoi les messages cachés dans les gènes du cancer comptent
Le cancer de l’endomètre, une tumeur fréquente de l’utérus, augmente dans le monde entier, et de nombreux patients atteints de formes avancées disposent encore de peu d’options efficaces. Cette étude révèle comment un processus discret à l’intérieur des cellules — la manière dont elles découpent et recollent les messages génétiques — peut pousser les tumeurs de l’endomètre à croître et à se propager. En mettant au jour un « schéma de câblage » fragile dont dépendent les cellules cancéreuses, ce travail ouvre la voie à de nouvelles stratégies pour arrêter les tumeurs à l’aide de médicaments génétiques de précision.
Un cancer croissant qui réclame de nouvelles réponses
Le cancer de l’endomètre est désormais le cancer gynécologique le plus fréquent dans de nombreux pays occidentaux, avec une augmentation constante des cas et des décès en Occident comme en Chine. La chirurgie, la radiothérapie, la chimiothérapie, les traitements hormonaux et l’immunothérapie sont tous utilisés, mais restent loin d’être parfaits. L’ablation de l’utérus met fin à la fertilité, les traitements hormonaux échouent souvent, et les tumeurs agressives récidivent fréquemment. Ces défis ont poussé les chercheurs à sonder plus profondément les cellules cancéreuses pour y identifier des vulnérabilités moléculaires susceptibles d’être ciblées par des thérapies plus précises.
La machinerie d’épissage de la cellule comme point faible
Pour fonctionner, nos gènes sont d’abord copiés en longues molécules d’ARN qui doivent être taillées et recousues dans un processus appelé épissage. Des machines protéiques spécialisées, appelées spliceosomes, décident quelles portions sont conservées et lesquelles sont éliminées, éditant ainsi effectivement le script utilisé par la cellule pour fabriquer des protéines. L’équipe s’est concentrée sur un composant du spliceosome nommé SNRPD2, membre d’une famille de protéines « Sm » qui aident à assembler la machinerie d’épissage. En exploitant de larges bases de données génomiques et protéomiques sur le cancer et en analysant des échantillons de patients, ils ont constaté que les niveaux de SNRPD2 sont nettement plus élevés dans les tumeurs de l’endomètre que dans la muqueuse utérine normale, et que les patients dont les tumeurs expriment davantage SNRPD2 ont tendance à avoir un mauvais pronostic.
Éteindre un éditeur maître ralentit les tumeurs
Pour tester si SNRPD2 est un simple observateur ou un acteur causal, les chercheurs l’ont diminué dans des lignées cellulaires de cancer de l’endomètre cultivées en laboratoire. Lorsque SNRPD2 a été silencieux, les cellules se divisaient plus lentement, formaient moins de colonies et avaient une capacité réduite de migration et d’invasion à travers des membranes — comportements liés aux métastases. Lorsque ces cellules altérées ont été implantées chez la souris, les tumeurs résultantes étaient beaucoup plus petites et montraient moins de cellules en division active. De manière importante, l’équipe a conçu des oligonucléotides antisens — de courts fragments d’ADN synthétique de type médicament — ciblant spécifiquement l’ARN de SNRPD2. Dans un modèle de xénogreffe dérivée de patients, où des fragments tumoraux humains croissent dans des souris immunodéficientes, ces médicaments antisens ont fortement réduit les niveaux de SNRPD2 et la taille des tumeurs, suggérant que SNRPD2 est une cible pharmacologique potentiellement exploitable cliniquement.
Une chaîne en trois étapes de l’erreur d’épissage à la croissance tumorale
En approfondissant les données génétiques, les chercheurs ont cherché à savoir comment la perte de SNRPD2 reconfigure les messages ARN à l’échelle du génome. Ils ont découvert que lorsque SNRPD2 est diminué, une enzyme clé du traitement de l’ARN, DDX39B, commence à dysfonctionner. Normalement, DDX39B aide à éliminer un intron particulier — un segment d’ARN qui doit être excisé — de son propre ARN. En l’absence de suffisamment de SNRPD2, cet intron est conservé, créant une version défectueuse de l’ARN de DDX39B que la cellule détruit rapidement. La baisse de DDX39B a ensuite un effet en cascade sur un autre gène, CTSC, qui code pour une enzyme protéolytique connue pour favoriser la croissance et la dissémination tumorales. Dans des conditions saines, un exon « cryptique » caché à l’intérieur de l’ARN de CTSC est ignoré, permettant la production d’une protéine CTSC complète et active. Avec moins de DDX39B, cet exon cryptique est inclus par erreur, insérant des signaux d’arrêt prématurés dans l’ARN. Le message CTSC malformé est dégradé avant de produire beaucoup de protéine, et les cellules cancéreuses perdent une partie de leur agressivité.
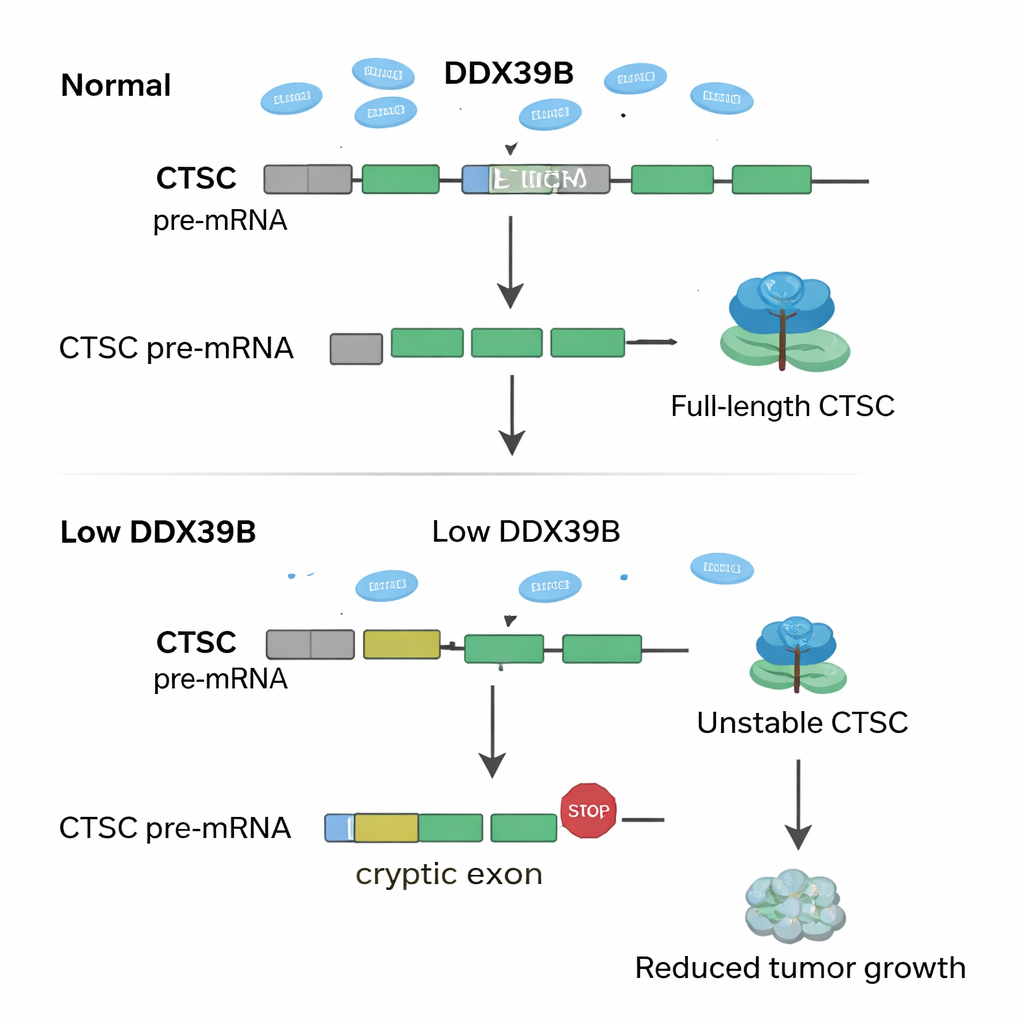
Ce que cela implique pour les traitements futurs
En résumé, les auteurs mettent au jour un système de relais — SNRPD2 → DDX39B → CTSC — que les cellules du cancer de l’endomètre exploitent pour prospérer. Un SNRPD2 élevé maintient DDX39B abondant ; DDX39B empêche à son tour CTSC d’utiliser des exons cryptiques délétères, préservant une protéine CTSC pleinement fonctionnelle qui aide les tumeurs à croître et à se propager. Lorsque SNRPD2 est bloqué, cette chaîne s’effondre, les niveaux de CTSC chutent et les tumeurs s’affaiblissent. Pour un public non spécialiste, l’idée clé est que les cellules cancéreuses dépendent d’un épissage de l’ARN très précis, et que de petites « erreurs » forcées peuvent empoisonner sélectivement leur croissance. Cibler SNRPD2 avec des médicaments antisens, ou forcer directement l’utilisation d’exons cryptiques dans CTSC, pourrait offrir de nouvelles thérapies plus ciblées pour les patients atteints de cancer de l’endomètre.
Citation: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Mots-clés: cancer de l’endomètre, épissage de l’ARN, SNRPD2, DDX39B, CTSC