Clear Sky Science · fr
DNMT2 inhibe la progression du cancer thyroïdien anaplasique en réduisant la production de 5’tiRNAGly-GCC
Pourquoi cette chimie cachée de l’ARN compte
Le cancer thyroïdien anaplasique fait partie des cancers humains les plus mortels, tuant souvent les patients en quelques mois malgré la chirurgie, la radiothérapie et la chimiothérapie. Cette étude met en lumière un coupable surprenant niché à l’intérieur des cellules tumorales : de minuscules marques chimiques sur les ARN de transfert, ces molécules qui aident à assembler les protéines. Les auteurs montrent que lorsqu’une enzyme particulière, DNMT2, est perdue ou réduite, les tumeurs thyroïdiennes croissent plus vite, se propagent plus facilement et résistent au médicament chimiothérapeutique courant doxorubicine. Plus intrigant encore, ils identifient un petit fragment d’ARN qui apparaît quand DNMT2 est bas et démontrent que bloquer ce fragment pourrait devenir une nouvelle stratégie thérapeutique.
Une enzyme protectrice qui disparaît
Les ARN de transfert (ARNt) transportent normalement les acides aminés vers la machinerie cellulaire de production des protéines, et leur stabilité dépend de décorations chimiques délicates. DNMT2 est une enzyme qui ajoute l’une de ces marques, appelée groupe méthyle, à des positions spécifiques sur l’ARNt. Dans de nombreux cancers, DNMT2 est élevé et pensé pour aider les tumeurs, mais ici l’histoire est inverse. En analysant de larges jeux de données de patients et des échantillons tumoraux, les chercheurs ont trouvé que les niveaux de DNMT2 sont significativement plus faibles dans les tissus de cancer thyroïdien anaplasique que dans la thyroïde normale. Les patients dont les tumeurs contenaient davantage de DNMT2 avaient tendance à vivre plus longtemps sans progression de la maladie, ce qui suggère que DNMT2 joue plutôt le rôle d’un frein que d’un accélérateur dans cette maladie.
Comment un faible DNMT2 alimente un comportement agressif
Pour déterminer ce que DNMT2 fait réellement dans les cellules cancéreuses, l’équipe a manipulé ses niveaux dans des lignées cellulaires de cancer thyroïdien anaplasique cultivées en laboratoire et dans des modèles murins. Lorsque DNMT2 était réduit, les cellules se multipliaient plus rapidement, infiltraient les membranes plus facilement et formaient davantage de colonies, autant de signes d’une tumeur agressive. Ces cellules devenaient également moins sensibles à la doxorubicine, un médicament de référence pour ce cancer. Chez la souris, des tumeurs modifiées pour exprimer moins de DNMT2 croissaient davantage et donnaient plus de métastases pulmonaires, tandis qu’une augmentation de l’expression de DNMT2 produisait l’effet inverse. Les chercheurs ont attribué en partie ces changements à l’activation d’un programme cellulaire connu sous le nom de transition épithélial–mésenchymateuse, qui rend les cellules cancéreuses plus mobiles et invasives.
De l’ARNt endommagé à de petits fragments nocifs
En creusant plus loin, l’étude montre que DNMT2 place une marque méthyle à une position spécifique (appelée C38) sur seulement trois types d’ARNt. Sans cette protection, ces ARNt deviennent plus vulnérables à la coupure par une autre enzyme, l’angiogénine. Cette coupure produit un court fragment d’ARN dérivé de l’ARNt-Gly-GCC, nommé 5’tiRNAGly-GCC. Grâce au séquençage et à des tests biochimiques, les auteurs ont montré que lorsque DNMT2 est bas, ce fragment s’accumule, en particulier à partir de l’ARNt transportant la glycine. Dans des expériences in vitro, l’ajout de la marque méthyle protégeait fortement l’ARNt contre la coupe, confirmant que DNMT2 protège normalement ces molécules contre leur fragmentation en morceaux plus petits et potentiellement nocifs.
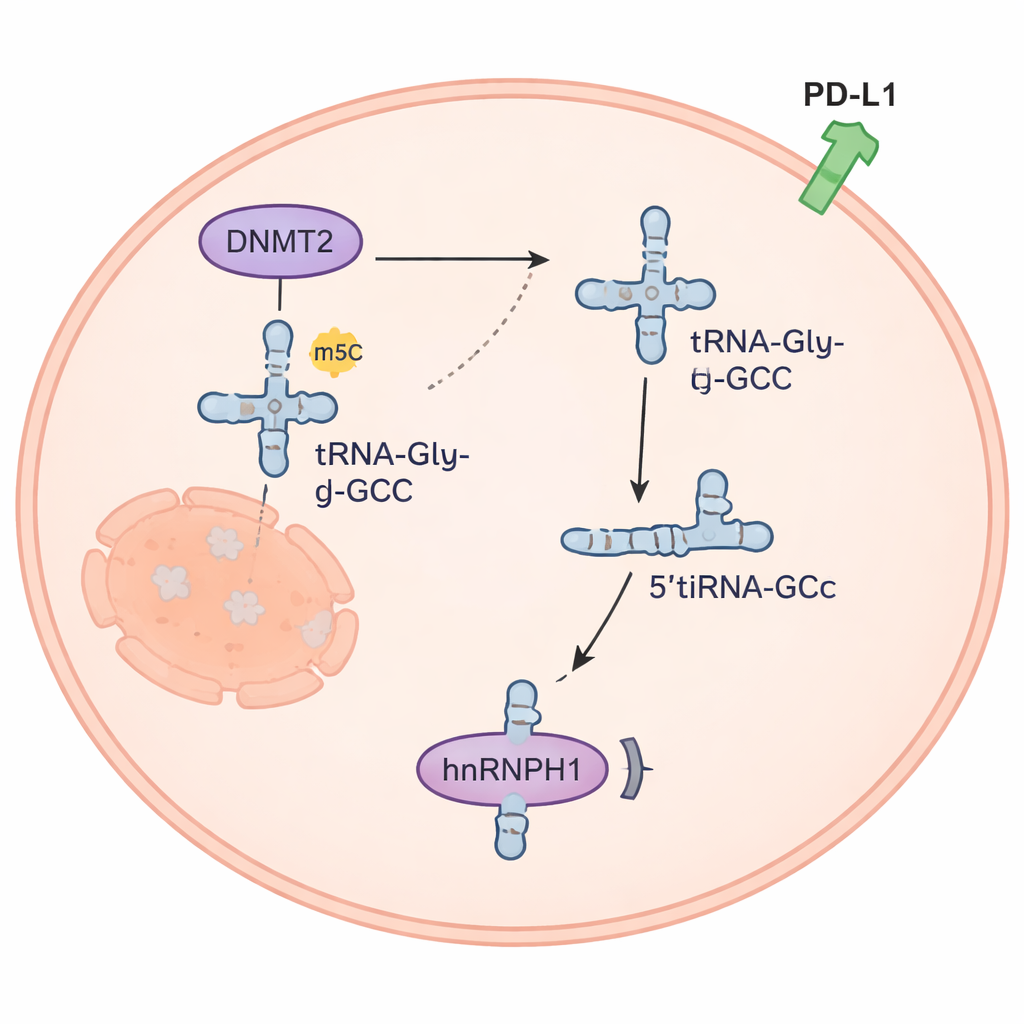
Un minuscule fragment d’ARN reprogramme les signaux du cancer
Le fragment 5’tiRNAGly-GCC s’est avéré être plus que de simples débris moléculaires. Il était abondant dans les cellules de cancer thyroïdien anaplasique mais rare dans les cellules thyroïdiennes normales. Lorsque les chercheurs ont augmenté artificiellement son niveau, les cellules cancéreuses proliféraient plus vite, envahissaient davantage et devenaient plus résistantes à la doxorubicine ; abaisser le fragment produisait l’effet inverse. Chez la souris, un inhibiteur chimiquement conçu de 5’tiRNAGly-GCC ralentissait la croissance tumorale, et la combinaison de cet inhibiteur avec la doxorubicine était encore plus efficace que chaque traitement seul. L’équipe a découvert que 5’tiRNAGly-GCC se lie à une protéine appelée hnRNPH1, en réduisant sa quantité à l’intérieur des cellules. Comme hnRNPH1 aide normalement à réguler à la baisse les niveaux de la protéine liée à l’immunité PD-L1, la perte de hnRNPH1 permet à PD-L1 d’augmenter, une modification qui peut aider les tumeurs à échapper à l’attaque immunitaire et qui est associée à l’accumulation de cellules T régulatrices autour des tumeurs.
Ce que cela signifie pour les traitements futurs
En termes simples, l’étude révèle une réaction en chaîne : lorsque DNMT2 est bas, certains ARNt perdent une marque protectrice, sont découpés en petits fragments, et l’un de ces fragments (5’tiRNAGly-GCC) désactive une protéine qui limite PD-L1. Il en résulte un cancer plus agressif, résistant aux médicaments et capable d’échapper au système immunitaire. Plutôt que d’essayer d’augmenter directement DNMT2 — ce qui pourrait être risqué dans d’autres tissus — les auteurs proposent de cibler le fragment d’ARN nocif lui-même. Leurs expériences murines avec un inhibiteur de 5’tiRNAGly-GCC, en particulier en association avec la doxorubicine, fournissent une preuve préliminaire que l’interruption de ce circuit microscopique d’ARN pourrait aider à maîtriser l’une des formes les plus létales de cancer thyroïdien.
Citation: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Mots-clés: cancer thyroïdien anaplasique, DNMT2, fragments d’ARN de transfert, chimiorésistance, PD-L1