Clear Sky Science · fr
Dévoiler ZNF124 comme nouveau déterminant dans la neurodégénérescence : orchestration de l’homéostasie des photorécepteurs via la régulation transcriptionnelle de MSX2
Pourquoi cette découverte compte pour la vision
La rétinite pigmentaire est une cause majeure de cécité héréditaire, et pourtant chez près de 40 % des patients les médecins ne parviennent toujours pas à identifier le gène en défaut. Cette étude met au jour un nouvel acteur génétique, nommé ZNF124, qui contribue à maintenir en vie les cellules sensibles à la lumière de l’œil. En montrant comment une mutation de ce gène perturbe une chaîne de « commutateurs » moléculaires dans la rétine, les chercheurs ouvrent de nouvelles voies pour le diagnostic et, potentiellement, des traitements ciblés pour les personnes en perte de vision.
Une cause cachée de perte de vision héréditaire
Les chercheurs ont étudié une grande famille dont plusieurs enfants ont développé des signes classiques de rétinite pigmentaire : cécité nocturne précoce, rétrécissement du champ visuel périphérique et perte progressive de la vision centrale. Des examens oculaires approfondis ont révélé un amincissement de la rétine et des réponses électriques affaiblies à la lumière, deux signes caractéristiques de lésions des photorécepteurs en bâtonnets et en cônes. Pourtant aucun des plus de 80 gènes connus de la rétinite pigmentaire ne présentait de défauts évidents chez ces patients, suggérant qu’un gène encore non identifié pouvait être responsable de leur maladie.
Identifier un commutateur génétique défectueux
En utilisant le séquençage de l’exome entier, qui lit les portions codantes de l’ADN, l’équipe a identifié une mutation rare et jusque-là non rapportée dans le gène ZNF124. Cette mutation modifie l’assemblage de l’ARN du gène, supprimant quelques bases à une jonction critique. En conséquence, la protéine ZNF124 est tronquée et perd sa région en doigt de zinc, une structure normalement utilisée pour reconnaître et se lier à des séquences d’ADN spécifiques. Comme les protéines à doigt de zinc agissent souvent comme des commutateurs maîtres qui activent ou répriment de nombreux autres gènes, un ZNF124 endommagé pourrait entraîner des effets étendus dans les cellules rétiniennes.
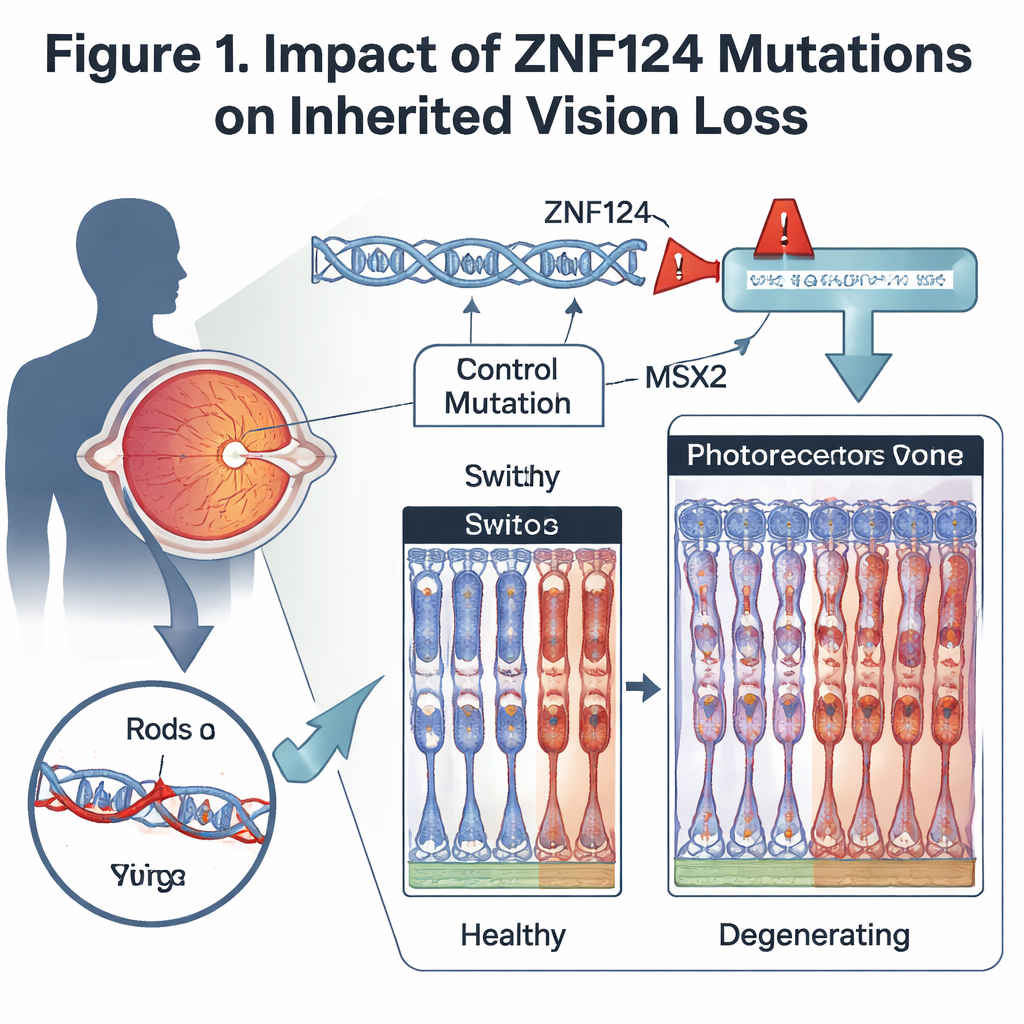
Tester le gène dans des modèles animaux
Pour évaluer comment la perte de ce commutateur affecte l’œil, les scientifiques ont créé des souris dépourvues de Gm20541, l’équivalent murin le plus proche de ZNF124, spécifiquement dans la rétine. Ces animaux ont développé des troubles visuels dépendant de l’âge : leurs réponses électriques à la lumière faible et intense se sont affaiblies, et l’examen microscopique a montré un amincissement progressif de la couche rétinienne contenant les photorécepteurs. Bâtonnets, qui soutiennent la vision nocturne, et cônes, qui soutiennent la vision diurne et la perception des couleurs, présentaient des segments externes raccourcis et une perte de protéines visuelles clés. D’autres cellules rétiniennes, comme certains bipolaires, étaient également réduites, et les cellules de soutien se sont activées, une réponse courante aux lésions rétiniennes chroniques.
Mettre au jour la voie de contrôle ZNF124–MSX2
La question suivante était de savoir quels gènes ZNF124 contrôle normalement. En combinant des méthodes biochimiques qui cartographient la position des protéines sur l’ADN et des relevés transcriptomiques globaux des rétines de souris, l’équipe a montré que ZNF124 se lie et active un autre gène appelé MSX2. Dans des cellules saines, ZNF124 se fixe à une courte séquence spécifique dans la région « on-switch » de MSX2 et en stimule l’activité. Chez les souris dépourvues de Gm20541, les niveaux de MSX2 chutaient de plus de moitié. Lorsque les chercheurs ont supprimé MSX2 spécifiquement dans les cellules en bâtonnets, ces animaux ont aussi présenté un amincissement de la couche des photorécepteurs et des segments externes raccourcis, reflétant les défauts observés chez les souris knock-out de type ZNF124. Cela place MSX2 directement en aval de ZNF124 dans une voie essentielle à la survie des photorécepteurs.
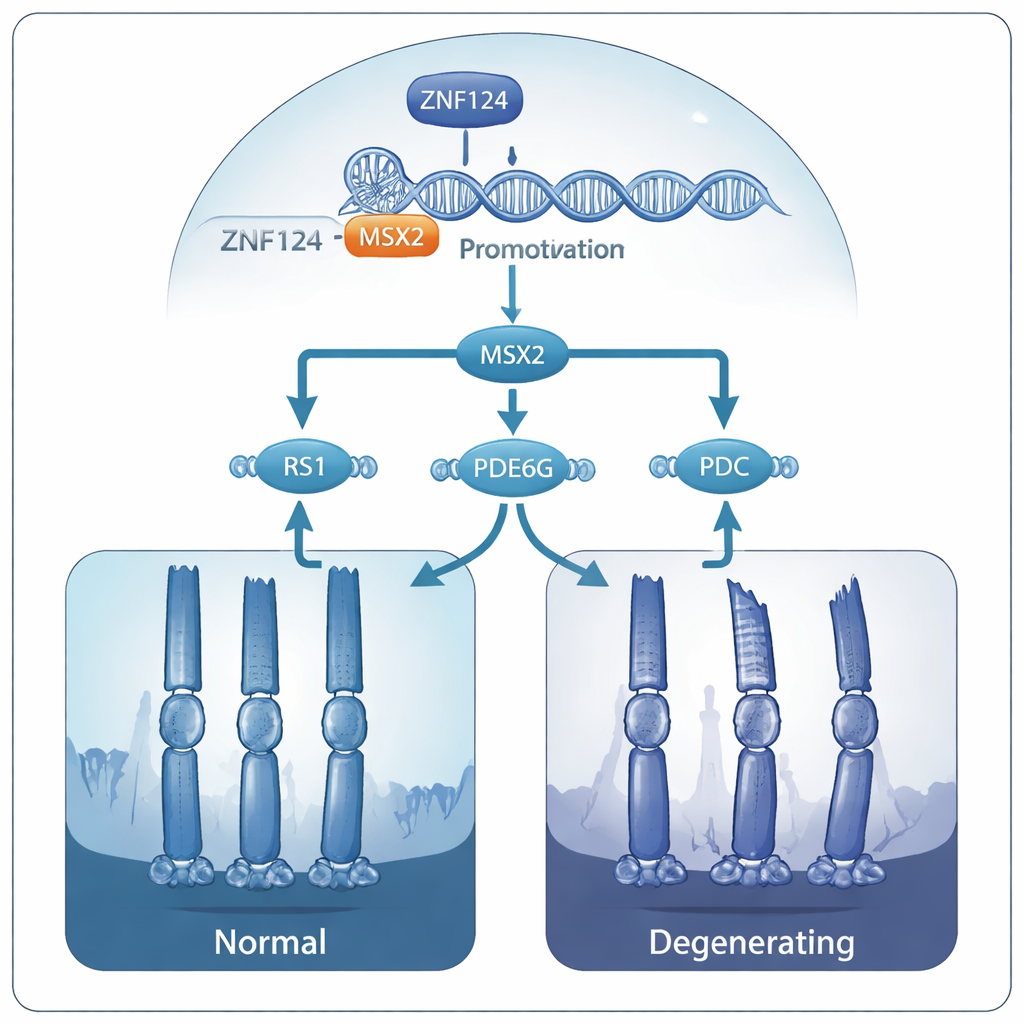
Des commutateurs génétiques aux photorécepteurs fragiles
Des analyses supplémentaires ont montré que MSX2 contribue à maintenir plusieurs autres gènes déjà liés aux maladies rétiniennes héréditaires : RS1, PDE6G et PDC. Ces gènes soutiennent la structure de la rétine et la chimie du signal visuel. Lorsque MSX2 diminuait, les trois gènes voyaient leur activité réduite et leurs produits protéiques déclinaient. Les auteurs proposent que, chez les personnes porteuses de mutations délétères de ZNF124, toute cette cascade est affaiblie : ZNF124 ne peut plus activer pleinement MSX2, MSX2 ne parvient pas à soutenir RS1, PDE6G et PDC, et avec le temps les photorécepteurs perdent leur intégrité structurale puis meurent, conduisant à une perte de vision progressive.
Ce que cela signifie pour les patients et les thérapies
Pour un non‑spécialiste, le message central est que la rétine dépend d’une hiérarchie finement réglée de commutateurs génétiques. Ce travail identifie ZNF124 comme un nouveau commutateur de premier plan dont la défaillance peut provoquer une cécité héréditaire via un partenaire en aval spécifique, MSX2, et ses gènes cibles. Sur le plan clinique, ZNF124 peut désormais être ajouté aux panels de tests génétiques, aidant davantage de familles à obtenir des diagnostics précis. À plus long terme, des thérapies visant à restaurer l’activité de ZNF124, de MSX2 ou des gènes en aval affectés pourraient stabiliser ou sauver les cellules sensibles à la lumière, offrant un nouvel espoir pour les personnes atteintes de formes de rétinite pigmentaire actuellement inexpliquées.
Citation: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
Mots-clés: rétinite pigmentaire, photorécepteurs, ZNF124, MSX2, maladie rétinienne héréditaire