Clear Sky Science · fr
TIGAR maintient la régénération épithéliale intestinale en stabilisant HMGCL et en favorisant la β‑hydroxybutyrylation de β‑caténine dans la sepsie induite par des brûlures
Pourquoi la réparation intestinale compte après des brûlures sévères
Les brûlures sévères n’endommagent pas seulement la peau ; elles peuvent aussi provoquer des conséquences profondes à l’intérieur du corps, en particulier au niveau des intestins. Lorsque la muqueuse intestinale se détériore, bactéries et toxines peuvent passer dans le sang, entraînant des infections graves et une défaillance d’organes. Cette étude examine comment un « interrupteur » métabolique naturel dans les cellules intestinales aide l’intestin à se réparer après une sepsie liée à des brûlures, et comment la perturbation de cet interrupteur peut transformer une lésion gérable en une crise potentiellement mortelle.
Une équipe de réparation cachée dans la muqueuse
L’intérieur de l’intestin grêle est couvert de petites projections en forme de doigts appelées villosités, qui se renouvellent en permanence. Ce renouvellement dépend de cellules souches intestinales nichées dans des replis à la base des villosités. Après des brûlures majeures et une sepsie, les chercheurs ont constaté que la structure de l’intestin de souris était gravement endommagée : les villosités se rétrécissaient, les niches régénératives disparaissaient et les marqueurs de prolifération cellulaire diminuaient. Parallèlement, les niveaux d’une protéine appelée TIGAR, normalement enrichie dans ces régions régénératives, chutaient fortement. Les souris présentant une baisse de TIGAR dans leurs cellules intestinales ont montré des lésions plus sévères et une activité réduite des cellules souches, suggérant que TIGAR agit comme un protecteur interne de la régénération intestinale en cas de maladie grave. 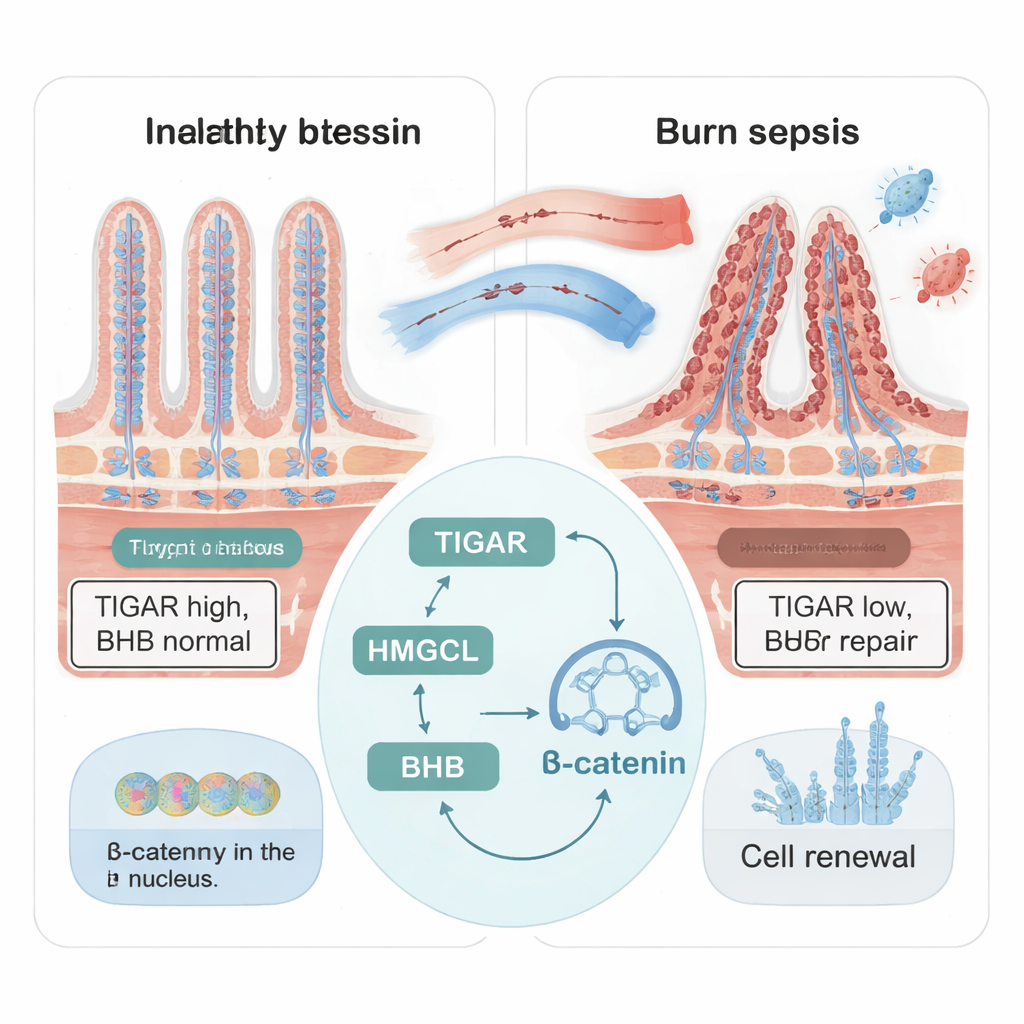
Alimenter la réparation avec une molécule issue des graisses
Les cellules intestinales peuvent utiliser non seulement le sucre et les acides aminés comme carburant, mais aussi les corps cétoniques — des molécules dérivées des graisses produites principalement dans le foie et, dans une moindre mesure, dans l’intestin. L’équipe s’est concentrée sur le β‑hydroxybutyrate (BHB), le corps cétonique le plus abondant, connu pour soutenir les cellules souches et le renouvellement tissulaire. Chez les souris avec sepsie induite par brûlure, les niveaux de BHB intestinaux augmentaient d’abord puis s’effondraient pour atteindre environ un tiers de la normale au septième jour, coïncidant avec la période de lésion maximale. Quand TIGAR était réduit dans les cellules intestinales, les niveaux de BHB diminuaient aussi. L’ajout de BHB dans des modèles cellulaires et des organoïdes a restauré la croissance cellulaire, rétabli les marqueurs des cellules souches et contré les effets délétères du stress inflammatoire, montrant que le BHB est un carburant et un signal clé pour la réparation intestinale.
Comment TIGAR maintient le moteur cétonique en marche
En creusant davantage, les chercheurs ont découvert comment TIGAR soutient la production de BHB. À l’intérieur des cellules intestinales, l’enzyme HMGCL constitue une étape cruciale de la synthèse des corps cétoniques. TIGAR se lie directement à HMGCL dans les mitochondries, les centrales énergétiques de la cellule. Cette interaction protège HMGCL d’une autre protéine, Park2, qui a pour rôle d’étiqueter HMGCL par des chaînes d’ubiquitine destinées au système de dégradation cellulaire. En bloquant cet étiquetage, TIGAR empêche la dégradation de HMGCL, maintenant ainsi la production de cétones. Lorsque TIGAR est supprimé ou que les cellules sont soumises à des toxines bactériennes, HMGCL devient instable, la production de BHB chute et la prolifération cellulaire ralentit ; restaurer HMGCL ou ajouter du BHB inverse nombre de ces défauts.
Une impulsion moléculaire qui envoie des signaux de croissance au noyau
Le BHB ne se contente pas de fournir de l’énergie : il modifie aussi des protéines. L’étude montre que le BHB ajoute une petite marque chimique, appelée β‑hydroxybutyrylation, à un site spécifique (lysine 335) sur la β‑caténine, un commutateur maître qui active les gènes de croissance et de renouvellement des cellules souches. Avec suffisamment de BHB, la β‑caténine portant cette marque migre vers le noyau cellulaire et s’associe à un autre facteur, TCF4, pour activer des gènes pro‑prolifération. Lorsque le BHB est faible, ou lorsque ce site spécifique de la β‑caténine est muté, la β‑caténine peine à entrer dans le noyau et le programme de croissance s’interrompt. TIGAR, en maintenant HMGCL et le BHB, contrôle donc indirectement si la β‑caténine peut atteindre le noyau et assurer le renouvellement de la muqueuse intestinale. 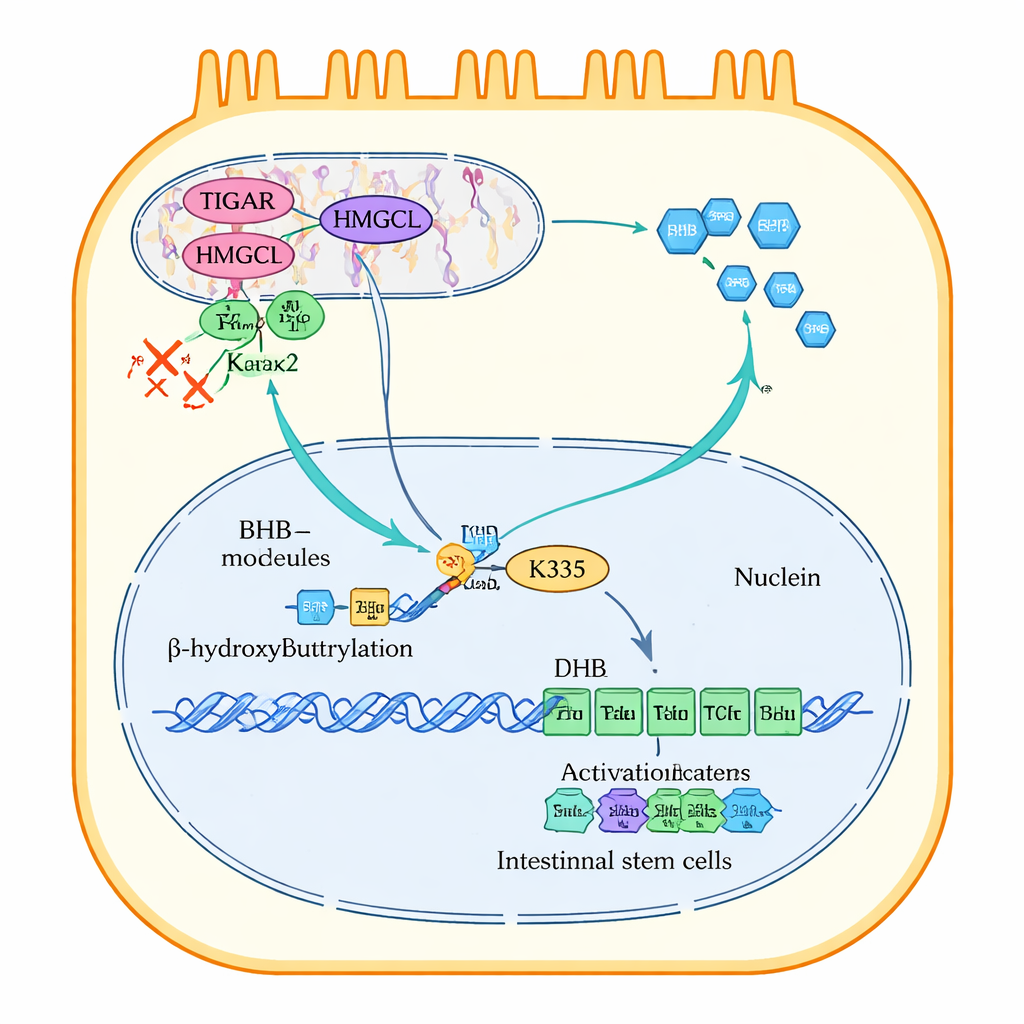
Ce que cela signifie pour les patients brûlés
En termes simples, ce travail révèle une réaction en chaîne : TIGAR protège une enzyme productrice de cétones (HMGCL), qui maintient des niveaux de BHB ; le BHB module ensuite un commutateur de croissance (β‑caténine) qui ordonne aux cellules souches intestinales de se diviser et de reconstruire la barrière intestinale. Lorsque les niveaux de TIGAR chutent après des brûlures sévères et une sepsie, cette chaîne protectrice se rompt, la réparation intestinale faiblit et la défaillance de la barrière aggrave les infections. Cibler cette voie TIGAR–HMGCL–BHB–β‑caténine — en renforçant la fonction de TIGAR, en stabilisant HMGCL ou en supplémentant prudemment le BHB — pourrait offrir de nouvelles approches pour préserver l’intégrité intestinale et améliorer la survie des patients souffrant de brûlures sévères et d’autres maladies critiques menaçant la barrière intestinale.
Citation: Zhang, P., Wu, D., Wei, Y. et al. TIGAR maintains intestinal epithelial regeneration by stabilizing HMGCL and promoting β-catenin β-hydroxybutyrylation in burn-induced sepsis. Cell Death Dis 17, 233 (2026). https://doi.org/10.1038/s41419-026-08486-7
Mots-clés: réparation de la barrière intestinale, corps cétoniques, TIGAR, sepsie par brûlure, cellules souches intestinales