Clear Sky Science · fr
La Lox induite par HIF2α protège la réussite de la grossesse en remodelant les collagènes à l’interface fœto-maternelle
Pourquoi l’utérus doit se préparer à une nouvelle arrivée
Avant qu’une grossesse puisse s’installer, un embryon précoce doit accomplir quelque chose de remarquable : s’enfouir dans la paroi de l’utérus et établir un système de soutien vital, le placenta. Cet article examine comment les tissus maternels se réorganisent discrètement pour accueillir l’embryon, en se concentrant sur la manière dont de faibles niveaux d’oxygène et une enzyme encore peu connue préparent la muqueuse utérine. Comprendre cette chorégraphie finement réglée pourrait éclairer les raisons pour lesquelles certaines grossesses échouent très tôt et suggérer de nouvelles voies pour prévenir l’infertilité et les complications de la grossesse.
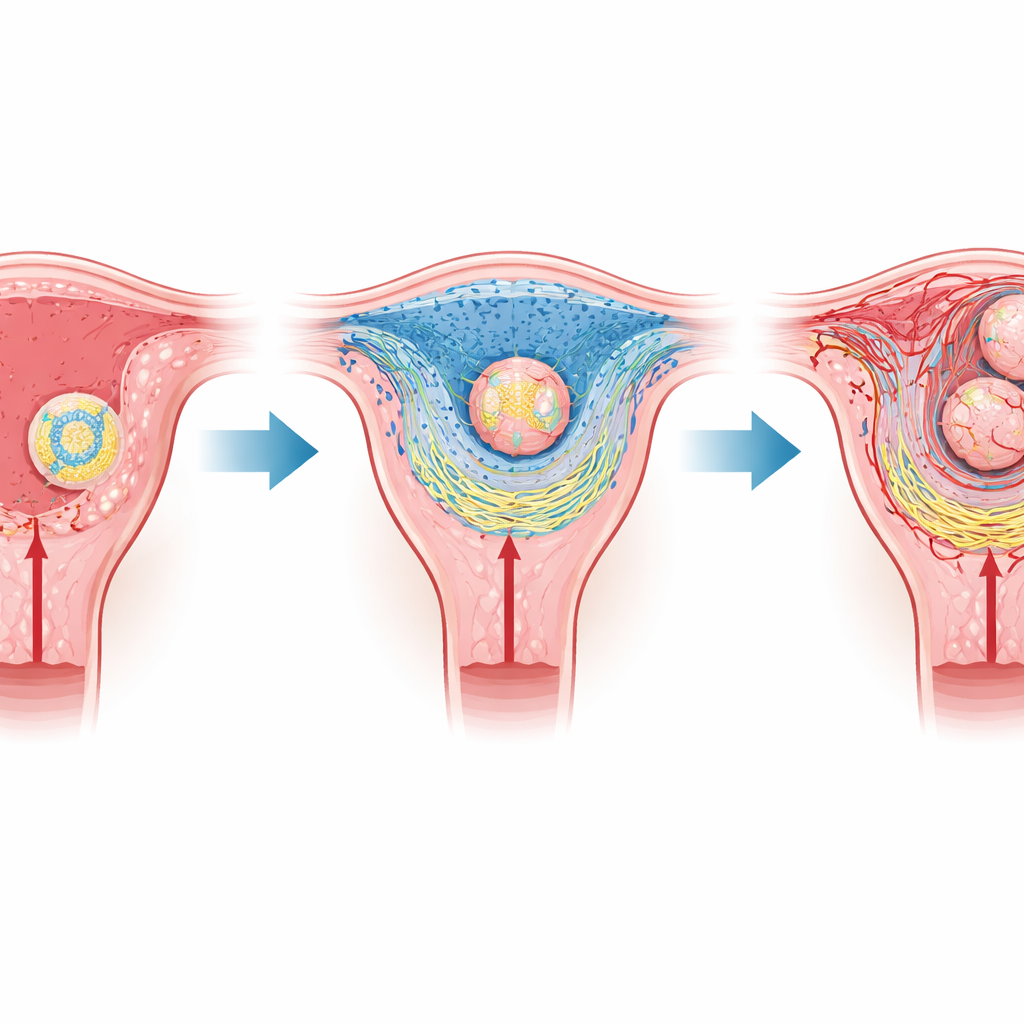
Une rencontre délicate entre la mère et l’embryon
Chez les mammifères comme la souris et l’humain, la phase la plus précoce de la grossesse dépend de l’implantation, lorsque l’embryon s’attache puis envahit la muqueuse utérine. L’embryon est entouré d’une couche de cellules spécialisées qui formeront plus tard le placenta, tandis que les tissus maternels se transforment en une couche semblable à un coussinet appelée décidue. La région la plus proche de l’embryon est une zone mince nommée zone déciduale primaire, dépourvue de vaisseaux sanguins et contenant donc peu d’oxygène. Des travaux antérieurs ont montré que cette poche naturellement hypoxique aide à déclencher l’implantation, mais on comprenait mal comment une condition physique aussi simple pouvait réorganiser des tissus entiers.
Le faible oxygène comme interrupteur caché
Les auteurs ont utilisé une technique puissante appelée transcriptomique spatiale, qui cartographie l’activité génétique directement sur des coupes de tissu, pour étudier l’utérus de souris pendant les jours où les embryons s’attachent et envahissent. Ils se sont concentrés sur une protéine appelée HIF2α, qui s’active en conditions de faible oxygène et joue le rôle d’un interrupteur génétique. Chez les souris normales, les cellules de la zone déciduale primaire montraient une forte activité de gènes liés à l’hypoxie et à la construction du matériau d’échafaudage environnant, y compris des collagènes qui constituent la matrice extracellulaire. Lorsque HIF2α était supprimé uniquement dans l’utérus, l’agencement global des types cellulaires paraissait étonnamment normal. Mais à haute résolution, le réseau de collagène était désorganisé, la surface épithéliale ne s’ouvrait pas correctement et les cellules embryonnaires peinaient à pénétrer les tissus maternels.
Une enzyme qui réticulise l’échafaudage
En approfondissant, l’équipe a identifié un acteur clé en aval de HIF2α : la lysyl oxydase, ou Lox, une enzyme qui réticulise chimiquement les fibres de collagène et contribue à raidir et stabiliser les tissus. Lors des grossesses normales, les niveaux de Lox augmentaient fortement autour des embryons précisément au moment où ceux-ci commençaient à envahir. Dans des utérus dépourvus de HIF2α, l’expression de Lox chutait et les fibres de collagène apparaissaient fragmentées au lieu de former un maillage dense. Pour tester directement l’importance de Lox, les chercheurs ont généré des souris où Lox était supprimée uniquement dans l’utérus. Ces femelles devenaient enceintes moins souvent, portaient moins d’embryons et présentaient fréquemment des signes de perte embryonnaire et de saignement plus tard dans la gestation, bien que les étapes initiales d’attachement et d’épaississement tissulaire semblent d’abord normales.
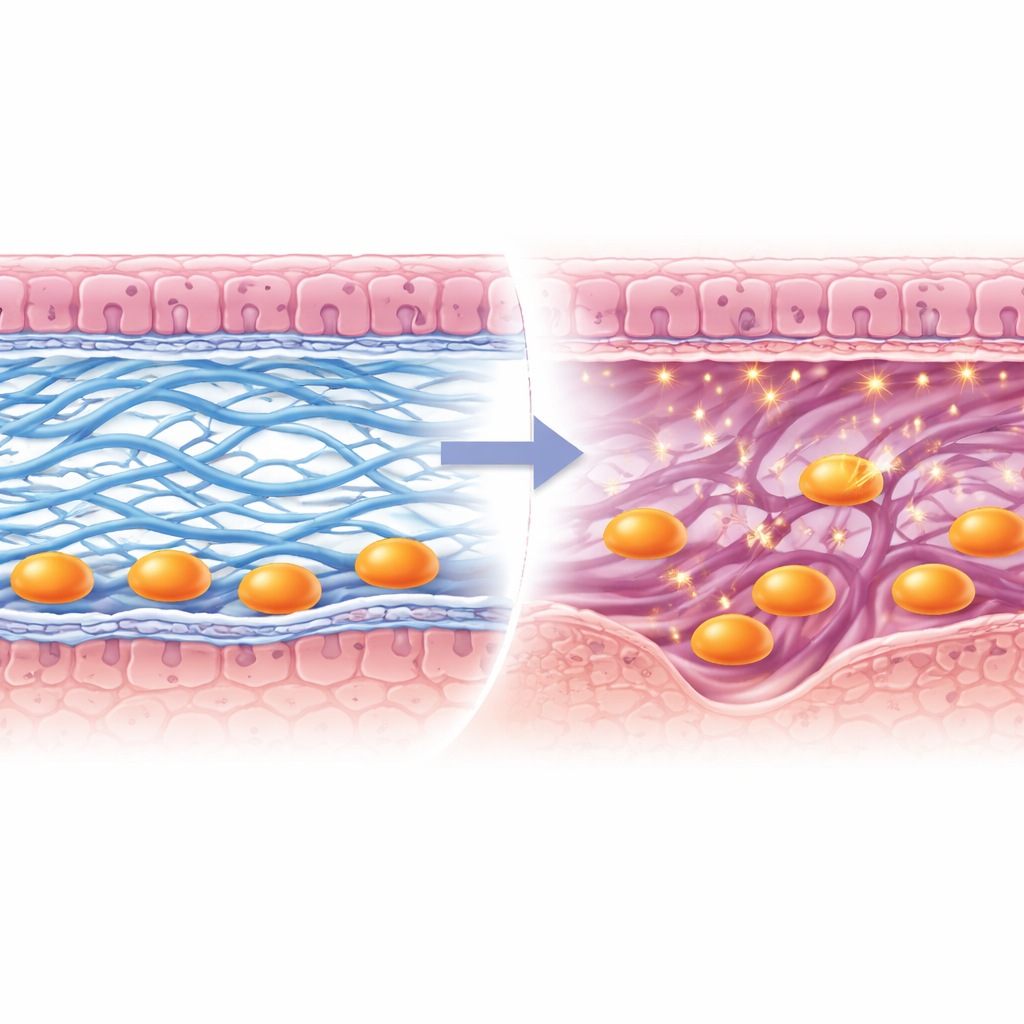
Ouvrir un passage pour le placenta
Des images détaillées ont révélé ce qui dysfonctionnait en l’absence de Lox. Une mince couche riche en protéines appelée membrane basale, qui se désagrège normalement pour laisser passer les cellules embryonnaires, restait en grande partie intacte. Les fibres de collagène de type I dans le stroma sous-jacent ne formaient pas de faisceaux robustes et continus, tandis que le collagène de type IV de la membrane basale ne se dégageait pas correctement à proximité des cellules envahissantes. En conséquence, les cellules trophoblastiques — les pionniers dérivés de l’embryon qui bâtissent le placenta — restaient piégées en surface au lieu de creuser un passage dans la couche maternelle. L’équipe a également constaté qu’une enzyme qui coupe le collagène, Mmp9, n’était pas activée dans ces trophoblastes, entravant encore leur progression. Avec le temps, les structures placentaires se formaient mal, les embryons croissaient de façon anormale et le taux de réussite de la grossesse diminuait.
Ce que cela signifie pour la santé de la grossesse
En somme, les résultats décrivent une chaîne d’événements dans laquelle la faible oxygénation de la zone d’implantation active HIF2α, qui à son tour stimule Lox. Lox remodelle et réticulise alors les fibres de collagène et contribue au démantèlement de la membrane basale, tout en permettant à des enzymes comme Mmp9 de dégager un passage. Ce remodelage fournit à la fois un échafaudage structurel et une porte ouverte pour que les cellules trophoblastiques envahissent et construisent le placenta. Pour un lecteur non spécialiste, le message est que la réussite d’une grossesse dépend non seulement d’un embryon sain et d’un équilibre hormonal, mais aussi de la réorganisation discrète de l’architecture tissulaire maternelle. Des perturbations de cette voie hypoxie–HIF2α–Lox pourraient sous-tendre certains cas d’infertilité inexpliquée, de fausse couche et de pathologies liées à une invasion placentaire déficiente, suggérant de nouveaux marqueurs diagnostiques et cibles thérapeutiques pour soutenir le début de grossesse.
Citation: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Mots-clés: implantation embryonnaire, matrice extracellulaire utérine, lysyl oxydase, invasion trophoblastique, développement placentaire