Clear Sky Science · fr
Cibler la phosphatase mitochondriale PGAM5 atténue la ferroptose et la pancréatite aiguë en augmentant l’expression de FSP1 médiée par NRF2
Pourquoi les cellules stressées et les pancréas douloureux comptent
Lorsque les cellules sont soumises à un excès de contraintes, elles peuvent mourir d’une façon qui endommage l’ensemble de l’organisme. Une de ces formes de mort cellulaire, appelée ferroptose, est entraînée par le fer et des réactions chimiques incontrôlées qui « rouillent » les lipides des membranes cellulaires. Ce processus a été associé à des lésions d’organes, notamment à une affection douloureuse et parfois mortelle connue sous le nom de pancréatite aiguë. L’étude décrite ici met au jour un commutateur de contrôle clé au sein des mitochondries — les centrales énergétiques de la cellule — capable d’amplifier ou de réduire la ferroptose, et montre comment bloquer ce commutateur peut protéger le pancréas dans un modèle murin.
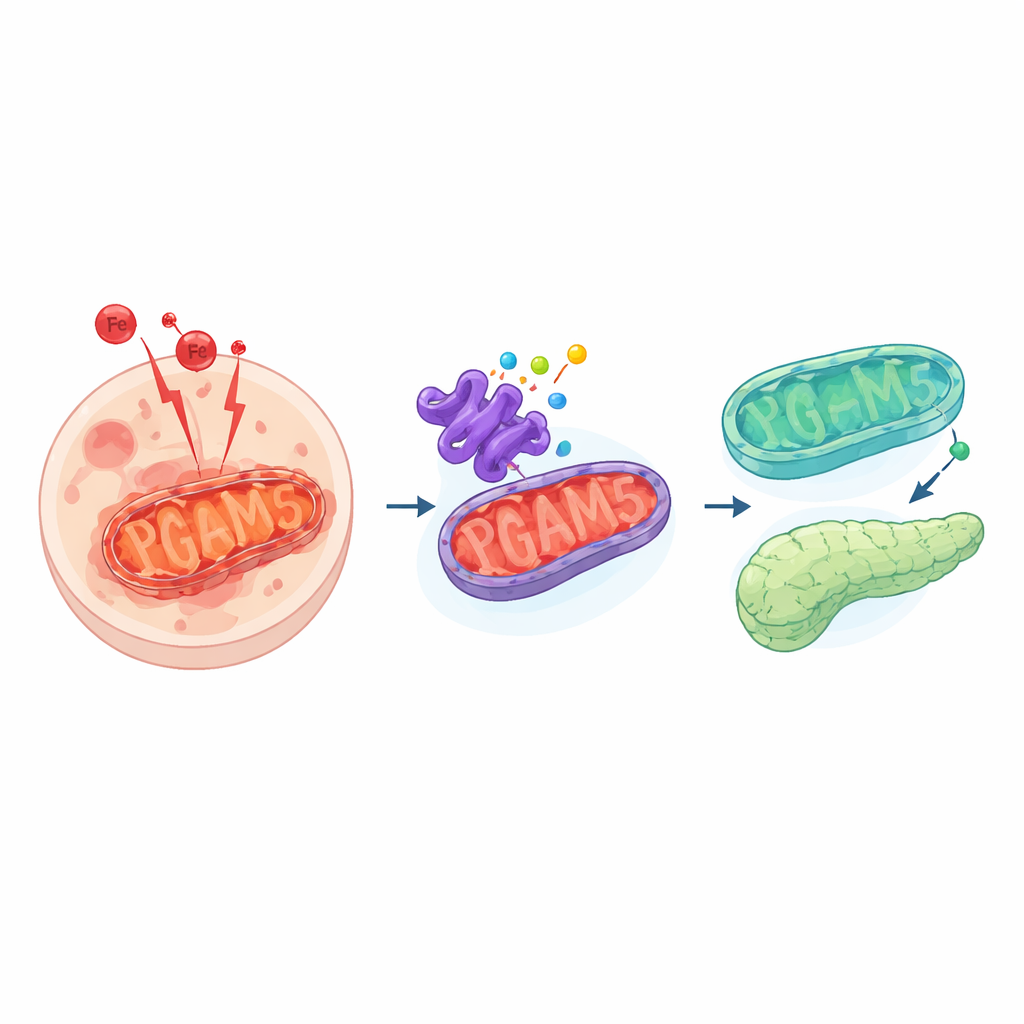
Une forme dangereuse de mort cellulaire
La ferroptose se distingue des formes de mort cellulaire plus familières comme l’apoptose. Plutôt que d’être une autodestruction ordonnée, les cellules soumises à la ferroptose subissent une tempête de réactions induites par le fer qui rendent rances les lipides délicats de leurs membranes. Cela crée des sous-produits toxiques et des perforations membranaires qui finissent par tuer la cellule. Habituellement, les cellules limitent ce phénomène grâce à des systèmes protecteurs qui neutralisent ces molécules réactives. Lorsque ces systèmes échouent ou sont dépassés, la ferroptose peut propager des dommages dans les tissus et contribuer à des maladies allant du cancer à l’insuffisance d’organes.
Un commutateur mitochondrial dans la ligne de mire
Les chercheurs se sont intéressés à une protéine appelée PGAM5, située à la face interne des mitochondries et agissant comme un centre de signalisation. PGAM5 aide à réguler la forme mitochondriale, répond au stress et influence la gestion de l’oxydation par la cellule. De manière surprenante, lorsque l’équipe a soit diminué PGAM5 soit forcé les cellules à en produire davantage, les cellules sont devenues plus difficiles à tuer par ferroptose. L’inhibition chimique de PGAM5, son amorcissement génétique et sa surexpression ont tous réduit l’accumulation de sous-produits lipidiques nuisibles et diminué la mortalité cellulaire déclenchée par un agent inducteur de ferroptose. Cela révèle que le système est finement réglé : trop peu ou trop de PGAM5 rendent les cellules plus protégées.
Activation d’un bouclier interne
En approfondissant, les auteurs ont découvert que l’influence de PGAM5 passe par un axe protecteur impliquant deux autres acteurs : NRF2 et FSP1. NRF2 est un régulateur maître qui, lorsqu’il est actif dans le noyau, active un large éventail de défenses antioxydantes. FSP1 est l’un de ses effecteurs en aval qui aide à régénérer un antioxydant liposoluble, empêchant les dommages lipidiques au niveau de la membrane. Lorsque les niveaux de PGAM5 étaient modifiés, les cellules augmentaient à la fois les transcriptions et les niveaux protéiques de NRF2, et NRF2 se déplaçait plus facilement du cytoplasme vers le noyau. Là, il stimulait la production de FSP1. Bloquer FSP1 ou NRF2 supprimait la protection et rétablissait la sensibilité à la ferroptose, ce qui montre que la chaîne PGAM5–NRF2–FSP1 est essentielle à la résilience observée.
Le stress énergétique comme messager caché
L’étude a également mis au jour comment le stress mitochondrial se traduit en cette réponse protectrice. La perturbation de PGAM5 déréglait l’équilibre mitochondrial et faisait basculer la monnaie énergétique cellulaire : le rapport des molécules à faible énergie (AMP et ADP) par rapport à l’ATP élevé augmentait, signalant un stress énergétique. Cela activait à son tour l’enzyme détectrice d’énergie AMPK. L’AMPK activée modifiait directement NRF2 d’une manière favorisant son entrée dans le noyau, augmentant encore la production de FSP1. Lorsque l’AMPK était retirée du système, NRF2 ne s’accumulait plus dans le noyau, les niveaux de FSP1 chutaient et les cellules succombaient de nouveau à la ferroptose. Ainsi, PGAM5 relie l’état mitochondrial à une réponse énergétique et antioxydante plus large qui protège les cellules contre la mort induite par le fer.
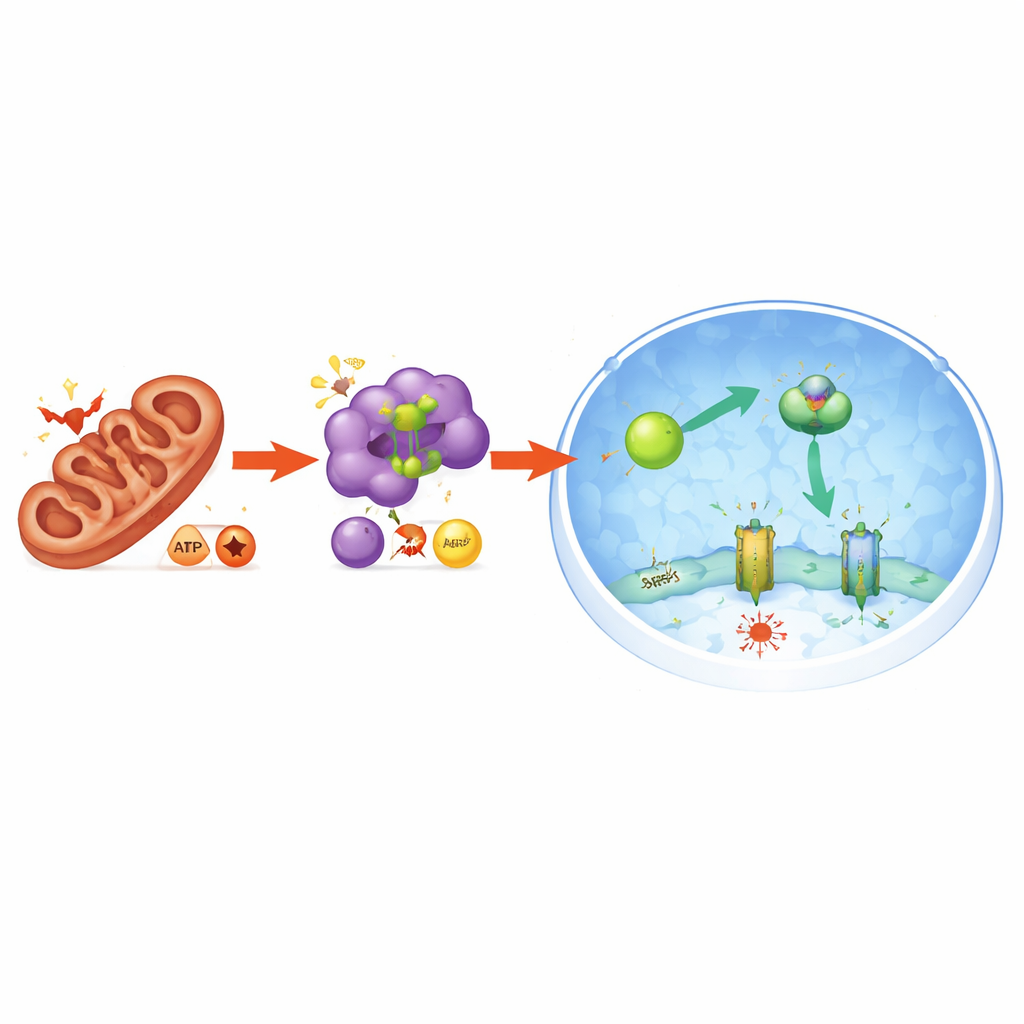
Protéger le pancréas chez l’animal vivant
Pour tester si ce mécanisme a un impact au niveau d’un organe entier, les scientifiques ont eu recours à un modèle murin de pancréatite aiguë déclenchée par de fortes doses de l’acide aminé arginine. Dans ce modèle, le pancréas présente des lésions étendues, des niveaux élevés d’enzymes sanguines indiquant des lésions tissulaires et une poussée de molécules inflammatoires. Les marqueurs de la peroxydation lipidique — signature de la ferroptose — augmentaient également fortement dans le pancréas. Le traitement des souris par un composé inhibiteur de PGAM5 a atténué ces symptômes : les marqueurs sanguins de lésions ont diminué, le tissu pancréatique paraissait plus sain au microscope et les signaux inflammatoires ont reculé. Parallèlement, les marqueurs de ferroptose ont diminué, tandis que l’activité d’AMPK, NRF2 et les niveaux de FSP1 augmentaient dans le pancréas, correspondant à la voie protectrice observée en culture cellulaire.
Ce que cela signifie pour de futurs traitements
En somme, ce travail identifie PGAM5 comme un point de contrôle central reliant le stress mitochondrial, l’état énergétique cellulaire et un puissant programme antioxydant qui bloque la ferroptose. En réduisant l’activité de PGAM5, les cellules activent AMPK et NRF2, augmentent FSP1 et résistent mieux aux dommages lipidiques induits par le fer. Chez la souris, cette stratégie réduit les lésions pancréatiques dans la pancréatite aiguë. Pour le lecteur non spécialiste, le message est que les chercheurs ont identifié un « disjoncteur » interne capable d’empêcher une forme destructrice de mort cellulaire. Bien qu’il reste beaucoup à faire avant une application clinique, cibler PGAM5 ou ses partenaires en aval pourrait ouvrir de nouvelles pistes pour traiter des affections où la ferroptose et la défaillance mitochondriale jouent un rôle néfaste.
Citation: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Mots-clés: ferroptose, mitochondries, pancréatite aiguë, stress oxydatif, mort cellulaire