Clear Sky Science · fr
La ciblage de la synthase des acides gras supprime le développement tumoral dans le mésothéliome pleural déficient en NF2/CDKN2A
Pourquoi cela compte pour les personnes exposées à l’amiante
Le mésothéliome pleural est un cancer rare mais presque toujours mortel qui se développe sur la membrane entourant les poumons, le plus souvent après une exposition à l’amiante des décennies plus tôt. Une fois diagnostiqué, il est difficile à traiter et résiste généralement à la chimiothérapie standard. Cette étude explore une autre approche : au lieu d’attaquer la tumeur avec des médicaments traditionnels, les chercheurs tentent d’affamer les cellules cancéreuses en coupant une source clé de leurs éléments de construction et d’énergie, ouvrant la voie à un traitement plus ciblé pour un sous-groupe génétique majeur du mésothéliome.
Comment les cellules tumorales détournent la machinerie de fabrication des lipides
Beaucoup de cancers augmentent l’activité d’une enzyme appelée synthase des acides gras, qui assemble des acides gras à longue chaîne utilisés par les cellules pour construire des membranes, stocker de l’énergie et contrôler la signalisation. L’équipe s’est concentrée sur des cellules de mésothéliome dépourvues de deux gènes protecteurs contre les tumeurs, NF2 et CDKN2A (également appelé p16), altérations fréquentes dans cette maladie. En testant 364 composés anticancéreux, ils ont trouvé qu’une molécule, la cérulénine, qui bloque la synthase des acides gras, était particulièrement efficace pour ralentir la croissance des cellules de mésothéliome déficientes en NF2/p16. En revanche, d’autres médicaments, y compris un autre inhibiteur de la synthase des acides gras appelé C75 et les agents standards cisplatine et pemetrexed, étaient beaucoup moins efficaces à doses comparables.
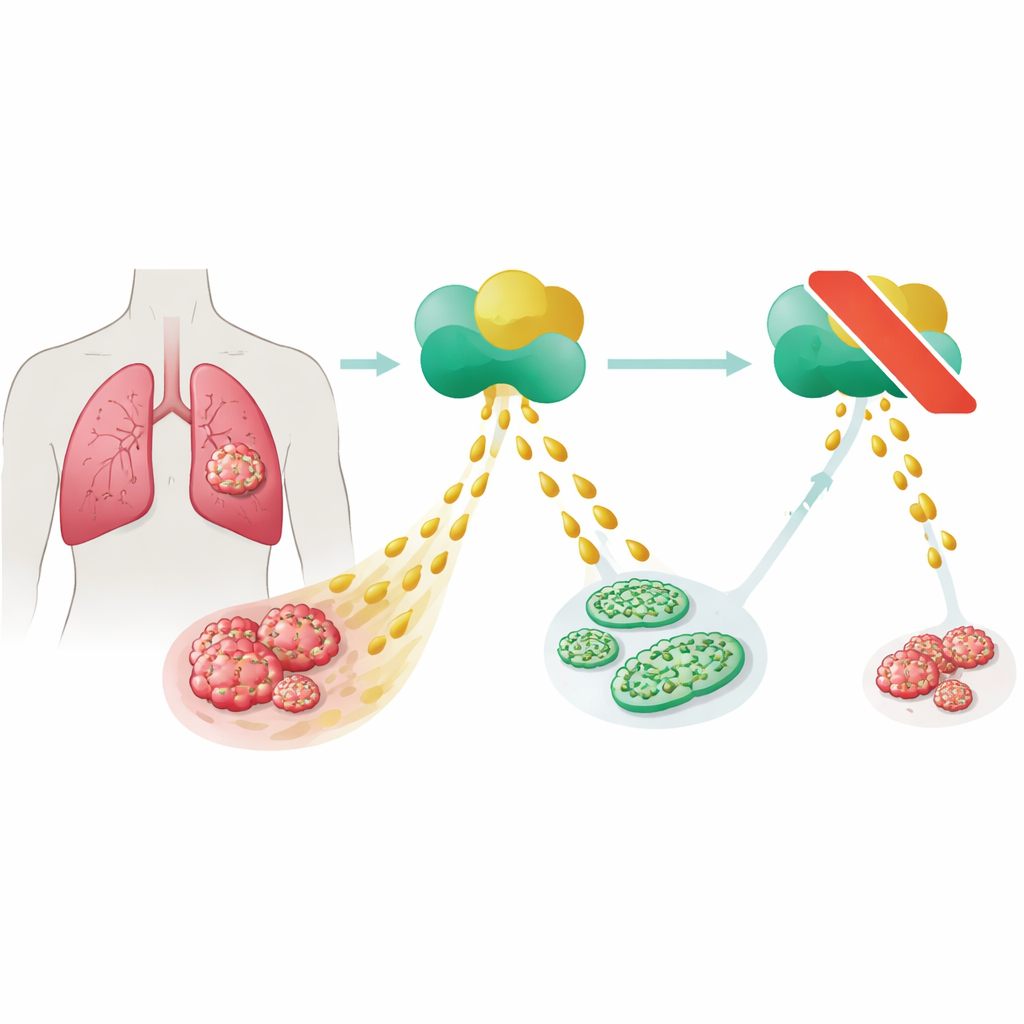
Relier une enzyme de fabrication des lipides aux tumeurs des patients
Pour vérifier si cette enzyme compte vraiment dans la maladie humaine, les chercheurs ont examiné des échantillons tissulaires de 45 personnes atteintes de mésothéliome pleural et les ont comparés à la plèvre normale. Ils ont trouvé la protéine synthase des acides gras dans chaque tumeur ayant perdu à la fois NF2 et p16, mais seulement dans environ un tiers des tumeurs où ces gènes étaient intacts, et pas du tout dans les tissus normaux. En consultant une grande base de données publique sur le cancer, les patients dont le mésothéliome exprimait des niveaux plus élevés du gène de la synthase des acides gras présentaient une survie globale plus courte que ceux avec des niveaux plus bas. Ensemble, ces résultats suggèrent que l’enzyme n’est pas un simple spectateur mais est étroitement liée à un comportement tumoral agressif dans ce type de cancer.
Tester un médicament ciblé chez l’animal
L’étape suivante a été de voir si le blocage de la synthase des acides gras pouvait réduire les tumeurs chez des organismes vivants. L’équipe a implanté des cellules humaines de mésothéliome déficientes en NF2/p16 sous la peau de souris immunodéficientes et les a traitées soit par cérulénine, soit par une solution saline inoffensive. La cérulénine a considérablement ralenti la croissance tumorale sans provoquer de perte de poids ni de dommages visibles au cœur, au foie ou aux reins. Les analyses sanguines de la fonction hépatique et rénale, des électrolytes, des lipides et du glucose sont également restées dans les plages normales. Ces résultats indiquent que, du moins dans ce contexte expérimental, la cérulénine peut freiner la croissance tumorale tout en semblant raisonnablement sûre.
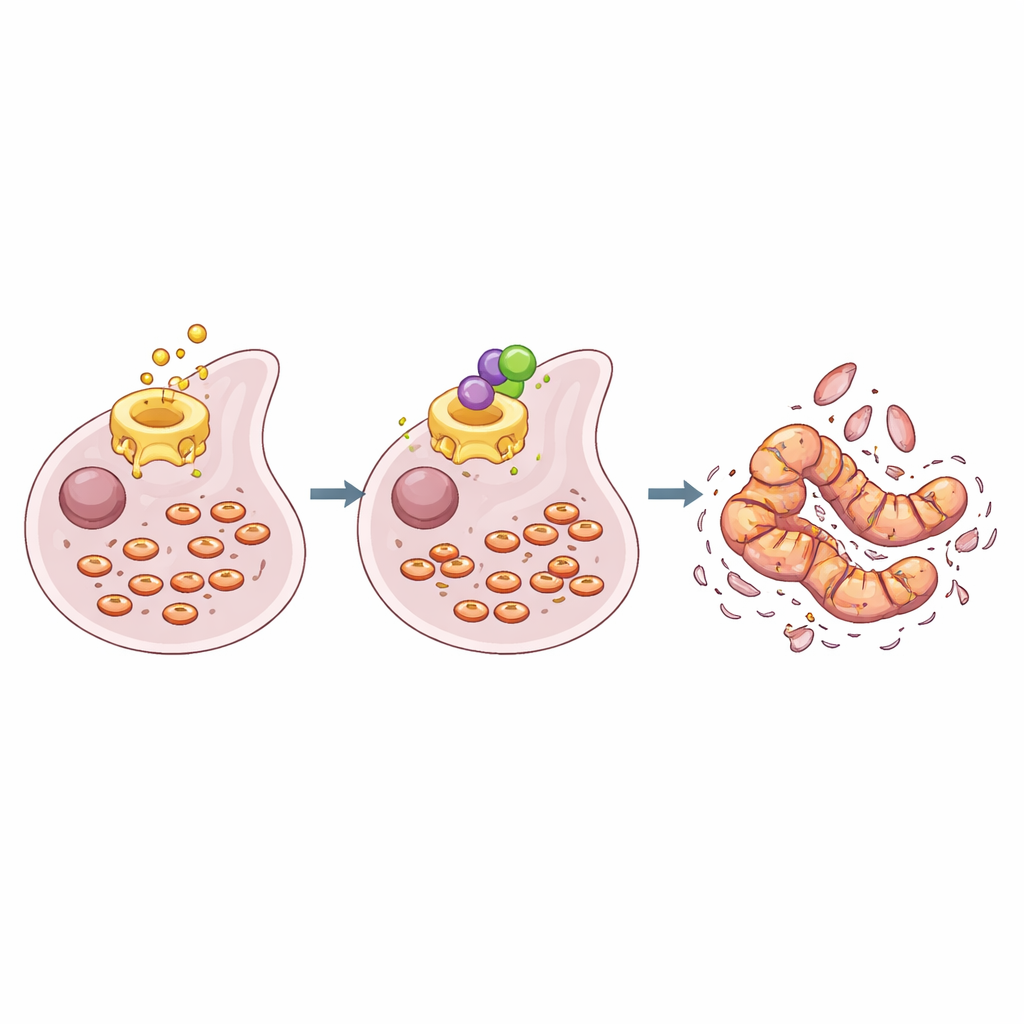
Comment le rebasage des petites centrales pousse les cellules cancéreuses vers la mort
Les cellules cancéreuses dépendent fortement de leurs mitochondries, ces petites structures qui génèrent la majeure partie de l’énergie cellulaire. Ces mitochondries se divisent et fusionnent constamment, et cet équilibre change en cas de maladie. Dans les cellules de mésothéliome déficientes en NF2/p16, l’activité de la synthase des acides gras favorisait un schéma de nombreuses mitochondries petites et fragmentées ainsi que des signaux actifs qui promeuvent la survie cellulaire. Lorsque les chercheurs ont ajouté la cérulénine, les mitochondries de ces cellules ont fusionné en longs réseaux tubulaires et l’activité de DRP1, une protéine qui conduit la fragmentation mitochondriale, a diminué. La signalisation via une voie de croissance majeure (PI3K–AKT–mTOR) et un système de contrôle de la croissance connu sous le nom de Hippo–YAP a également été atténuée. La cytométrie en flux et les analyses protéiques ont montré qu’un plus grand nombre de cellules traitées entraient en mort cellulaire programmée, marquée par une augmentation des niveaux de PARP clivé et de caspase-3.
Preuve génétique que la synthase des acides gras est une vulnérabilité
Pour confirmer que ces effets provenaient réellement du blocage de la synthase des acides gras et non d’une action hors cible de la cérulénine, l’équipe a utilisé l’édition génique CRISPR pour supprimer le gène de la synthase des acides gras lui-même dans des cellules mésothéliales déficientes en NF2/p16, créant des cellules « triple knockout ». Ces cellules modifiées croissaient plus lentement, présentaient des mitochondries plus fusionnées et allongées, et montraient des niveaux réduits de DRP1 mais des niveaux accrus de protéines favorisant la fusion mitochondriale. Elles produisaient aussi davantage d’espèces réactives de l’oxygène, signe de mitochondries stressées, et affichaient plus de marqueurs d’apoptose. Des expériences supplémentaires ont suggéré que, en l’absence de la synthase des acides gras, DRP1 devient davantage marquée par l’ubiquitine et est dégradée, inclinant encore l’équilibre vers la fusion mitochondriale et la mort cellulaire.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, l’étude montre que les cellules de mésothéliome dépourvues de NF2 et p16 dépendent de la synthase des acides gras pour maintenir leurs centrales énergétiques dans un état pro-croissance et soutenir des signaux de survie puissants. Bloquer cette enzyme avec la cérulénine affaiblit sélectivement ces tumeurs in vitro, dans des échantillons humains et chez la souris, tout en épargnant les tissus normaux à court terme. Pour les patients, ce travail suggère que des médicaments ciblant la synthase des acides gras, en particulier dans les tumeurs testées pour la perte de NF2 et CDKN2A, pourraient devenir partie d’une stratégie de médecine de précision exploitant une dépendance métabolique spécifique de leur cancer.
Citation: Karnan, S., Ota, A., Hasan, M.N. et al. Targeting fatty acid synthase suppresses tumor development in NF2/CDKN2A-deficient pleural mesothelioma. Cell Death Dis 17, 287 (2026). https://doi.org/10.1038/s41419-026-08481-y
Mots-clés: mésothéliome pleural, synthase des acides gras, cérulénine, dynamique mitochondriale, oncologie de précision