Clear Sky Science · fr
Ubiquitination de mH2A1 médiée par UBE3A active la transcription de TERT pour promouvoir la résistance à la sénescence dans le cancer du pancréas
Pourquoi cette recherche est importante pour les patients
Le cancer du pancréas figure parmi les cancers les plus mortels, en partie parce que les cellules tumorales sont particulièrement habiles à contourner les freins naturels liés au vieillissement. Cette étude met au jour un « circuit de sabotage » moléculaire caché qui aide les cellules du pancréas à rester jeunes, à continuer de se diviser et à résister aux traitements. En comprenant ce circuit, les chercheurs proposent une nouvelle manière d’induire la sénescence dans ces cellules puis de les éliminer sélectivement, ouvrant la voie à des thérapies combinées plus intelligentes.
La sénescence, frein tumoral naturel de l’organisme
Toutes les cellules portent une horloge interne qui finit par les empêcher de se diviser, un processus connu sous le nom de sénescence. Dans les lésions pancréatiques précoces, cette horloge peut ralentir le développement tumoral en mettant les cellules précancéreuses en retraite permanente. De nombreux traitements anticancéreux fonctionnent aussi en partie en forçant les cellules tumorales à entrer dans cet état de vieillissement. Toutefois, si ces cellules sénescentes ne sont pas éliminées, elles peuvent alimenter l’inflammation et favoriser la rechute. Cela a conduit à une nouvelle idée thérapeutique : d’abord pousser les cellules cancéreuses en sénescence, puis éliminer ces cellules âgées avec des médicaments « sénolytiques » spécifiquement toxiques pour elles.
Une enzyme favorisant le cancer dans la lumière
Pour identifier les gènes qui aident les cellules du pancréas à défier la sénescence, l’équipe a exploité de larges jeux de données de patients puis validé ses observations sur des échantillons tumoraux et des lignées cellulaires. Les chercheurs se sont concentrés sur une protéine appelée UBE3A, une enzyme qui étiquette d’autres protéines en vue de leur destruction. Les taux d’UBE3A étaient bien plus élevés dans les tumeurs pancréatiques que dans les tissus sains adjacents, et les patients présentant des niveaux plus élevés d’UBE3A avaient tendance à avoir des cancers plus volumineux, plus avancés et un pronostic moins bon. En culture, l’augmentation d’UBE3A accélérava la croissance, réduisait les marqueurs classiques du vieillissement cellulaire et diminuait les sécrétions inflammatoires typiques des cellules sénescentes. L’inhibition d’UBE3A produisait l’effet inverse et, dans des modèles murins, réduisait fortement la croissance tumorale et les métastases hépatiques. 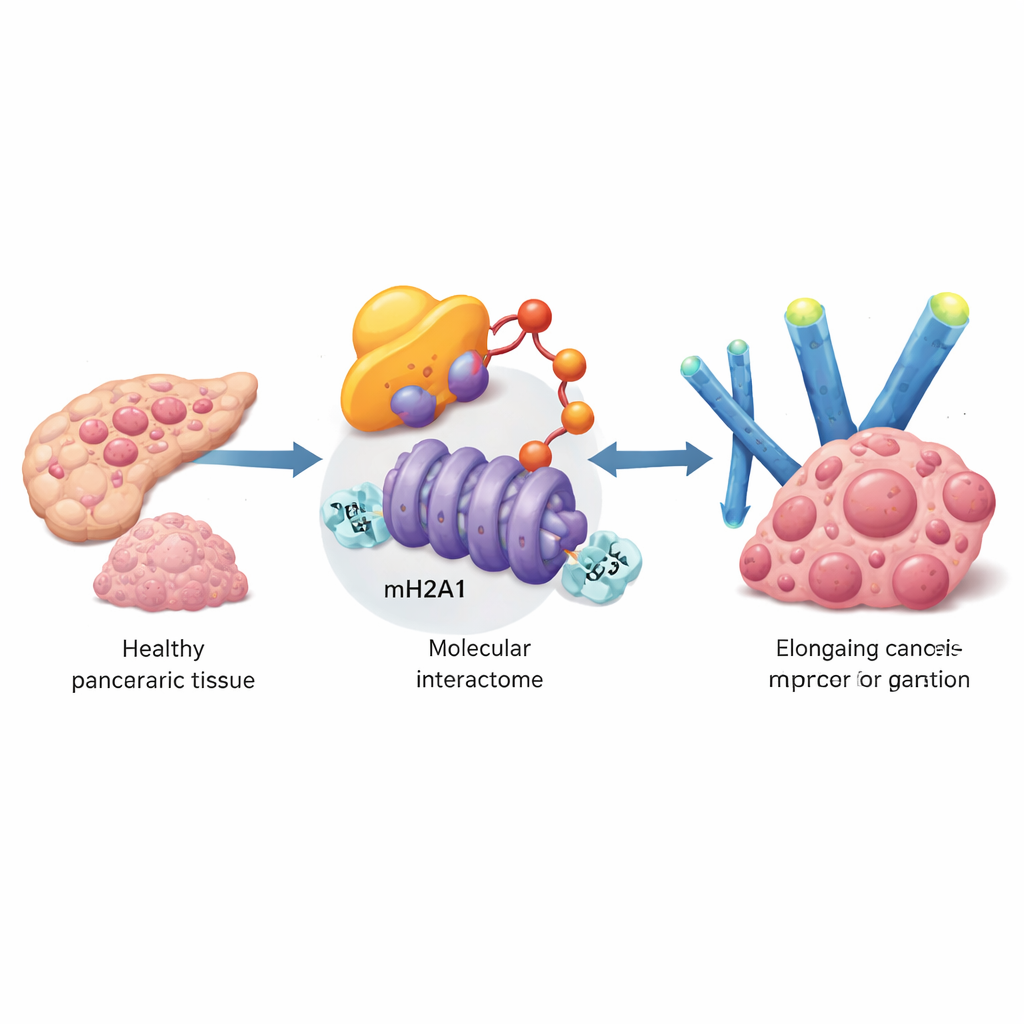
Comment les cellules cancéreuses effacent un frein chromatinien
En approfondissant, les chercheurs ont cherché quelles molécules sont ciblées par UBE3A. Grâce à des criblages par spectrométrie de masse avancée, ils ont découvert qu’UBE3A se lie à une variante particulière d’histone appelée macroH2A1 (mH2A1) et la marque chimiquement. mH2A1 aide à compacter l’ADN et agit généralement comme un frein sur l’activité génique. UBE3A attache une chaîne d’étiquettes « détruisez-moi » à mH2A1 en un site spécifique, provoquant sa dégradation par le système d’élimination des protéines de la cellule. Dans les tumeurs pancréatiques, les niveaux de mH2A1 étaient plus faibles là où UBE3A était élevé, et la restauration de mH2A1 contrait la capacité d’UBE3A à bloquer la sénescence et à stimuler la croissance tumorale. Cela révèle une étape clé : les cellules cancéreuses du pancréas suppriment une marque chromatinienne protectrice en utilisant UBE3A pour éliminer mH2A1.
Dégager la télomérase pour maintenir la jeunesse cellulaire
La question suivante était : quels gènes sont libérés lorsque mH2A1 est éliminée ? En combinant le séquençage de l’ARN et les cartes de liaison de l’ADN, l’équipe a identifié le gène de la télomérase TERT comme cible centrale. La télomérase maintient les capuchons protecteurs aux extrémités des chromosomes, permettant aux cellules de continuer à se diviser au lieu d’entrer en sénescence. L’étude montre que mH2A1 se trouve normalement à un élément amplificateur (enhancer) à l’intérieur du gène TERT, où elle recrute une autre enzyme, EZH2, pour déposer une marque chimique répressive sur les histones voisins. Cette combinaison maintient TERT réprimé et laisse les télomères se raccourcir. Quand UBE3A détruit mH2A1, le complexe répressif se dissout, l’enhancer devient actif, TERT s’active, les télomères sont maintenus et les cellules cancéreuses du pancréas gagnent en résistance au vieillissement. Des formes mutantes d’UBE3A incapables d’étiqueter des protéines, ou une mH2A1 mutée qui ne peut pas être marquée, interrompent ce circuit et restaurent le frein de la sénescence.
Associer induction de la sénescence et nettoyage sénolytique
Enfin, les chercheurs ont testé si cette voie pouvait être exploitée thérapeutiquement. L’arrêt d’UBE3A poussa les cellules du cancer pancréatique vers la sénescence et augmenta leur dépendance aux protéines anti‑mort de la famille BCL‑2 — une vulnérabilité connue des cellules sénescentes. L’équipe combina alors l’inhibition d’UBE3A avec ABT‑263, un médicament sénolytique ciblant ces protéines de survie. En culture cellulaire, la combinaison a entraîné beaucoup plus de cellules cancéreuses en mort cellulaire programmée que chaque traitement pris séparément. Dans les modèles murins, les tumeurs avec UBE3A réduit ont encore davantage diminué lorsque les animaux ont reçu ABT‑263, et les marqueurs de prolifération à l’intérieur des tumeurs ont fortement chuté. 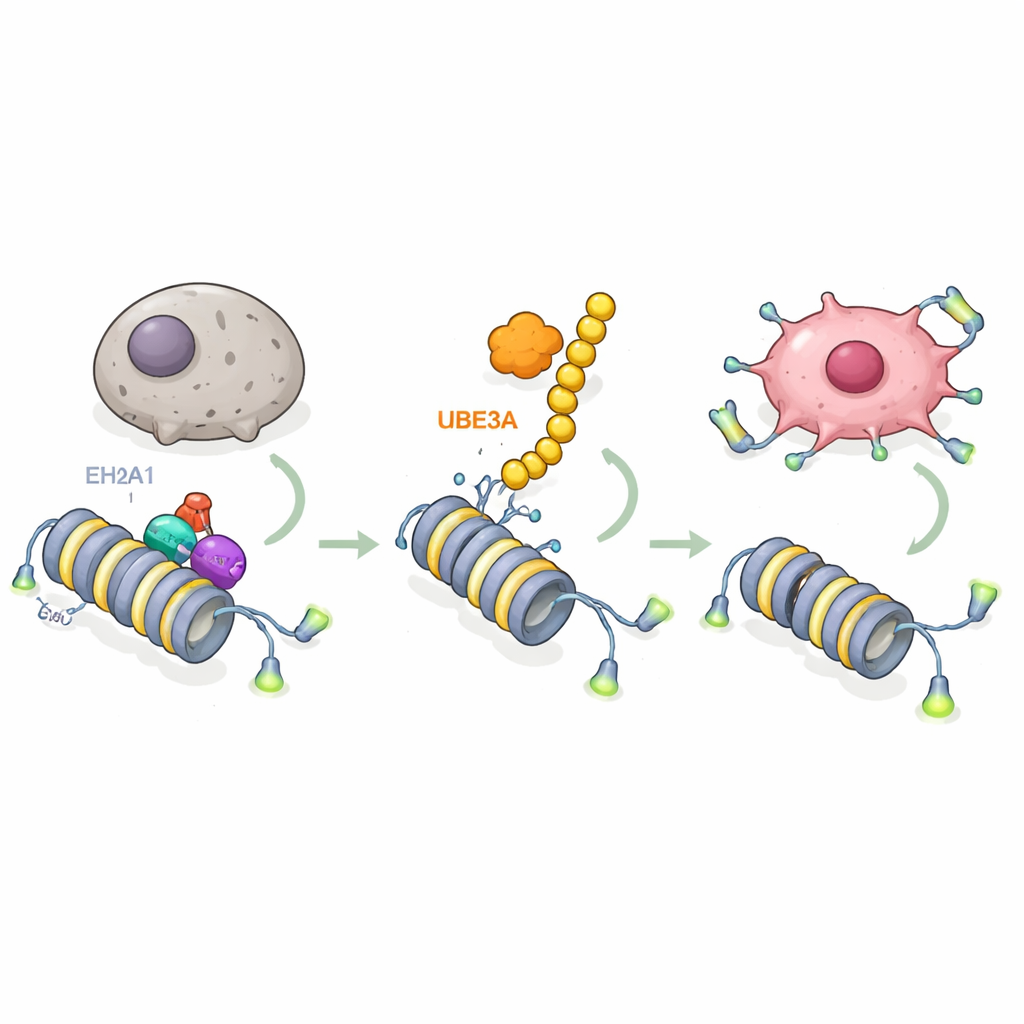
Ce que cela signifie pour les traitements futurs
Ce travail révèle une chaîne d’événements détaillée par laquelle les cellules du cancer pancréatique évitent de vieillir : UBE3A détruit le frein chromatinien mH2A1, ce qui lève la répression du gène de la télomérase TERT et contribue au maintien des télomères, permettant aux cellules de continuer à se diviser. En ciblant UBE3A, les cliniciens pourraient réengager le programme naturel de vieillissement cellulaire puis utiliser des médicaments sénolytiques comme ABT‑263 pour éliminer sélectivement ces cellules cancéreuses vulnérables et vieillies. Bien que des études supplémentaires soient nécessaires pour traduire ce mécanisme en thérapies pour les patients, l’axe UBE3A–mH2A1–TERT offre un levier prometteur contre l’un des cancers les plus résistants aux traitements.
Citation: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Mots-clés: cancer du pancréas, sénescence cellulaire, <keyword>ligase ubiquitine, thérapie sénolytique