Clear Sky Science · fr
Un petit inhibiteur moléculaire de la protéine GTPase ARF1 limite la croissance et les métastases des cellules du foie et du côlon
Pourquoi cette recherche est importante
Les cancers du foie et du côlon figurent parmi les tumeurs les plus mortelles, et les traitements actuels réduisent souvent les tumeurs au prix d’effets secondaires sévères. Cette étude explore une nouvelle catégorie de médicament qui n’empoisonne pas simplement les cellules à prolifération rapide, mais qui pénètre dans les cellules cancéreuses pour désassembler un « centre de contrôle » protéique dont elles dépendent pour croître et se disséminer. En ciblant ce centre, le composé expérimental vise à ralentir la croissance tumorale tout en épargnant les tissus sains.
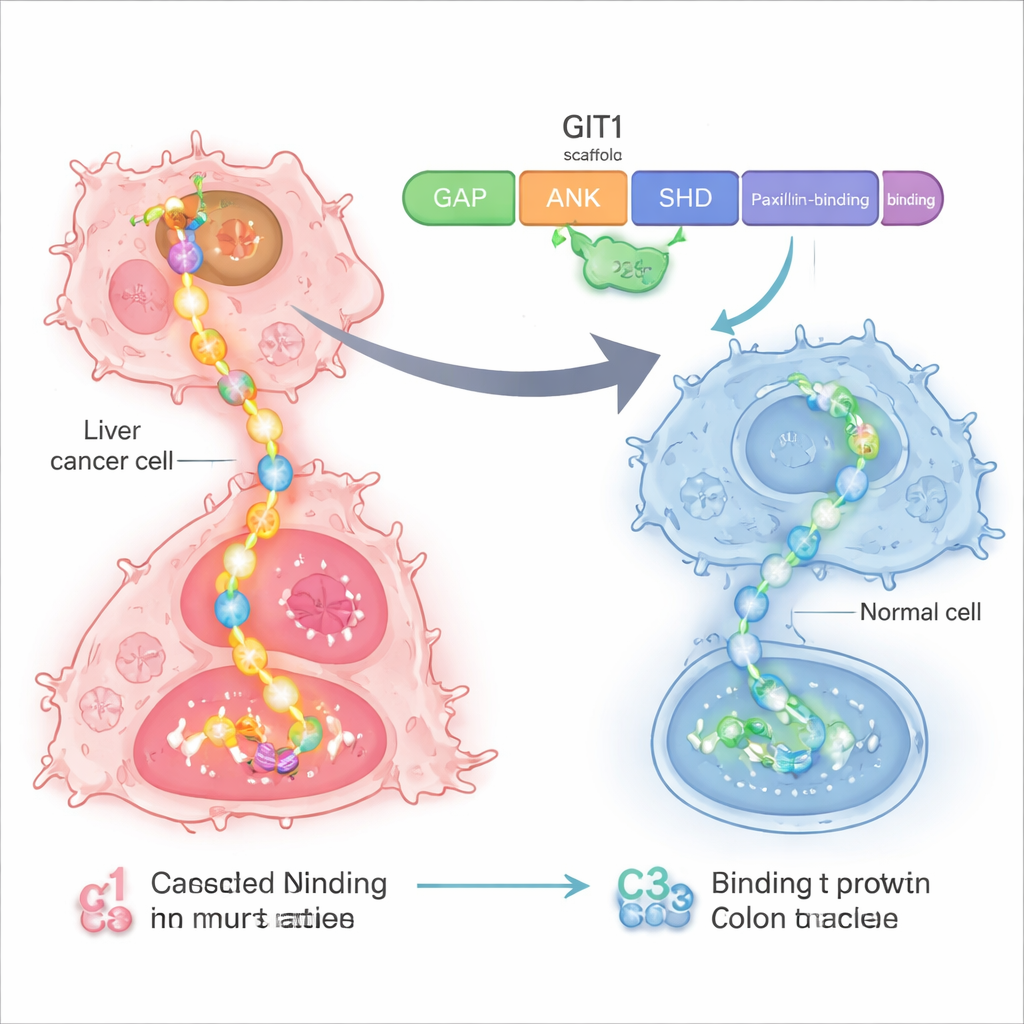
Un point de contrôle vulnérable à l’intérieur des cellules cancéreuses
Les chercheurs se sont intéressés à une protéine appelée GIT1, qui joue le rôle d’échafaudage ou de multiprise au sein des cellules. Dans les cancers du foie et du côlon, GIT1 et sa protéine partenaire MAT2B sont surproduites. Ensemble, elles assemblent plusieurs éléments d’une voie de croissance majeure connue sous le nom RAS–RAF–MEK–ERK, une chaîne de signaux qui incite les cellules à se diviser et à migrer. Des travaux antérieurs ont montré que lorsque GIT1 et MAT2B sont abondants, les tumeurs hépatiques et colorectales croissent plus vite et se propagent plus aisément, et que la diminution de ces protéines ralentit la progression tumorale. Cela a rendu le complexe GIT1–MAT2B attractif comme cible pour une thérapie plus précise.
Concevoir une petite molécule sans plan
Un défi majeur était l’absence de structure cristalline tridimensionnelle de GIT1, si bien que l’équipe ne pouvait pas « consulter » directement la forme de la protéine. Ils ont donc utilisé la modélisation informatique pour prédire la structure d’une région de GIT1 composée de répétitions ankyrines, située près des sites d’attachement de MAT2B et d’autres protéines de signalisation. Ils ont ensuite effectué un criblage virtuel d’une vaste bibliothèque de petites molécules contre ce modèle pour voir lesquelles pourraient se lier à cette zone. Parmi neuf candidats testés en culture cellulaire, une molécule — appelée composé 3 (C3) — s’est distinguée. C3 se liait spécifiquement à GIT1, mais pas à sa proche homologue GIT2, et réduisait l’activité du signal de croissance ERK dans plusieurs lignées cellulaires cancéreuses.
Empêcher les cellules cancéreuses de se diviser et de se disséminer
Lorsque des cellules de cancer du foie et du côlon ont été traitées par C3, leur croissance a ralenti et, à des doses plus élevées, de nombreuses cellules sont mortes, tandis que les cellules hépatiques et rénales non cancéreuses sont restées en grande partie épargnées. C3 a provoqué un blocage des cellules au niveau de la transition entre les phases G2 et M du cycle cellulaire, le point de contrôle juste avant et pendant la mitose où une cellule se divise en deux. Le composé a aussi fortement réduit la capacité des cellules cancéreuses à former des colonies et à migrer sur une surface — deux mesures in vitro liées à la repousse tumorale et aux métastases. Au niveau moléculaire, C3 a affaibli les interactions entre GIT1, MAT2B et les protéines de la cascade RAF–MEK–ERK, entraînant une baisse de l’activité de MEK et ERK et une diminution du régulateur du cycle cellulaire cycline D1.
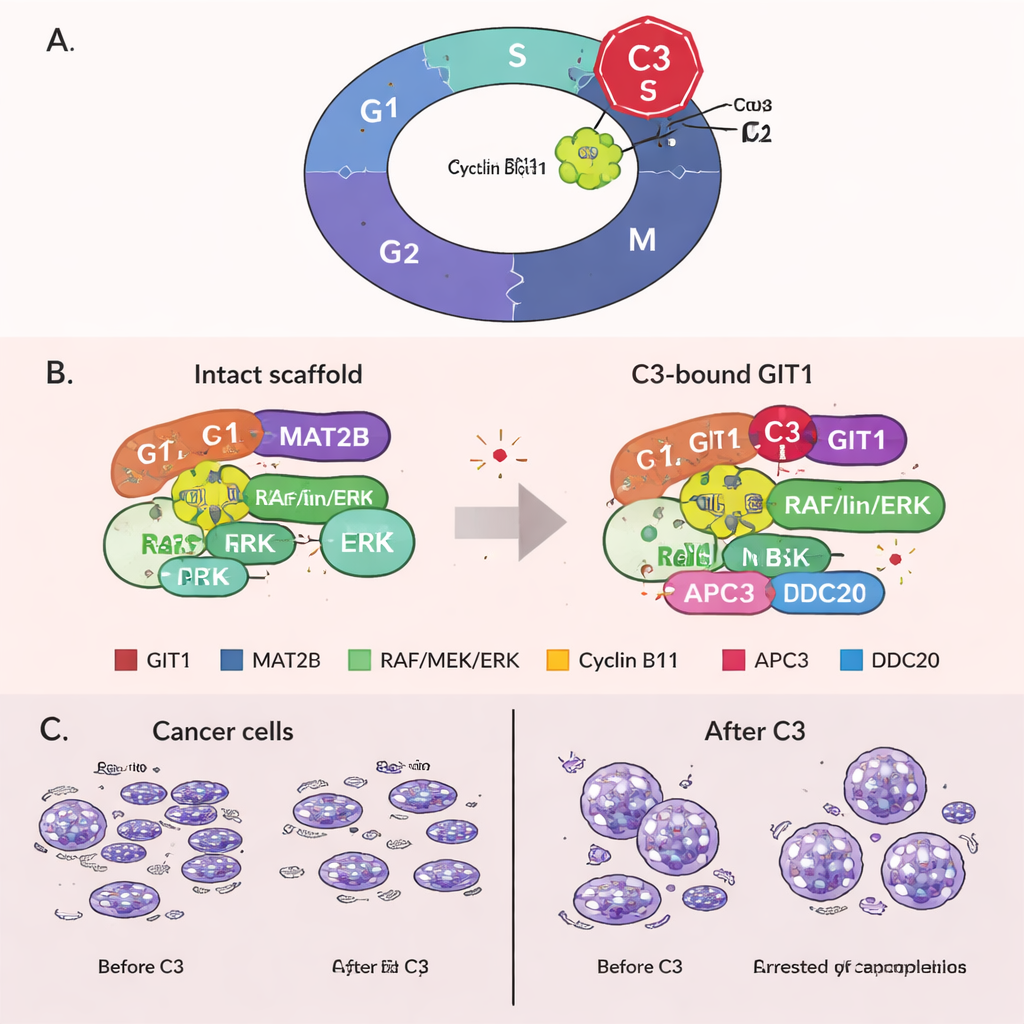
Verrouiller les cellules en mitose grâce à un rôle inédit de GIT1
De manière inattendue, l’équipe a mis au jour un rôle nouveau de GIT1 dans les étapes finales de la division cellulaire. Ils ont découvert que GIT1 se lie à la cycline B1, une protéine qui favorise l’entrée en mitose, ainsi qu’à des composants d’un complexe protéique appelé complexe promoteur de l’anaphase (APC/C), qui marque normalement la cycline B1 pour sa dégradation afin que les cellules puissent sortir de la mitose. Le traitement par C3 a renforcé le lien entre GIT1 et la cycline B1 mais affaibli les connexions entre GIT1, la cycline B1 et les composants de l’APC/C. En conséquence, la cycline B1 n’était plus efficacement dégradée, ses niveaux restaient élevés et les cellules restaient bloquées en mitose. Cet arrêt prolongé est connu pour déclencher la mort cellulaire, offrant un second mécanisme par lequel C3 peut éliminer les cellules cancéreuses. De façon importante, lorsque GIT1 était réduit expérimentalement, C3 perdait une grande partie de sa capacité à augmenter la cycline B1, à bloquer le cycle cellulaire et à inhiber la croissance, montrant que ses effets dépendent réellement de GIT1.
Résultats prometteurs dans des modèles animaux
Les chercheurs sont ensuite passés à des modèles murins pour évaluer si C3 pouvait être efficace in vivo. Chez des souris immunocompétentes porteuses de tumeurs colorectal implantées, des injections directes de C3 dans les tumeurs ont fortement ralenti leur croissance sans toxicité évidente pour les organes majeurs. Dans deux modèles supplémentaires — des cellules de cancer du côlon humain implantées dans le foie de souris immunodéficientes, et des cellules de cancer du côlon de souris ayant métastasé au foie chez des souris immunocompétentes — l’administration intrapéritonéale de C3 a réduit la charge tumorale et les signes de dissémination. Les analyses sanguines et histologiques suggèrent que les traitements étaient bien tolérés, et des études pharmacocinétiques ont montré que les niveaux de médicament dans le sang restaient suffisamment élevés pendant plusieurs heures après l’administration.
Ce que cela pourrait signifier pour les traitements du cancer à venir
Pour un non-spécialiste, le message essentiel est que les chercheurs ont trouvé une façon d’attaquer le cancer non pas en ciblant une enzyme mutée unique, mais en perturbant un assemblage multi-protéique dont les cellules cancéreuses dépendent à la fois pour les signaux de croissance et pour une division cellulaire correcte. Leur petite molécule, C3, se lie spécifiquement à GIT1, reconfigure son réseau de partenaires, diminue une voie de croissance majeure et piège les cellules cancéreuses dans un embouteillage fatal lors de la mitose. Bien que C3 reste pour l’instant un outil expérimental et non un médicament destiné aux patients, ce travail montre que cibler des protéines échafaudage comme GIT1 pourrait ouvrir une nouvelle voie pour traiter les cancers du foie et du côlon avec plus de précision et potentiellement moins d’effets secondaires.
Citation: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Mots-clés: cancer du foie, cancer du côlon, thérapie ciblée, arrêt du cycle cellulaire, protéine échafaudage