Clear Sky Science · fr
RIPK1 régule le destin des cellules β via des actions sur l’expression génique et la signalisation kinase dans un modèle murin d’auto-réactivité des cellules β
Pourquoi il est important de sauver les cellules productrices d’insuline
Le diabète de type 1 se développe lorsque le système immunitaire de l’organisme détruit les cellules bêta productrices d’insuline dans le pancréas. Une fois ces cellules perdues, les personnes doivent dépendre d’injections d’insuline à vie. Cette étude examine un « interrupteur » interne clé au sein des cellules bêta, appelé RIPK1, qui contribue à décider si ces cellules survivent ou meurent lors des attaques immunitaires. Comprendre et contrôler cet interrupteur pourrait ouvrir de nouvelles voies pour protéger les cellules bêta restantes et éventuellement retarder ou atténuer l’évolution du diabète de type 1.
Un interrupteur de stress à l’intérieur des cellules bêta
Les cellules bêta vivent dans un environnement hostile lorsque le diabète de type 1 se développe. Les cellules immunitaires libèrent des signaux inflammatoires — tels que le TNFα et l’IFNγ — qui poussent les cellules bêta vers le stress et la mort. La protéine RIPK1 agit comme un décideur central dans de nombreux types cellulaires, intégrant ces signaux et orientant les cellules soit vers la survie, soit vers différentes formes de mort programmée. Dans ce travail, les chercheurs ont cherché à savoir si RIPK1 joue le même rôle dans les cellules bêta attaquées par le système immunitaire, et si réduire l’activité de RIPK1 pourrait aider ces cellules à rester en vie.
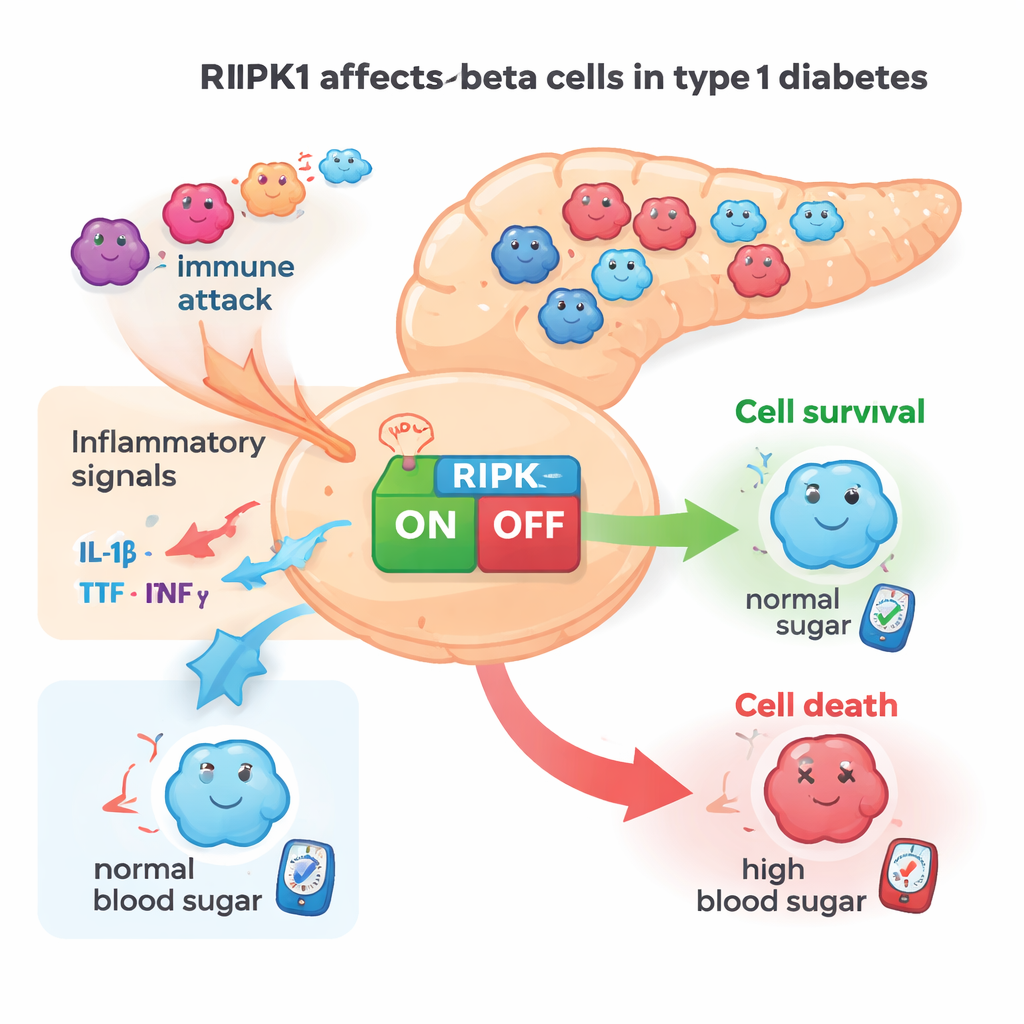
Les niveaux de RIPK1 augmentent dans les cellules prédisposées au diabète
L’équipe a d’abord cherché des signes d’une implication de RIPK1 dans le diabète de type 1. Ils ont constaté que les signaux inflammatoires augmentaient l’activité de RIPK1 dans des lignées de cellules bêta de souris et dans des cellules bêta humaines cultivées en laboratoire. Dans les tissus pancréatiques de souris et d’humains, RIPK1 était clairement présent dans les cellules productrices d’insuline. Fait important, les îlots de souris NOD prédisposées au diabète montraient une activité accrue du gène Ripk1 à mesure que les animaux vieillissaient et que l’auto-immunité augmentait. Les données transcriptomiques unicellulaires de donneurs humains montraient un schéma similaire : les cellules bêta de personnes atteintes de diabète de type 1 contenaient davantage d’ARN de RIPK1 que celles de donneurs non diabétiques. Ensemble, ces observations désignent RIPK1 comme une protéine liée au stress qui s’active précisément quand les cellules bêta subissent une pression auto-immune.
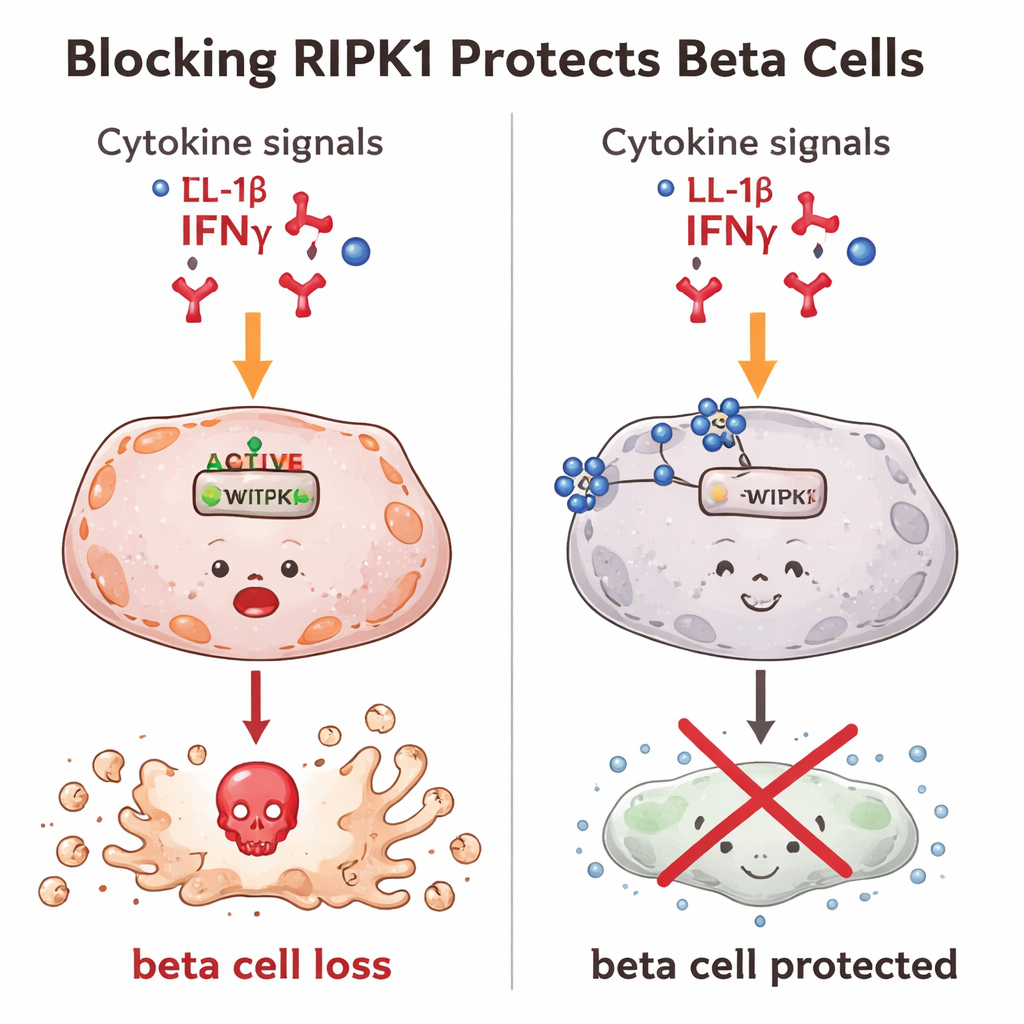
Bloquer RIPK1 aide les cellules bêta à survivre
Puis, les chercheurs ont testé ce qui se passe lorsque RIPK1 est bloqué. Dans des cellules bêta murines exposées à des signaux inflammatoires, RIPK1 s’active normalement et la mort cellulaire augmente. Lorsque les scientifiques ont utilisé de petits composés pharmacologiques pour inhiber l’activité de RIPK1 ou réduire sa quantité à l’intérieur de la cellule, beaucoup moins de cellules bêta sont mortes. Ils ont ensuite utilisé des outils d’édition génétique pour affaiblir le gène Ripk1 lui-même, créant des cellules bêta avec des niveaux de RIPK1 beaucoup plus bas. Ces cellules modifiées étaient remarquablement résistantes à la fois aux formes classiques de mort cellulaire « programmée » et à une forme plus explosive et inflammatoire de mort. En d’autres termes, réduire RIPK1 a permis à davantage de cellules bêta de survivre, même face à des signaux fortement dommageables.
Profonds changements dans les programmes cellulaires et la signalisation
Protéger les cellules bêta n’était pas seulement une question d’interrompre une voie de mort. À l’aide d’un séquençage à grande échelle de l’ARN, l’équipe a découvert que la suppression de RIPK1 remodelait de nombreux programmes géniques au sein des cellules bêta. Les gènes liés à l’inflammation et aux réponses immunitaires innées étaient atténués, tandis que plusieurs gènes associés à l’identité des cellules bêta et à la production d’insuline étaient augmentés. Parallèlement, un large inventaire des enzymes actives a montré que la perte de RIPK1 réorganisait plusieurs voies de signalisation, y compris les systèmes MAPK et JAK qui transmettent des messages de stress et immunitaires. Ces changements suggèrent que RIPK1 influence non seulement la survie des cellules bêta, mais aussi leur degré d’« inflammation », leur visibilité pour le système immunitaire et leur fonctionnalité durant une attaque auto-immune.
Résister à l’attaque immunitaire in vivo
Pour déterminer si ces résultats ont un impact dans un contexte plus réaliste, les chercheurs ont mélangé des cellules immunitaires responsables du diabète provenant de souris NOD avec des cellules bêta normales ou déficientes en RIPK1. Les deux types de cellules bêta pouvaient encore activer les cellules immunitaires, mais les cellules déficientes en RIPK1 étaient tuées à seulement environ la moitié du taux des cellules normales. Dans un modèle murin, l’équipe a implanté à la fois des cellules bêta normales et déficientes en RIPK1 dans les mêmes animaux puis a déclenché une attaque auto-immune. Au fil du temps, les greffons de cellules bêta ordinaires ont presque disparu, tandis que les greffons déficients en RIPK1 restaient des dizaines à plus d’une centaine de fois plus lumineux en imagerie bioluminescente, indiquant que beaucoup plus de cellules avaient survécu à l’assaut immunitaire.
Ce que cela pourrait signifier pour les personnes atteintes de diabète de type 1
Ce travail montre que RIPK1 agit comme un interrupteur central de stress qui contribue à décider si les cellules productrices d’insuline vivent ou meurent lors d’attaques auto-immunes. Lorsque RIPK1 est atténué, les cellules bêta ont moins de chances de mourir, moins de chances d’émettre des signaux inflammatoires et davantage de chances de conserver leur identité et leur fonction. Des médicaments ciblant en toute sécurité RIPK1 sont déjà explorés pour d’autres maladies, de sorte qu’adapter des stratégies similaires pour protéger les cellules bêta pourrait offrir une nouvelle approche pour prévenir ou ralentir le diabète de type 1, notamment tôt dans la maladie lorsque certaines cellules bêta sont encore vivantes.
Citation: Contreras, C.J., Mukherjee, N., Harris-Kawano, A. et al. RIPK1 regulates β-cell fate via actions on gene expression and kinase signaling in a mouse model of β-cell self-reactivity. Cell Death Dis 17, 220 (2026). https://doi.org/10.1038/s41419-026-08471-0
Mots-clés: diabète de type 1, cellules bêta, RIPK1, auto-immunité, mort cellulaire