Clear Sky Science · fr
L’inhibition du récepteur du facteur de stimulation des colonies 1 préserve les photorécepteurs lors d’un décollement de la rétine
Pourquoi cette recherche compte pour la vue
Le décollement de la rétine est une urgence qui peut mener à une perte de vision même après une chirurgie réussie. Une grande partie de ce dommage persistant provient des propres cellules immunitaires chargées du nettoyage, qui peuvent endommager les cellules sensibles à la lumière en voulant aider. Cette étude chez la souris examine si l’atténuation d’un commutateur immunitaire clé, appelé CSF1R, peut protéger ces photorécepteurs fragiles et ouvrir une nouvelle voie pour préserver la vision.
Le service de nettoyage de l’œil et ses effets indésirables
Lorsque la rétine se détache de son épaisseur de soutien, les photorécepteurs perdent soudainement l’accès à l’oxygène et aux nutriments. Beaucoup de ces cellules meurent et le tissu émet des signaux de détresse. Les cellules immunitaires locales de la rétine, connues sous le nom de microglies, changent de forme, migrent vers la lésion et augmentent leur activité phagocytaire. En parallèle, des cellules immunitaires provenant du sang, y compris différents types de monocytes, affluent dans la rétine. Ensemble, elles tentent d’éliminer les débris et de lancer la réparation. Mais cette réaction bénéfique peut aussi dépasser son objectif, entraînant une inflammation supplémentaire qui tue des photorécepteurs encore viables et aggrave la perte de vision.
Un médicament qui cible un commutateur immunitaire partagé
Tant les microglies résidentes que les monocytes entrants dépendent du même récepteur de surface, le CSF1R, pour leur survie et leur fonction. Les chercheurs ont utilisé le PLX5622, un composé administré par voie orale qui bloque le CSF1R, pour étudier comment l’interférence avec ce commutateur modifie le comportement immunitaire dans le décollement de la rétine. Ils ont d’abord cartographié ses effets dans le sang et la rétine. Dans la circulation, un traitement bref n’a pas modifié le nombre total de monocytes mais a rééquilibré leurs sous‑types : les monocytes « classiques » pro‑inflammatoires ont augmenté, tandis que les monocytes « non‑classiques » de surveillance ont diminué. Dans l’œil, le PLX5622 a efficacement épuisé les microglies rétiniennes et modifié le nombre de cellules immunitaires d’origine sanguine entrant dans la rétine lésée ainsi que leurs formes et comportements.
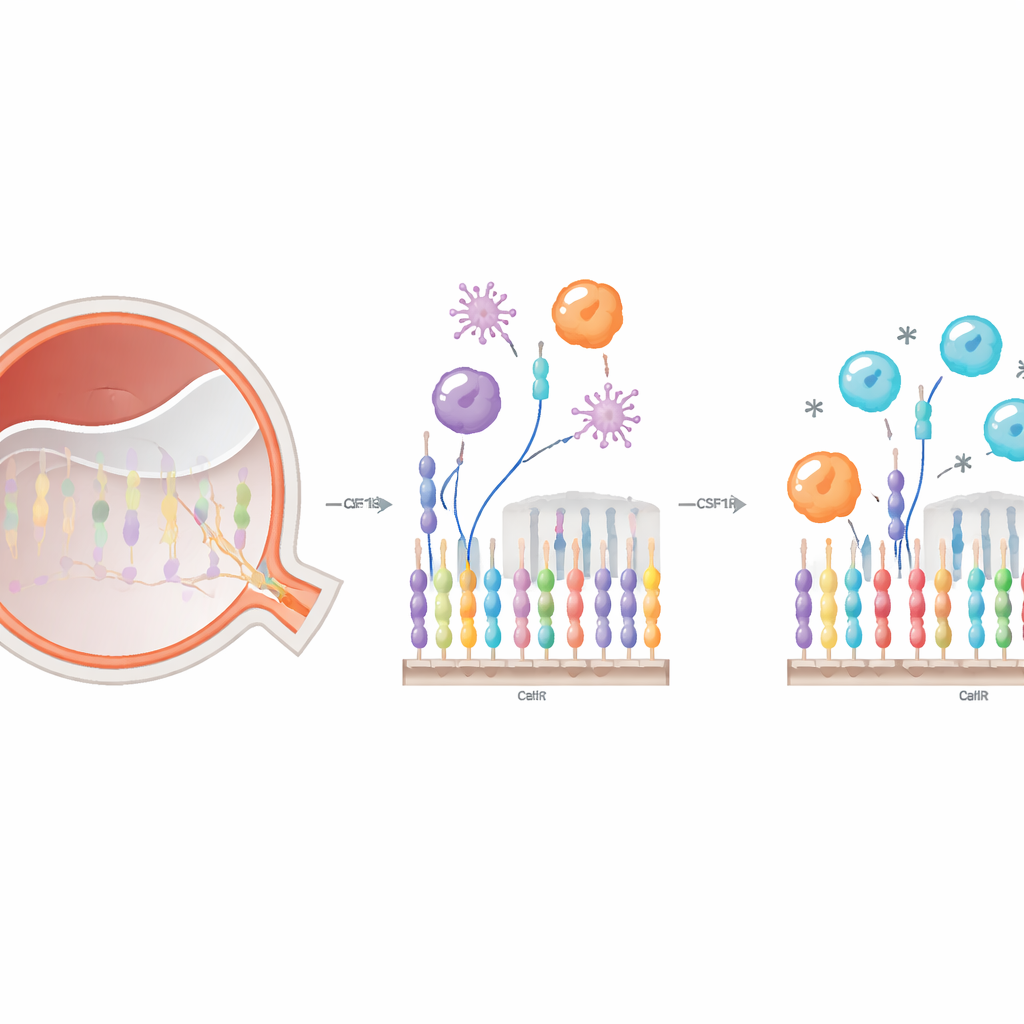
Suivre les cellules locales et entrantes grâce à des marqueurs colorés
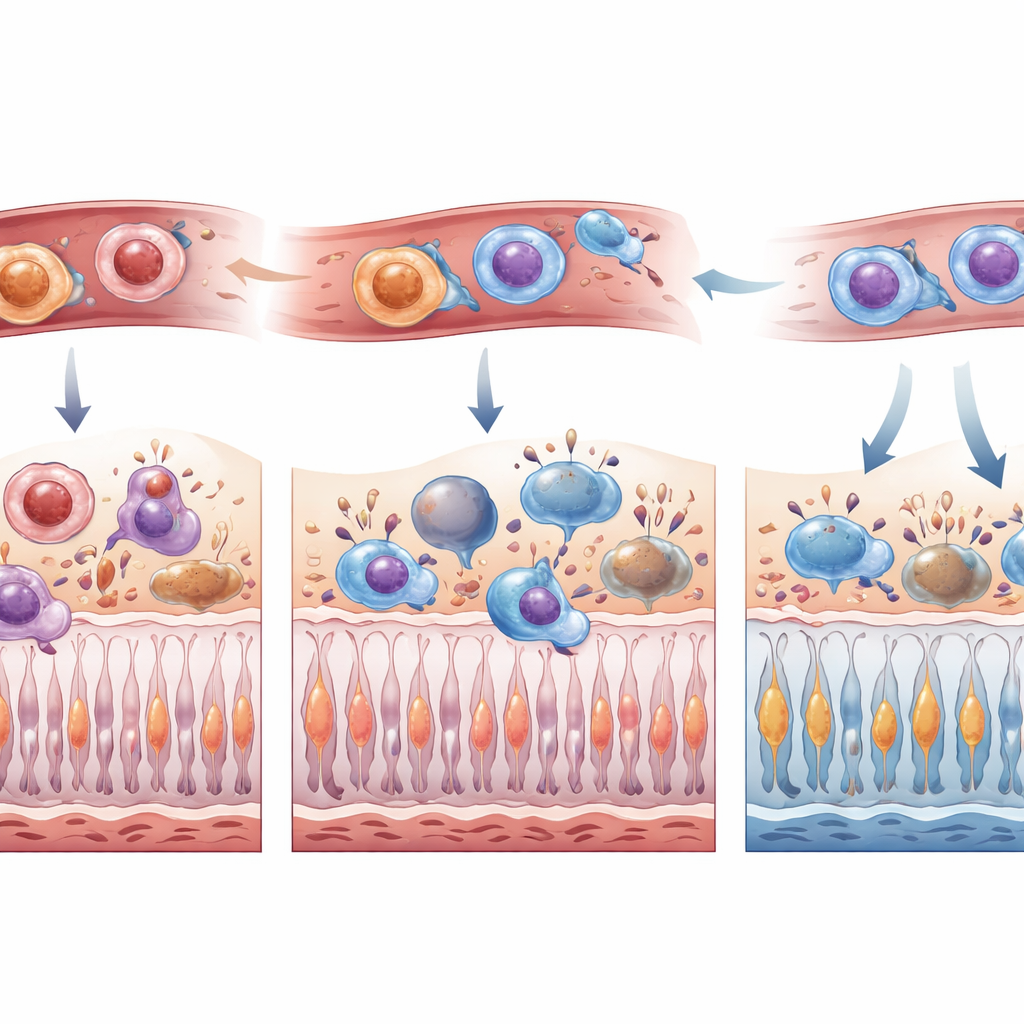
Parce que les microglies et les monocytes infiltrants peuvent paraître très similaires une fois dans la rétine, l’équipe a créé un système de souris à double marquage : les microglies résidentes brillaient d’une couleur et les cellules dérivées de la moelle osseuse d’une autre. Après induction d’un décollement rétinien contrôlé, ils ont suivi les déplacements et les transformations de ces cellules pendant la première semaine. Sans traitement, les microglies s’accumulaient principalement dans les couches supérieures de la rétine, tandis que les cellules d’origine médullaire inondaient surtout l’espace sous-rétinien, adoptant souvent une forme amoeboïde très phagocytaire. Avec l’inhibition du CSF1R, les microglies étaient nettement réduites dans les couches dès les premières phases, et moins de cellules dérivées de la moelle, en particulier le type amoeboïde, atteignaient la rétine dans les jours qui ont suivi la lésion. Au septième jour, la vague de cellules entrantes avait en grande partie rattrapé son retard, ce qui suggère que le blocage du CSF1R retarde plutôt qu’il n’empêche définitivement leur arrivée.
Comment le changement d’équilibre immunitaire protège les cellules sensibles à la lumière
Pour comprendre ce que signifiaient ces modifications immunitaires pour la vision, les chercheurs ont compté les photorécepteurs mourants et survivants à plusieurs moments. Dans les premières heures après le décollement, les animaux traités par PLX5622 présentaient moins de photorécepteurs en voie d’apoptose et davantage de cellules survivantes. À une semaine, à la fois une courte pré‑préparation et un traitement continu ont préservé l’épaisseur de la couche de photorécepteurs — un indicateur structurel de survie cellulaire — et réduit la présence de cellules immunitaires dans l’espace sous‑rétinien. Un profilage immunitaire détaillé a montré que, malgré une baisse globale du nombre de leucocytes infiltrants, ceux qui entraient sous l’inhibition du CSF1R affichaient plutôt un profil plus inflammatoire. Les auteurs suggèrent que cette combinaison — moins de cellules, mais davantage orientées vers un nettoyage rapide des débris — pourrait accélérer l’élimination sûre des photorécepteurs mourants tout en épargnant leurs voisins encore sains.
Ce que cela pourrait signifier pour les traitements futurs
Ce travail montre qu’un inhibiteur systémique du CSF1R peut remodeler les réponses immunitaires locales et circulantes dans le décollement de la rétine et, de manière quelque peu contre‑intuitive, qu’une équipe de nettoyage plus petite mais plus inflammatoire peut protéger la vision. En dépeuplant temporairement les microglies, en retardant la première vague de cellules d’origine sanguine et en réorientant les sous‑types de monocytes, le PLX5622 a créé une fenêtre temporelle durant laquelle les dommages précoces d’origine immunitaire ont été réduits et davantage de photorécepteurs ont survécu. Bien que l’étude ait été réalisée chez la souris et que l’équilibre entre inflammation bénéfique et nocive diffère selon les maladies oculaires, ces résultats soutiennent l’inhibition du CSF1R comme point de départ prometteur pour des médicaments visant à ajuster finement la réponse immunitaire et préserver la vue après une lésion rétinienne.
Citation: Pastor-Puente, S., Jung, R., Gonzalez-Buendia, L. et al. Colony-stimulating factor 1 receptor inhibition is neuroprotective to photoreceptors in retinal detachment. Cell Death Dis 17, 264 (2026). https://doi.org/10.1038/s41419-026-08470-1
Mots-clés: décollement de la rétine, microglie, survie des photorécepteurs, neuroinflammation, inhibition du CSF1R