Clear Sky Science · fr
Reconfigurer le destin des cellules de mélanome : des modulateurs de TRPM8 provoquent l’apoptose et renforcent la cytotoxicité des cellules NK
Pourquoi utiliser un « capteur de froid » contre le cancer cutané a de l’importance
Le mélanome est une forme dangereuse de cancer de la peau qui apprend souvent à échapper à la fois aux médicaments et au système immunitaire. Cette étude explore une faiblesse inattendue des cellules de mélanome : une protéine appelée TRPM8, mieux connue comme le capteur qui permet aux neurones de percevoir le froid ou le menthol. Les chercheurs montrent que des composés conçus pour bloquer TRPM8 peuvent pousser les cellules de mélanome à s’auto-détruire tout en les rendant plus faciles à cibler par les cellules immunitaires tueuses naturelles (NK). Cette double action suggère une nouvelle voie de traitement pour les mélanomes avancés et résistants.
Un interrupteur caché sur les cellules de mélanome
En examinant de vastes bases de données sur le cancer et en étudiant des cellules de mélanome dérivées de patients en laboratoire, l’équipe a constaté que TRPM8 est beaucoup plus abondant dans le mélanome métastatique que dans la peau normale, y compris les mélanocytes sains et les fibroblastes dermiques. Par imagerie, ils ont montré que TRPM8 se trouve à la fois à la surface cellulaire et sur des membranes internes, le plaçant à des emplacements stratégiques pour influencer le comportement cellulaire. Lorsqu’ils ont testé une série de nouvelles molécules ciblant TRPM8, deux composés (nommés 4 et 9) se sont démarqués de façon constante : ils réduisaient fortement la survie des cellules de mélanome au fil du temps tout en épargnant en grande partie les cellules cutanées normales. Des tests génétiques ont confirmé que, lorsque TRPM8 était supprimé, ces drogues perdaient leur pouvoir létal, et lorsque TRPM8 était surexprimé, les cellules de mélanome devenaient encore plus sensibles, prouvant que l’effet dépend de ce canal spécifique. 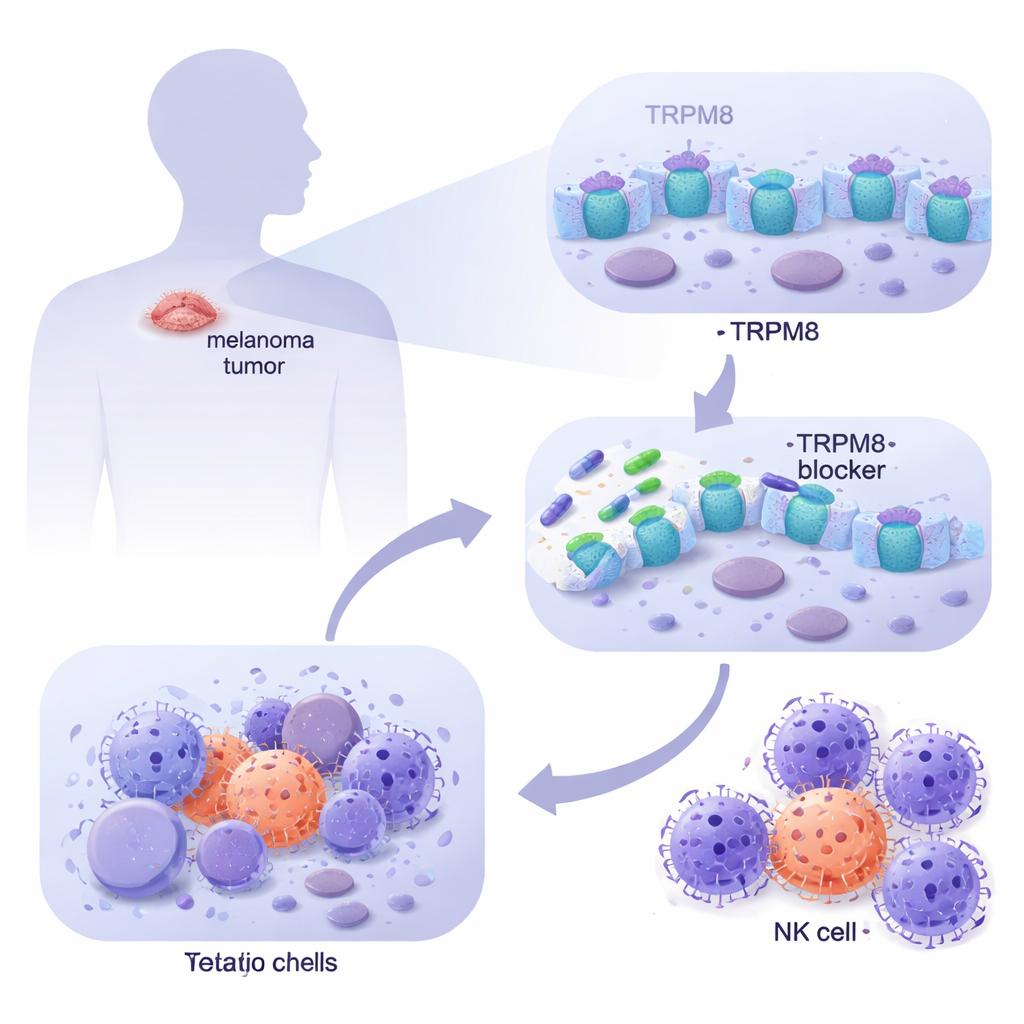
Forcer les cellules cancéreuses dans une crise énergétique
Contrairement aux activateurs classiques de TRPM8 comme le menthol, qui entraînent une entrée massive de calcium dans les cellules, ces nouveaux bloqueurs n’ont pas déclenché de variations calciques. À la place, ils ont lancé une vague de stress oxydatif à l’intérieur des cellules de mélanome. Les composés ont rapidement augmenté les espèces réactives de l’oxygène, en particulier au sein des mitochondries, les centrales énergétiques de la cellule. Cette explosion oxydative a provoqué la perte du potentiel électrique mitochondrial, leur fragmentation et la fuite de cytochrome c, une étape clé pour activer le programme interne de « suicide » cellulaire. Des antioxydants qui neutralisent ces molécules réactives ont en grande partie protégé les cellules, montrant que le déséquilibre redox n’est pas un effet secondaire mais le moteur de la mort cellulaire. En aval, des marqueurs classiques de la mort tels que l’activation de la caspase-3 et la clivage de PARP ont confirmé que les cellules subissaient une apoptose programmée plutôt qu’une lésion aléatoire.
Désarmer les signaux de survie et réveiller un gardien
Le choc oxydatif a déclenché une réponse de stress plus large. Les médicaments ont activé ATM, un détecteur de dommages à l’ADN, et conduit à l’accumulation et à l’activation de p53, une célèbre protéine suppresseur de tumeur qui décide si une cellule endommagée doit se réparer ou mourir. Parallèlement, les composés ont affaibli l’une des principales voies de survie du mélanome : la voie PI3K–AKT. Normalement, TRPM8 interagit physiquement avec des composants de la PI3K pour maintenir AKT dans sa forme active, promotrice de croissance. Après traitement, ce partenariat s’est rompu et l’activité d’AKT a chuté, basculant davantage l’équilibre en faveur de la mort cellulaire. Fait important, ces changements ont été prononcés dans les cellules de mélanome mais pas dans les cellules non cancéreuses, suggérant une fenêtre thérapeutique où la tumeur est fortement affectée tandis que les tissus sains sont épargnés.
Rendre les tumeurs plus visibles aux « escouades » immunitaires
Le danger du mélanome tient aussi à sa capacité à échapper à la surveillance immunitaire. Les chercheurs ont donc examiné ce qui arrive aux cellules tumorales qui survivent à de faibles doses de bloqueurs de TRPM8 sur des périodes plus longues. Ils ont découvert que ces cellules persistantes commençaient à afficher davantage un marqueur de surface appelé ULBP1, qui joue le rôle de signal de détresse reconnu par les récepteurs NKG2D des cellules NK. D’autres signaux apparentés ne changeaient pas, indiquant un effet sélectif. Dans des sphéroïdes de mélanome en trois dimensions, qui imitent mieux les tumeurs réelles, un pré-traitement par les bloqueurs de TRPM8 a non seulement réduit la taille des structures et augmenté la mort cellulaire, mais les a aussi rendues bien plus vulnérables à l’attaque des cellules NK. Lorsque ULBP1 ou NKG2D était bloqué par des anticorps, cette augmentation de la destruction disparaissait en grande partie, montrant que l’amélioration du nettoyage immunitaire passe par cette interaction spécifique entre la tumeur et les cellules NK. 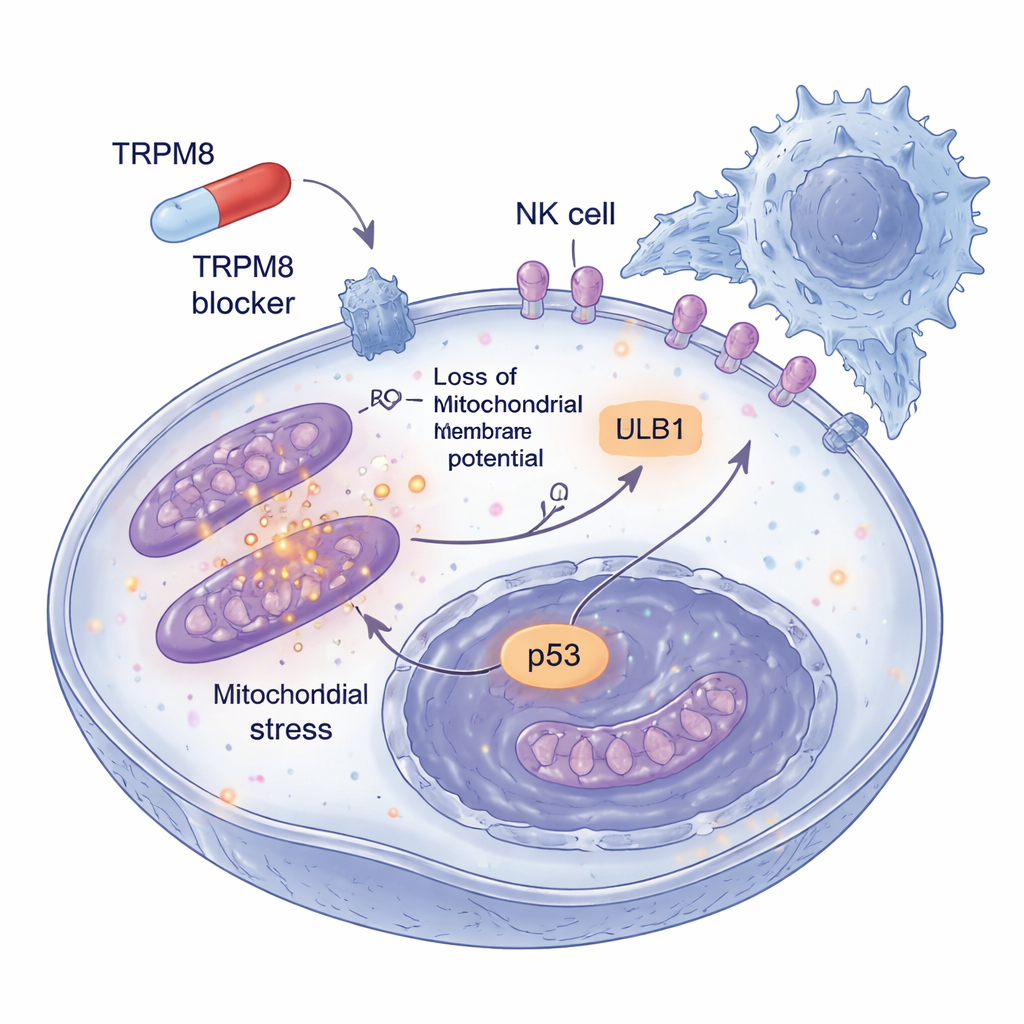
Ce que cela pourrait signifier pour la prise en charge future du mélanome
En termes simples, bloquer le « capteur de froid » TRPM8 le transforme en levier thérapeutique : il pousse les cellules de mélanome dans une crise mitochondriale et d’ADN fatale tout en les signalant pour destruction par les cellules NK. Parce que ces médicaments épargnent les cellules cutanées normales et n’endommagent pas les cellules NK elles-mêmes, ils constituent une base prometteuse pour de nouveaux traitements. Les auteurs suggèrent que les bloqueurs de TRPM8 pourraient être combinés avec des immunothérapies existantes pour attaquer le mélanome avancé et résistant aux médicaments sur deux fronts : tuer directement les cellules tumorales et rendre les survivantes plus faciles à repérer et à détruire par le système immunitaire.
Citation: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Mots-clés: mélanome, TRPM8, mitochondries, stress oxydatif, cellules tueuses naturelles