Clear Sky Science · fr
La lactylation activant TRIM29 induit un comportement invasif et des métastases ganglionnaires dans le cancer gastrique via la voie Wnt/β-caténine médiée par hnRNPA1
Pourquoi cette recherche est importante
Le cancer gastrique (de l’estomac) est l’un des cancers les plus mortels au monde, en grande partie parce qu’il se propage tôt aux ganglions lymphatiques voisins, rendant la guérison par chirurgie difficile. Cette étude dévoile comment une modification chimique liée au métabolisme tumoral suractive une protéine appelée TRIM29, aidant les cellules cancéreuses à envahir les tissus environnants, à stimuler la formation de nouveaux vaisseaux lymphatiques et à résister à la chimiothérapie. Comprendre cette chaîne d’événements ouvre la voie à de nouvelles stratégies pour ralentir voire bloquer la dissémination du cancer de l’estomac.
Un partenariat dangereux dans les tumeurs gastriques
Les chercheurs ont commencé par comparer des échantillons de cancer gastrique avec des tissus sains adjacents provenant de 100 patients, ainsi que de larges bases de données publiques de gènes. Ils ont constaté que TRIM29, une protéine précédemment associée à la régulation immunitaire et à d’autres cancers, était systématiquement plus élevée dans les cellules tumorales. Les patients dont les tumeurs présentaient davantage de TRIM29 étaient plus susceptibles d’avoir un cancer dans les ganglions lymphatiques et les vaisseaux sanguins et présentaient une survie globale plus mauvaise. Ces constatations suggèrent que TRIM29 n’est pas seulement présent, mais qu’il participe activement à rendre le cancer gastrique plus agressif.
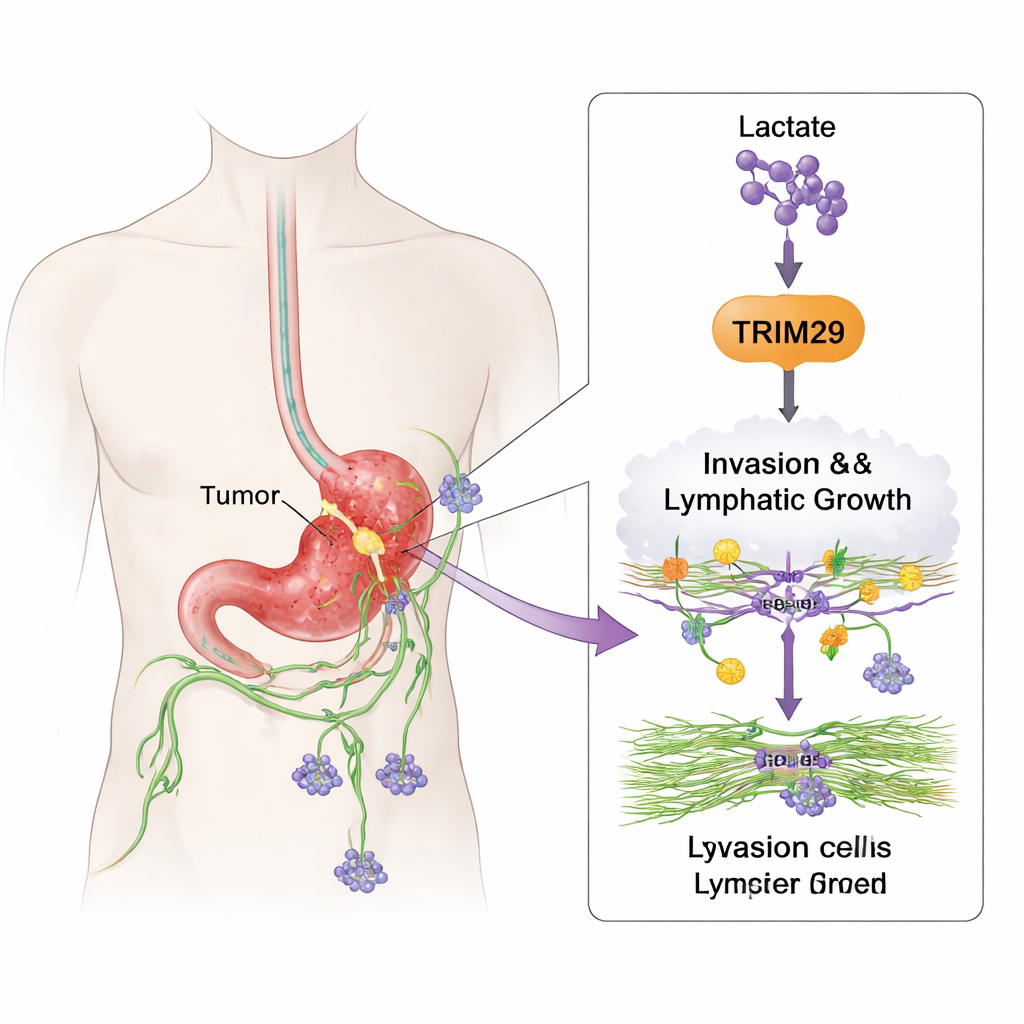
Comment les cellules cancéreuses apprennent à migrer
Pour comprendre ce que fait TRIM29, l’équipe a modifié ses niveaux dans des lignées cellulaires de cancer gastrique. Lorsqu’ils ont réduit TRIM29, les cellules sont devenues nettement moins mobiles et moins capables de traverser des gels 3D imitant les tissus corporels. Augmenter TRIM29 produisait l’effet inverse, rendant les cellules plus invasives. Les chercheurs ont également étudié les cellules endothéliales lymphatiques, les cellules qui tapissent les vaisseaux lymphatiques. Les cellules cancéreuses riches en TRIM29 ont encouragé ces cellules vasculaires à bourgeonner et à former des structures tubulaires, signe d’une nouvelle formation de vaisseaux lymphatiques (lymphangiogenèse). Dans des modèles murins, les tumeurs exprimant beaucoup de TRIM29 ont généré davantage de métastases hépatiques et ganglionnaires, tandis que celles avec TRIM29 réduit se sont moins propagées et ont formé moins de vaisseaux lymphatiques.
Relais moléculaire : protection d’un régulateur clé
En approfondissant, les scientifiques ont découvert que TRIM29 se lie physiquement à une autre protéine, hnRNPA1, connue pour influencer le traitement des gènes et liée à la dissémination tumorale. Normalement, hnRNPA1 peut être marqué pour destruction par une autre protéine, une enzyme appelée ZFP91, via le système d’élimination cellulaire. TRIM29 perturbe ce processus en entrant en compétition avec ZFP91 pour la liaison à hnRNPA1. Lorsque TRIM29 est abondant, il protège hnRNPA1 d’être étiqueté et dégradé. En conséquence, hnRNPA1 devient plus stable et s’accumule dans les cellules cancéreuses, déclenchant une cascade de signaux qui aboutit à l’activation de la voie Wnt/β-caténine, un moteur bien connu de la croissance et de la mobilité tumorales. Cela augmente à son tour la production de VEGF‑C, une molécule qui stimule la formation de nouveaux vaisseaux lymphatiques, offrant aux cellules cancéreuses davantage de « routes » pour s’échapper.
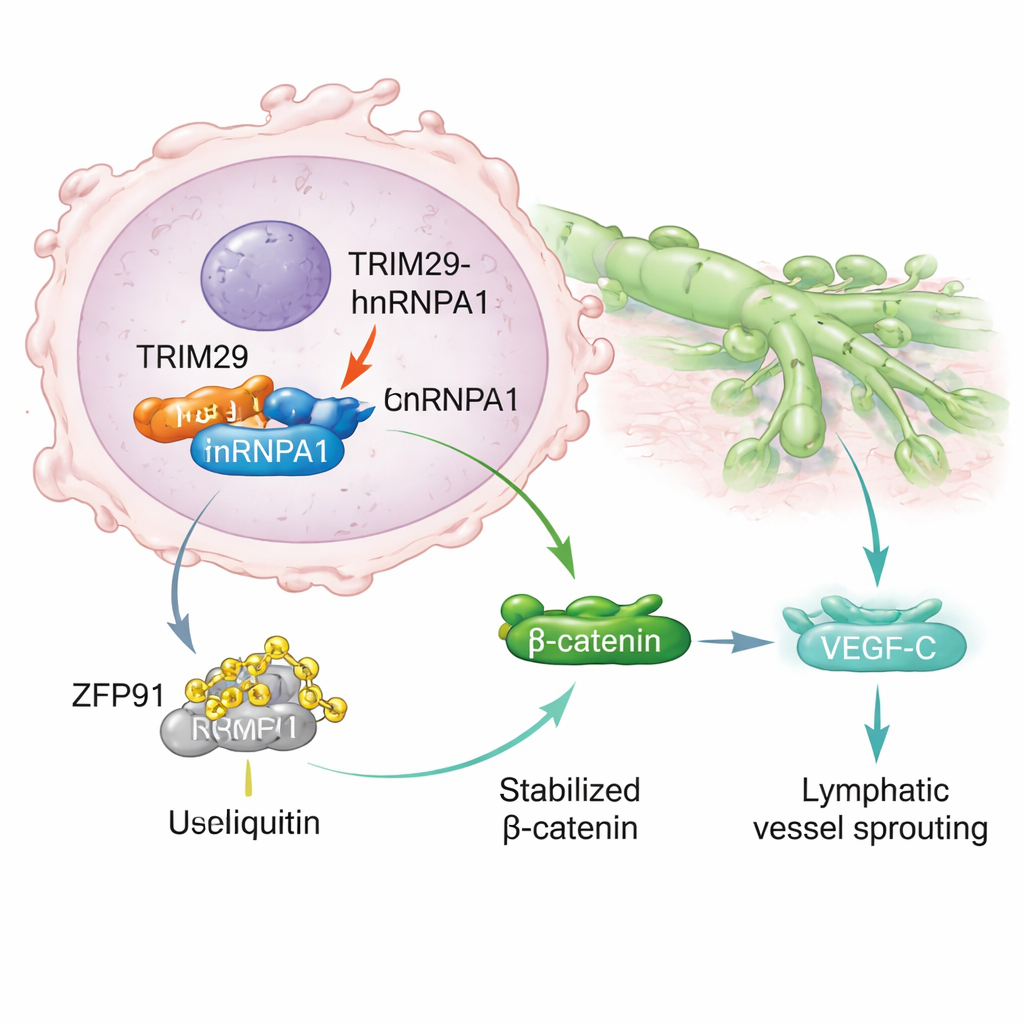
Alimenter le cancer avec le lactate
L’étude relie également ce comportement invasif à la manière dont les tumeurs métabolisent les sucres. Les cancers à croissance rapide reposent souvent sur une forme de métabolisme qui produit de grandes quantités de lactate, un sous-produit longtemps considéré comme un simple déchet. Ici, les auteurs montrent que le lactate peut modifier chimiquement les histones qui emballent l’ADN, spécifiquement en un site appelé H3K9. Cette « lactylation » agit comme un interrupteur d’activation pour le gène TRIM29, augmentant son expression. Lorsque les chercheurs ont réduit la production de lactate avec des médicaments métaboliques, les niveaux de TRIM29 ont diminué ; lorsqu’ils ont augmenté le lactate, TRIM29 a augmenté. Les tissus gastriques des patients présentaient des niveaux plus élevés de cette lactylation sur H3K9, en corrélation avec une TRIM29 accrue, plus de propagation aux ganglions lymphatiques et une survie plus mauvaise. En substance, le métabolisme altéré de la tumeur contribue à écrire un programme génétique plus agressif.
Nouvelles façons d’améliorer la chimiothérapie
Les vaisseaux lymphatiques font plus que transporter des cellules cancéreuses ; ils peuvent aussi drainer les médicaments de chimiothérapie hors des tumeurs. En utilisant des greffes tumorales dérivées de patients et implantées chez la souris, les chercheurs ont testé si bloquer TRIM29 et la croissance des vaisseaux lymphatiques pouvait améliorer l’effet du 5‑fluorouracile (5‑FU), un médicament standard contre le cancer gastrique. Inhiber TRIM29 ou bloquer la lymphangiogenèse a rendu le 5‑FU plus efficace pour réduire la taille des tumeurs et diminuer la division cellulaire. La combinaison des deux stratégies a produit la réponse la plus forte, suggérant une piste pour surmonter certaines formes de résistance aux médicaments dans les stades avancés.
Ce que cela signifie pour les patients
Ce travail décrit étape par étape : les tumeurs gastriques produisent un excès de lactate, qui active TRIM29 ; TRIM29 protège alors hnRNPA1, stabilise une voie de croissance et augmente la formation de vaisseaux lymphatiques et la propagation vers les ganglions. Cliniquement, des niveaux élevés de TRIM29 et des marques de lactylation associées identifient les patients à risque plus élevé de maladie agressive. À l’avenir, des médicaments qui réduisent le signalement du lactate, bloquent TRIM29 ou empêchent la formation de vaisseaux lymphatiques pourraient être associés à la chimiothérapie existante pour limiter la dissémination du cancer gastrique et améliorer l’efficacité des traitements.
Citation: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Mots-clés: métastase du cancer gastrique, TRIM29, lactate et lactylation, lymphangiogenèse, voie Wnt bêta-caténine