Clear Sky Science · fr
KIF20A inhibe l’ubiquitination dépendante de TRIM21 de DHX9 pour renforcer la stabilité de SOX2, augmentant la « stemness » et la résistance à la ferroptose dans le carcinome épidermoïde buccal
Pourquoi cette recherche compte pour les patients atteints de cancer buccal
Le carcinome épidermoïde buccal, une forme courante de cancer de la bouche, récidive souvent et résiste aux traitements. De nombreux échecs de chirurgie, chimiothérapie et radiothérapie sont liés à un petit groupe persistant de « cellules souches cancéreuses » capables de régénérer la tumeur et de résister à la mort cellulaire. Cette étude révèle un circuit moléculaire clé qui aide ces cellules à survivre et à résister à une forme émergente de mort cellulaire appelée ferroptose, et elle pointe vers une stratégie médicamenteuse susceptible d’améliorer l’efficacité de la chimiothérapie standard.
Un moteur caché dans les tumeurs buccales
Les chercheurs ont commencé par comparer des échantillons tumoraux de patients atteints de cancer buccal à des tissus sains adjacents. Ils ont constaté que la protéine KIF20A était systématiquement beaucoup plus abondante dans les cellules tumorales. En examinant des séries de patients plus larges, les personnes dont les tumeurs exprimaient davantage de KIF20A avaient tendance à avoir une survie plus courte, ce qui suggère que cette protéine est associée à une maladie agressive. 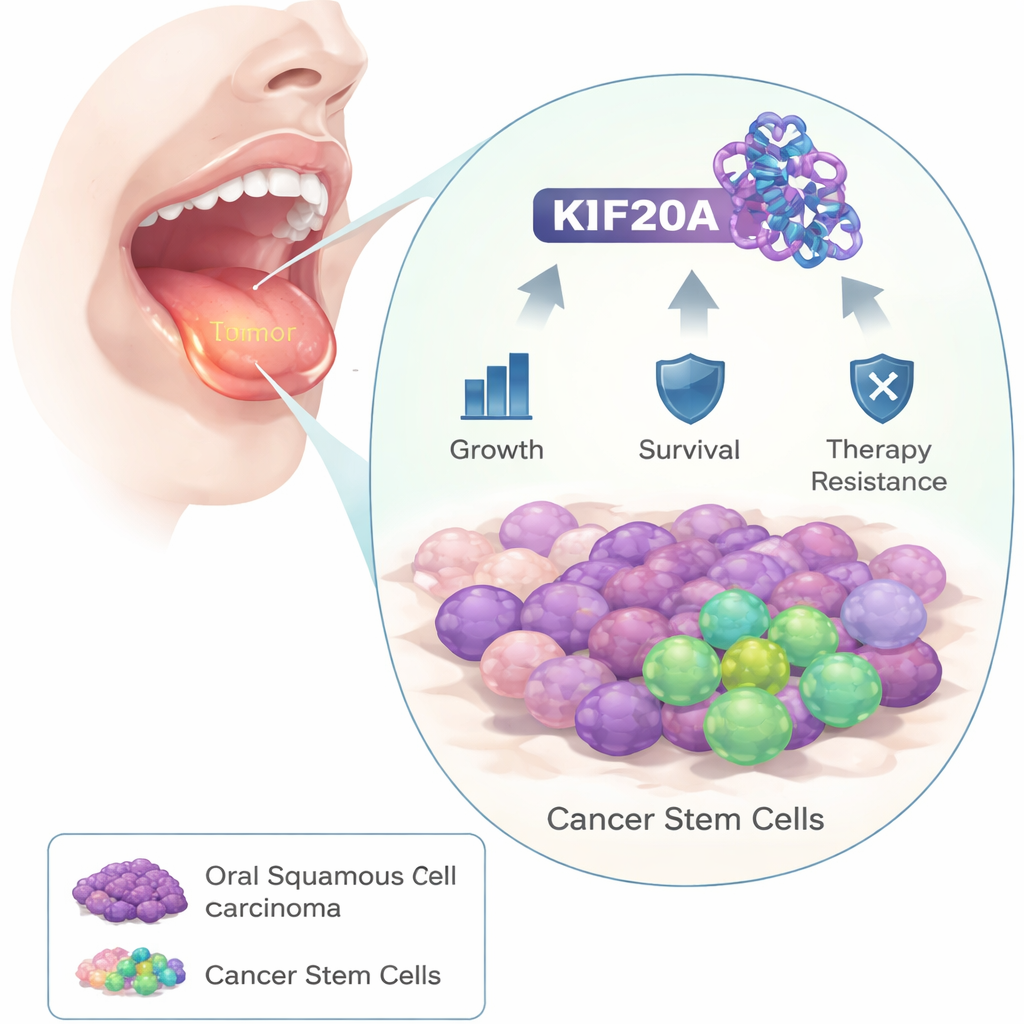
Comment KIF20A protège un aideur clé de l’ARN
Pour comprendre ce que fait KIF20A, l’équipe a utilisé des méthodes de cartographie des protéines pour chercher ses partenaires à l’intérieur des cellules cancéreuses. Un partenaire central mis en évidence a été DHX9, une protéine qui aide à réguler les molécules d’ARN et influence la durée de vie de certains messages cellulaires. Les scientifiques ont découvert que KIF20A se lie à DHX9 et l’empêche d’être marqué pour destruction par une autre protéine, la ligase E3 TRIM21, qui normalement étiquette DHX9 par des chaînes d’ubiquitine envoyant la protéine vers le broyeur cellulaire. En bloquant ce marquage, KIF20A ralentit la dégradation de DHX9 et augmente ses niveaux, en particulier dans le cytoplasme où il peut agir sur des cibles ARN spécifiques.
De la stabilité de l’ARN aux cellules souches cancéreuses et à la résistance à la ferroptose
Avec DHX9 stabilisé, un autre acteur crucial entre en jeu : SOX2, un gène maître qui aide les cellules à rester dans un état de type souche et à résister aux traitements. L’étude montre que DHX9 protège le message ARN de SOX2 contre la dégradation, permettant la synthèse d’une plus grande quantité de protéine SOX2. Dans les cellules cancéreuses buccales, un excès de KIF20A entraînait davantage de DHX9 et de SOX2, une augmentation de la formation de sphéroïdes tumoraux en culture et une plus grande fraction de cellules exprimant des marqueurs de cellules souches — des signes d’une « stemness » tumorale renforcée. KIF20A rendait également les cellules moins vulnérables à la ferroptose, un type de mort cellulaire liée au fer et aux lipides étudié comme moyen d’éliminer les cellules résistantes. Lorsque KIF20A était inhibé, les tumeurs régressaient plus facilement chez la souris et les marqueurs de ferroptose augmentaient, indiquant que les tumeurs avaient perdu cette protection.
Un circuit moléculaire avec une faiblesse pharmacologique
En rassemblant ces éléments, les auteurs proposent un axe KIF20A–DHX9–SOX2 : KIF20A stabilise DHX9, DHX9 stabilise l’ARN de SOX2, et SOX2 à son tour maintient les cellules souches cancéreuses et empêche la ferroptose. Ce circuit alimente également la voie PI3K–AKT, une voie majeure de croissance et de survie dans de nombreux cancers. 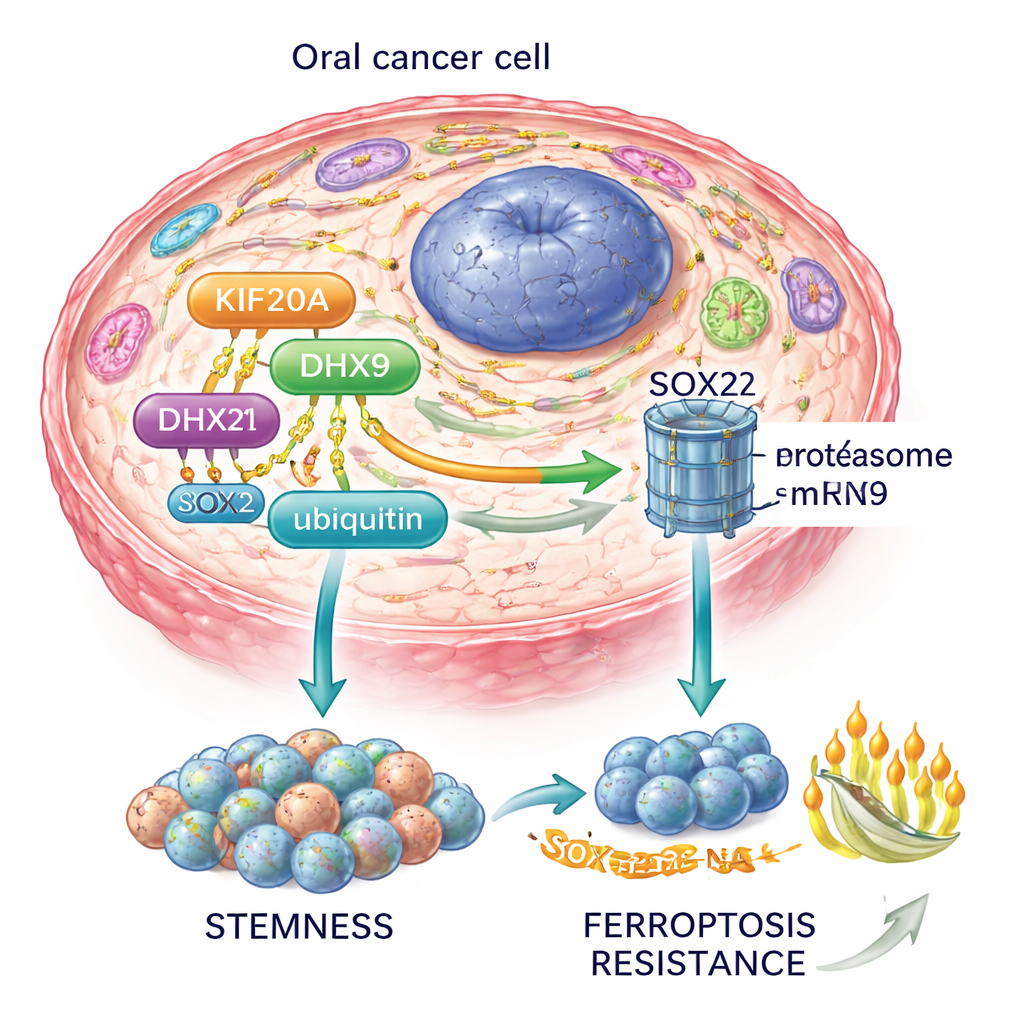
Un médicament candidat pour affaiblir les tumeurs résistantes
Pour avancer vers une thérapie, l’équipe a exploré de larges bases de données médicament–gène à la recherche de composés susceptibles de contrer les profils d’expression associés à KIF20A. Ils ont identifié ENMD-2076, un inhibiteur oral multitarget des kinases déjà testé dans d’autres cancers. Dans des cellules cancéreuses buccales à forte expression de KIF20A, l’ENMD-2076 réduisait les niveaux de KIF20A, DHX9 et SOX2, atténuait la signalisation liée à la stemness et ralentissait la croissance. Associé au cisplatine, chimiothérapique standard, ENMD-2076 produisait un effet anticancéreux plus marqué que chaque médicament pris séparément, tant en culture cellulaire que sur des tumeurs murines, sans toxicité ajoutée évidente.
Ce que cela signifie pour les thérapies futures
Pour un public non spécialiste, l’essentiel est que cette étude révèle comment une protéine hyperactive, KIF20A, aide les tumeurs buccales à conserver une petite réserve de cellules « graine » vivantes et protégées contre une forme prometteuse de mort cellulaire. En cartographiant cette chaîne — de KIF20A à DHX9 puis à SOX2 — les chercheurs mettent en lumière de nouvelles cibles médicamenteuses et montrent qu’un médicament expérimental existant, ENMD-2076, peut affaiblir cet axe et rendre le cisplatine plus efficace dans des modèles. Bien que des travaux supplémentaires soient nécessaires pour évaluer la sécurité et confirmer les bénéfices chez les patients, ces résultats soutiennent l’idée qu’inhiber ce circuit pourrait, à l’avenir, aider à prévenir les rechutes et à surmonter la résistance aux traitements dans le cancer buccal.
Citation: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Mots-clés: carcinome épidermoïde buccal, cellules souches cancéreuses, ferroptose, KIF20A, SOX2