Clear Sky Science · fr
La sélénométhionine comme inhibiteur de la ferroptose à double mécanisme : apport en sélénium stimulant la biosynthèse de GPX4 au‑delà de la transsulfuration et élimination des ROS par capacité réductrice indépendante de l’activité de GPX4
Pourquoi il est important de protéger nos cellules d’une mort « analogue à la rouille »
Les cellules de notre organisme peuvent mourir de multiples façons, et l’une des plus récentes et intrigantes est la ferroptose — une détérioration des membranes cellulaires entraînée par le fer, semblable à une « rouille ». Ce processus est désormais associé à des maladies allant des lésions rénales à la neurodégénérescence. L’oligo‑élément sélénium, connu du grand public via les compléments alimentaires, joue un rôle clé pour contrer cette forme dangereuse de mort cellulaire. Cette étude examine comment un acide aminé courant contenant du sélénium, la sélénométhionine, peut protéger les cellules de la ferroptose par deux stratégies distinctes mais complémentaires.
Un nouveau protecteur identifié grâce à un large criblage de composés
Pour identifier de petites molécules capables de bloquer la ferroptose, les chercheurs ont testé des milliers de composés issus de médicaments approuvés et de produits naturels. Ils ont utilisé un composé chimique, le RSL3, pour déclencher la ferroptose dans des lignées cellulaires cancéreuses humaines, puis ont surveillé la mort cellulaire et l’accumulation de lipides oxydés endommagés dans les membranes. Parmi tous les candidats, la sélénométhionine est apparue comme un protecteur efficace : elle a réduit à la fois les dommages lipidiques et la mort cellulaire dans différents types cellulaires et dans deux modèles majeurs de ferroptose — l’un induit par l’inhibition directe de GPX4 (avec RSL3) et l’autre par la privation en cystine, précurseur du glutathion antioxydant. Ces résultats positionnent la sélénométhionine comme un inhibiteur de la ferroptose à la fois large et robuste. 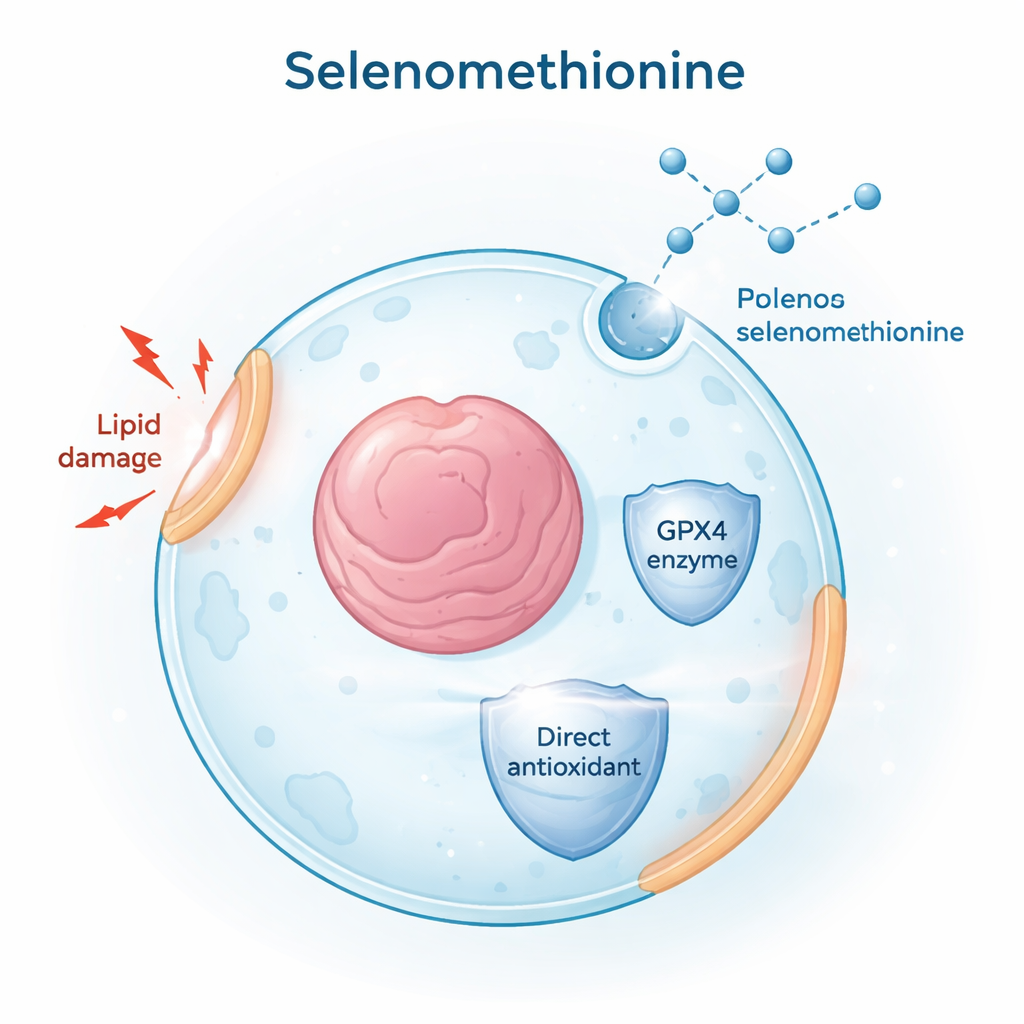
Approvisionnement en sélénium pour une enzyme protectrice essentielle
Un bouclier anti‑ferroptose central dans les cellules est l’enzyme GPX4, qui nécessite du sélénium pour fonctionner. L’équipe a voulu déterminer si la sélénométhionine se contente d’alimenter cette voie ou si elle joue un rôle plus large. Ils ont suivi la conversion du sélénium provenant de la sélénométhionine en formes utilisables pour la synthèse de GPX4, même lorsque la voie habituelle — la transsulfuration — était affaiblie ou bloquée. En utilisant des diminutions d’expression génétique et des inhibiteurs chimiques des enzymes impliquées dans les voies sulfurées–sélénées, ils ont constaté que la sélénométhionine augmentait malgré tout les niveaux de GPX4 et protégeait les cellules. Cela montre que les cellules peuvent exploiter plusieurs voies métaboliques pour extraire le sélénium de la sélénométhionine et maintenir la production de GPX4, même dans des tissus où la voie classique est faible.
Une protection indépendante de l’enzyme habituelle
De manière surprenante, lorsque les chercheurs ont supprimé complètement GPX4 des cellules par édition génétique CRISPR, la sélénométhionine a continué à protéger contre la ferroptose. Elle réduisait toujours les dommages lipidiques membranaires et la mort cellulaire, indiquant que GPX4 n’explique pas tout. D’autres expériences ont suggéré qu’une partie de cette protection impliquait l’incorporation de la sélénométhionine dans des protéines nouvellement synthétisées, mais cela ne rendait pas compte de l’effet integrale. Les auteurs se sont alors intéressés à la réactivité chimique de la sélénométhionine elle‑même. Ils ont montré qu’elle peut neutraliser directement des espèces réactives de l’oxygène (ROS), y compris le peroxyde d’hydrogène, et qu’elle est convertie en une forme oxydée, un « sulfoxyde ». La spectrométrie de masse a confirmé ce produit, et l’administration de la forme sulfoxyde aux cellules réduisait aussi la ferroptose, suggérant que les cellules peuvent la recycler en sélénométhionine active via un cycle redox.
Du modèle cellulaire à la protection rénale chez l’animal entier
Pour tester si ces mécanismes ont un impact au niveau de l’organisme, l’équipe s’est tournée vers un modèle murin de lésion rénale aiguë induite par le médicament anticancéreux cisplatine, une condition connue pour impliquer la ferroptose. Les souris traitées par cisplatine présentaient une perte de poids, des reins enflés, une fonction rénale altérée et des niveaux élevés de marqueurs de ferroptose. Lorsque les animaux ont reçu de la sélénométhionine, nombre de ces problèmes se sont atténués : le poids corporel s’est rétabli, le gonflement rénal a diminué, les paramètres sanguins de la fonction rénale se sont normalisés, les signaux inflammatoires ont baissé et les marqueurs chimiques des dommages lipidiques ont chuté. Le tissu rénal montrait également des niveaux de GPX4 plus élevés et moins de lésions structurelles. Ces bénéfices étaient comparables à ceux observés avec la ferrostatine‑1, un bloqueur expérimentale bien connu de la ferroptose. 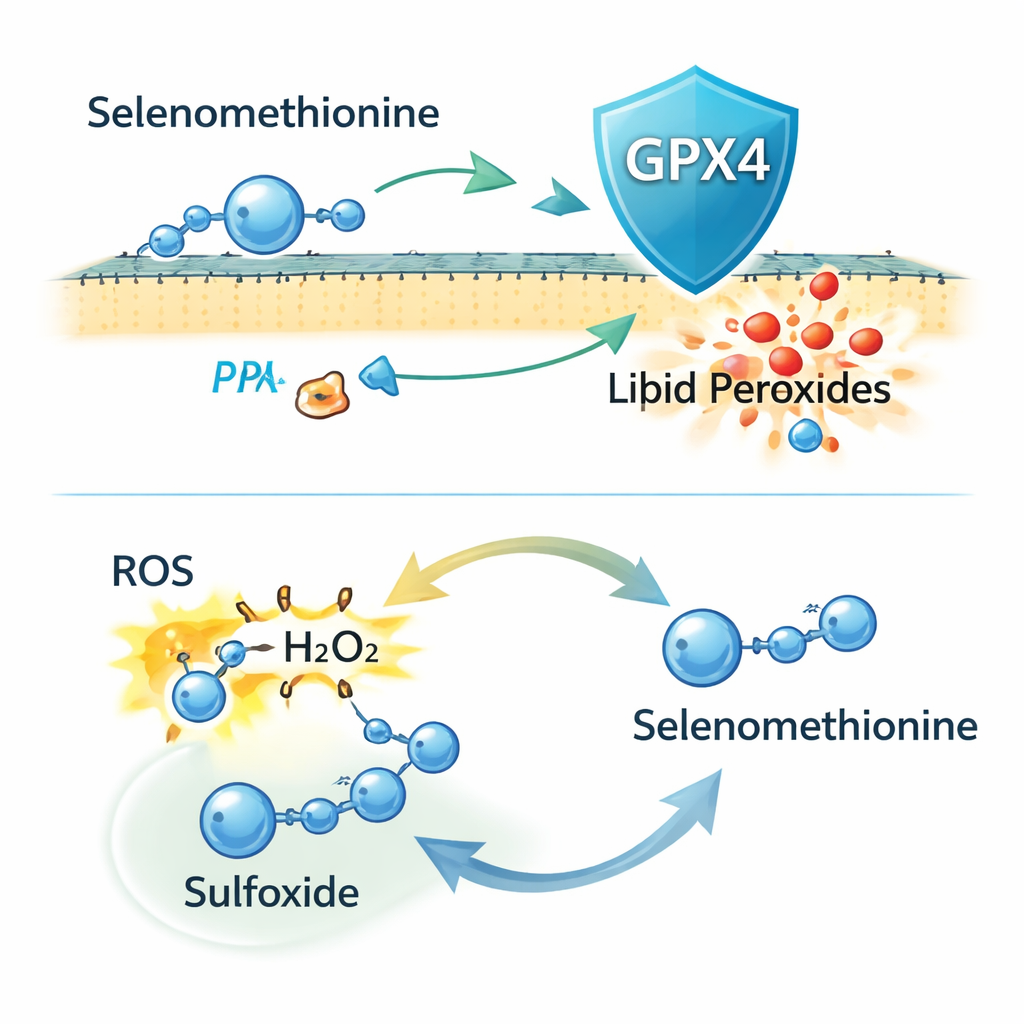
Ce que cela signifie pour les thérapies futures
Concrètement, ce travail suggère que la sélénométhionine agit comme un extincteur à double usage contre une « rouille » membranaire alimentée par le fer. D’une part, elle fournit du sélénium pour permettre aux cellules de synthétiser davantage de l’enzyme GPX4, qui élimine les lipides endommagés. D’autre part, la sélénométhionine elle‑même peut absorber les oxydants nocifs et être recyclée, offrant une protection de secours indépendante de GPX4. Ensemble, ces propriétés font de la sélénométhionine une candidate prometteuse pour prévenir ou traiter des maladies où la ferroptose joue un rôle central, telles que les lésions rénales induites par des médicaments et potentiellement d’autres affections liées à un stress oxydatif incontrôlé.
Citation: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Mots-clés: ferroptose, sélénium, sélénométhionine, stress oxydatif, lésion rénale aiguë