Clear Sky Science · fr
La chaperonine TRiC composant Cct3 est nécessaire pour le transport axonal, la myélinisation et l’affinement des jonctions neuromusculaires
Quand le câblage nerveux déraille
Nos cerveaux et nos corps dépendent de longs fibres nerveuses en forme de câbles pour transmettre les signaux rapidement et de façon fiable. Pour accomplir cette tâche, de nombreuses fibres sont entourées d’une gaine isolante, la myéline, et leurs terminaisons doivent établir des contacts précis avec les muscles. Cet article explore ce qui se produit lorsqu’un « aide » cellulaire clé pour le repliement des protéines, appelé Cct3, fait défaut. À l’aide de poissons zèbres et de tissus humains, les auteurs montrent comment ce seul composant d’un grand appareil chaperon peut perturber la myéline, les connexions nerf–muscle et le système de transport interne qui maintient les neurones en vie et fonctionnels.
Un tailleur cellulaire pour construire les nerfs
À l’intérieur de chaque cellule, les protéines nouvellement synthétisées doivent prendre la bonne forme, un peu comme on ajuste soigneusement un costume chez le tailleur. Le complexe TRiC, qui inclut la sous-unité Cct3, est l’un des principaux « tailleurs », aidant au repliement correct d’environ 10 % des protéines cellulaires — en particulier les protéines structurelles actine et tubuline. Ces éléments forment l’armature interne de la cellule et les voies le long desquelles le fret vital est déplacé. Chez des patients porteurs de versions défectueuses de CCT3 et de gènes associés, les scanners cérébraux révèlent une réduction de la substance blanche (le câblage riche en myéline du cerveau) et des problèmes au niveau des nerfs périphériques et des muscles. Les auteurs se sont donné pour objectif de comprendre comment la perte de Cct3 fait dérailler le développement et la fonction nerveux.
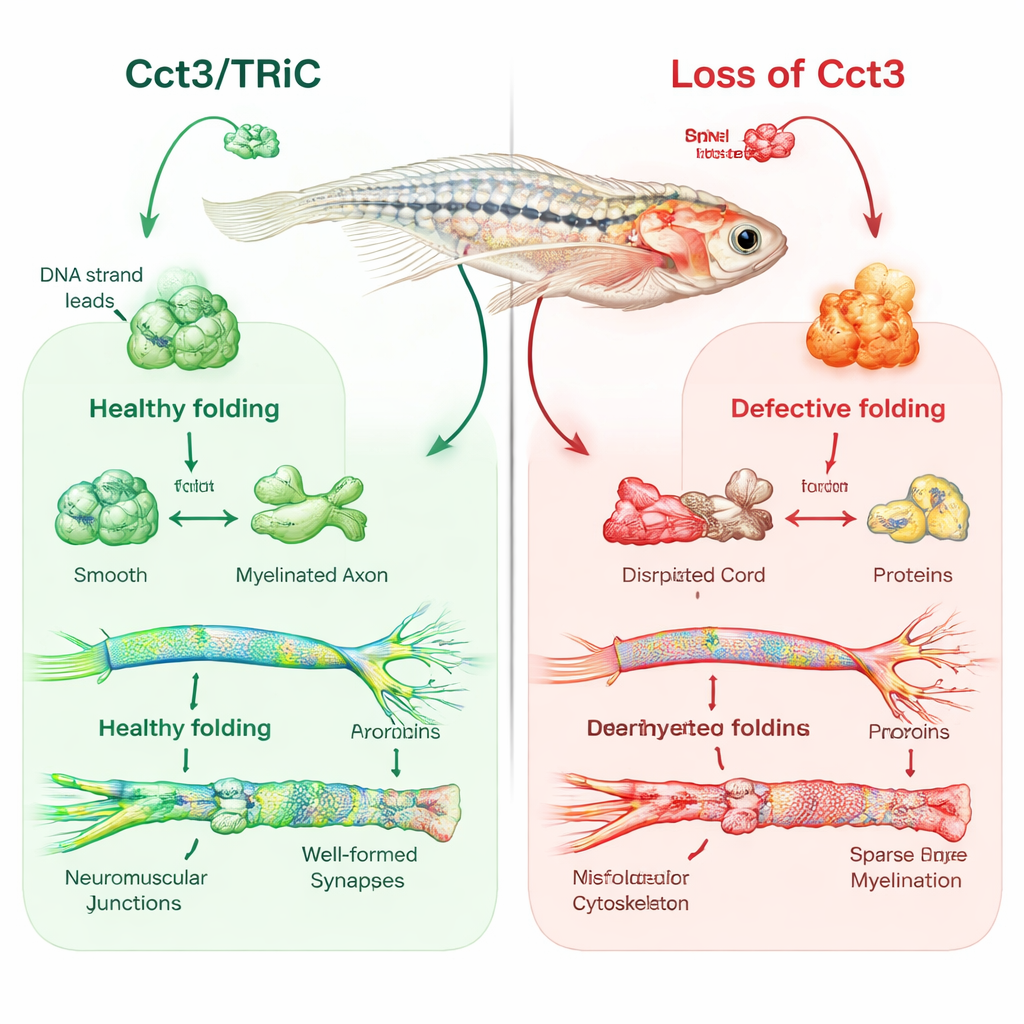
Le poisson zèbre, fenêtre sur l’isolation nerveuse
L’équipe a utilisé l’édition génomique CRISPR/Cas9 pour créer des poissons zèbres dépourvus de cct3 fonctionnel. Ces petits poissons présentaient un cerveau et des yeux plus petits, un encombrement liquidien autour du cœur, une faiblesse des réponses au toucher et mouraient en quelques jours. Lorsque les chercheurs ont rétabli un cct3 normal en injectant son ARN messager, beaucoup de ces défauts se sont atténués, confirmant que la perte de Cct3 était la cause principale. En se concentrant sur la myéline, ils ont utilisé des marqueurs fluorescents et la microscopie électronique pour visualiser les couches isolantes autour des nerfs. Chez les poissons normaux, les cellules myélinisantes du cerveau et des nerfs périphériques entouraient les axones de gaines régulières et stratifiées dès le quatrième jour de développement. En revanche, les mutants cct3 présentaient beaucoup moins de cellules myélinisantes et pratiquement pas de myéline correcte autour de nombreux axones, malgré un aspect superficiel apparemment normal de ces axones.
Cellules de soutien fragiles et liens nerf–muscle sous tension
Pour comprendre pourquoi la myéline faisait défaut, les auteurs ont examiné les cellules de Schwann et les cellules de la crête neurale apparentées — les cellules de soutien qui entourent les nerfs périphériques. Chez les poissons normaux, ces cellules étendaient de longs processus fins puis affinaient leur forme en formant des segments de myéline. Chez les mutants, elles se sont arrondies, ont raccourci leurs prolongements et se sont fragmentées. Leurs noyaux se sont désintégrés selon un schéma typique de mort cellulaire programmée, et un marqueur clé de la mort (Caspase 3 activée) est apparu, montrant que beaucoup de ces cellules mouraient précocement. Parallèlement, aux jonctions neuromusculaires où les nerfs rencontrent les muscles, le motif des « points chauds » récepteurs sur les muscles n’a pas été affiné. Au lieu de nombreux petits clusters précis, les mutants présentaient moins de plaques réceptrices, mais plus grandes, rappelant les plis synaptiques simplifiés observés chez un patient humain porteur d’une mutation de CCT3.
Pistes internes brisées et trafic de cargaison ralenti
Parce que TRiC aide au repliement de l’actine et de la tubuline, les auteurs ont observé de près l’armature interne des axones moteurs. Ils ont constaté que les niveaux globaux de tubuline étaient fortement réduits chez les mutants, et que le nombre de microtubules normaux — ces tubes creux qui servent de voies pour le transport — chutait de façon spectaculaire dans les nerfs centraux et périphériques. Les « étiquettes » chimiques sur la tubuline, importantes pour des microtubules stables et aptes au transport, étaient également gravement altérées. En utilisant l’imagerie en direct de mitochondries et d’endosomes fluorescents à l’intérieur des axones moteurs, ils ont observé le déplacement de ces cargaisons. Chez les poissons sains, les organites circulaient rapidement et de façon directionnelle le long de l’axone. Chez les mutants, beaucoup d’organites s’arrêtaient ou se balançaient d’avant en arrière, conforme à des voies endommagées et à un transport perturbé.
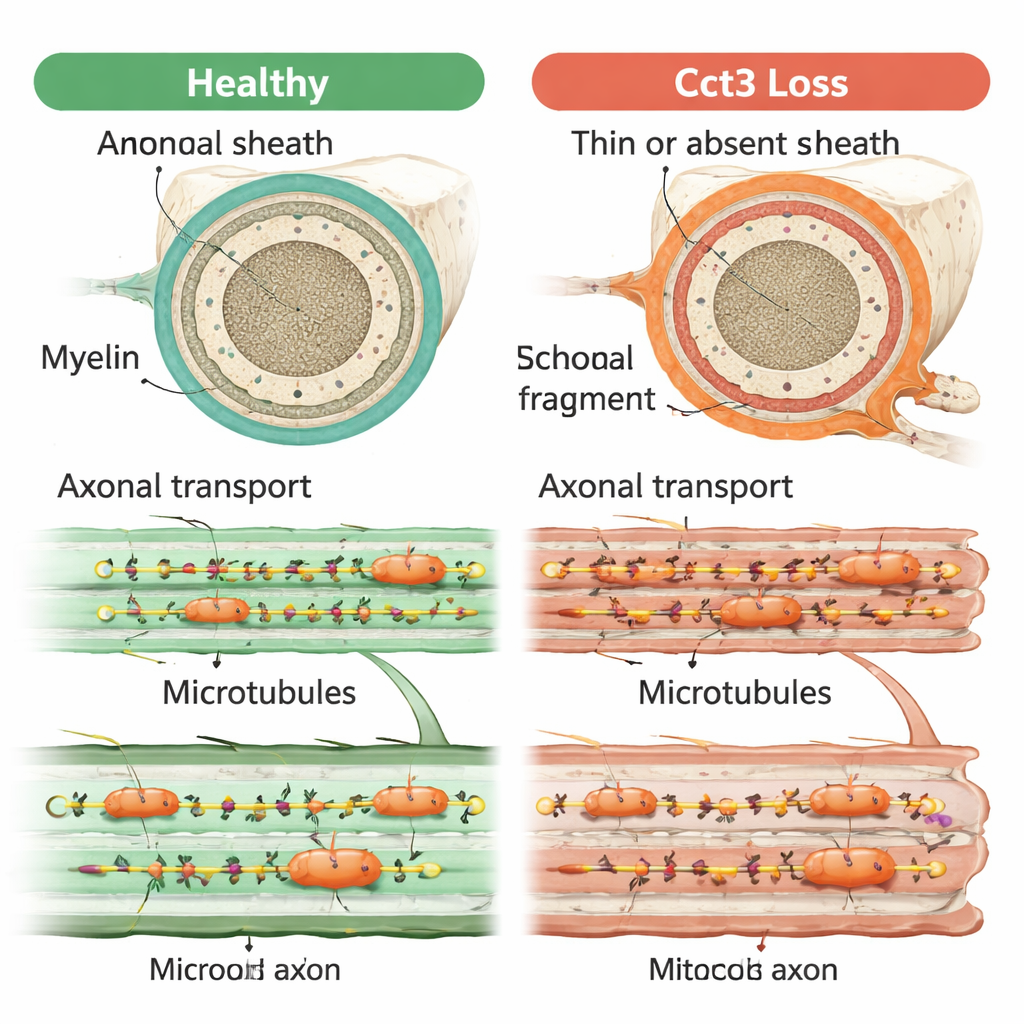
Un problème central derrière de nombreux symptômes
Dans l’ensemble, les résultats montrent que Cct3 est essentiel à plusieurs aspects interconnectés de la santé nerveuse : il soutient la survie des cellules de soutien myélinisantes, permet un enroulement myélinique correct et autorise l’affinement des jonctions neuromusculaires en maturation. Tous ces rôles remontent à sa fonction dans le repliement et le maintien des protéines qui constituent le cytosquelette et les pistes microtubulaires utilisées pour le transport axonal. Lorsque ces voies échouent, signaux et matériaux clés ne peuvent pas atteindre les bons endroits le long de l’axone, compromettant vraisemblablement à la fois la communication avec les cellules myélinisantes et la formation précise des contacts nerf–muscle. Ce travail suggère que l’altération du transport axonal pourrait être le fil conducteur reliant les divers problèmes cérébraux et nerveux observés dans les troubles liés à TRiC.
Citation: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Mots-clés: myélinisation, transport axonal, jonction neuromusculaire, chaperons moléculaires, modèle de poisson zèbre