Clear Sky Science · fr
Trafic et signalisation BDNF-TrkB altérés dans les neurones du télencéphale basal de la trisomie 21
Pourquoi cette étude cérébrale est importante
Les personnes atteintes de trisomie 21 vivent plus longtemps qu’autrefois, mais elles présentent aussi un risque très élevé de développer une démence de type Alzheimer dès la moitié de la vie. Cette étude examine en profondeur des cellules nerveuses individuelles pour comprendre pourquoi certains neurones sont particulièrement vulnérables. En suivant la manière dont ces cellules déplacent et répondent à une molécule clé « fertilisante » du cerveau, les chercheurs mettent au jour un embouteillage à l’intérieur des neurones qui pourrait aider à expliquer la perte de mémoire et orienter de nouvelles stratégies thérapeutiques.
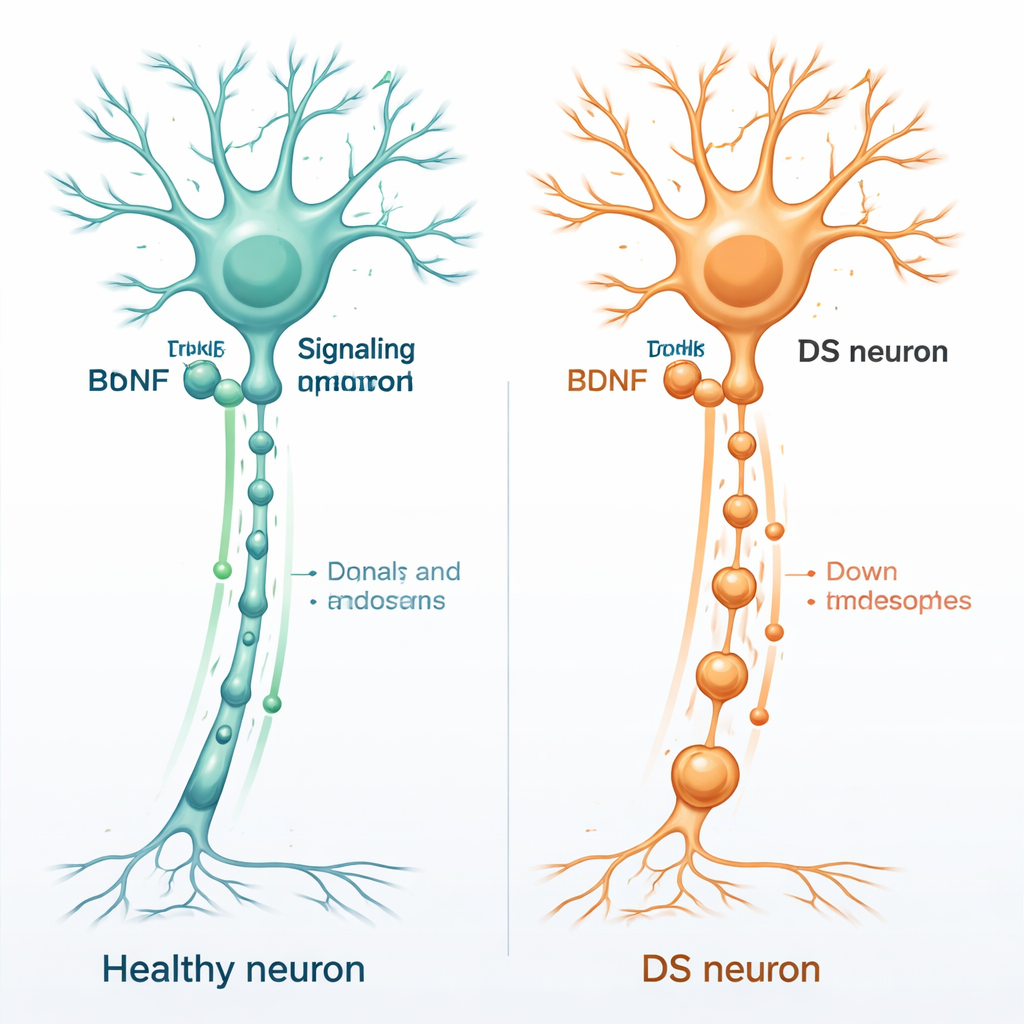
Le « fertilisant » cérébral et la santé des neurones
Les cellules cérébrales saines dépendent d’un ensemble de molécules de soutien appelées neurotrophines, qui agissent comme un fertilisant pour les neurones. L’une des plus importantes est le facteur neurotrophique d’origine cérébrale, ou BDNF. Le BDNF se lie à une protéine d’ancrage sur les neurones appelée TrkB, généralement aux extrémités distales des fibres nerveuses. Une fois le BDNF fixé, le complexe BDNF–TrkB est internalisé dans de petites sphères membranaires et transporté en sens rétrograde le long de l’axone jusqu’au corps cellulaire. Ces vésicules en mouvement, appelées endosomes de signalisation, informent le noyau des gènes à activer pour maintenir le neurone en vie, connecté et adaptable.
Quand les conteneurs cellulaires gonflent trop
L’équipe s’est concentrée sur les neurones du télencéphale basal, un groupe de cellules qui soutient fortement la mémoire et l’attention et qui fait partie des premiers à dégénérer dans la trisomie 21 comme dans la maladie d’Alzheimer. En utilisant un modèle de souris de la trisomie 21 appelé Dp1Tyb, ils ont marqué les neurones pour un marqueur d’endosomes précoces et les ont comparés à des neurones normaux. Les neurones de trisomie 21 contenaient beaucoup plus d’endosomes précoces, dont plus de 50 % étaient plus gros que la normale. Ces structures sont régulées par Rab5, un interrupteur moléculaire qui aide à former et trier ces « conteneurs d’expédition » internes. Les chercheurs ont trouvé que Rab5 était bloqué dans un état hyperactif dans les neurones de trisomie 21, même avant la stimulation par le BDNF, ce qui suggère que le système endosomal était déjà poussé en suractivité.
Embouteillages le long de l’axone
Les scientifiques ont ensuite cherché à savoir si ce paysage interne déformé gênait le déplacement des signaux BDNF. Ils ont cultivé des neurones dans des dispositifs microfluidiques qui séparent les corps cellulaires des terminaisons axonales, ce qui leur permet de stimuler uniquement les pointes axonales. En suivant des traceurs fluorescents anodins qui empruntent la même voie de transport que les complexes BDNF–TrkB, ils ont mesuré la vitesse de retour des endosomes de signalisation vers les corps cellulaires. Dans les neurones normaux, l’ajout de BDNF augmentait d’environ 30 % la vitesse des endosomes et réduisait leurs arrêts, témoignant d’une réponse robuste aux signaux de croissance. Dans les neurones de trisomie 21, en revanche, le BDNF n’a pas réussi à accélérer le transport ni à diminuer les pauses. Une expérience distincte suivant les récepteurs TrkB réels a confirmé que moins d’entre eux atteignaient avec succès le corps cellulaire dans les cellules de trisomie 21.
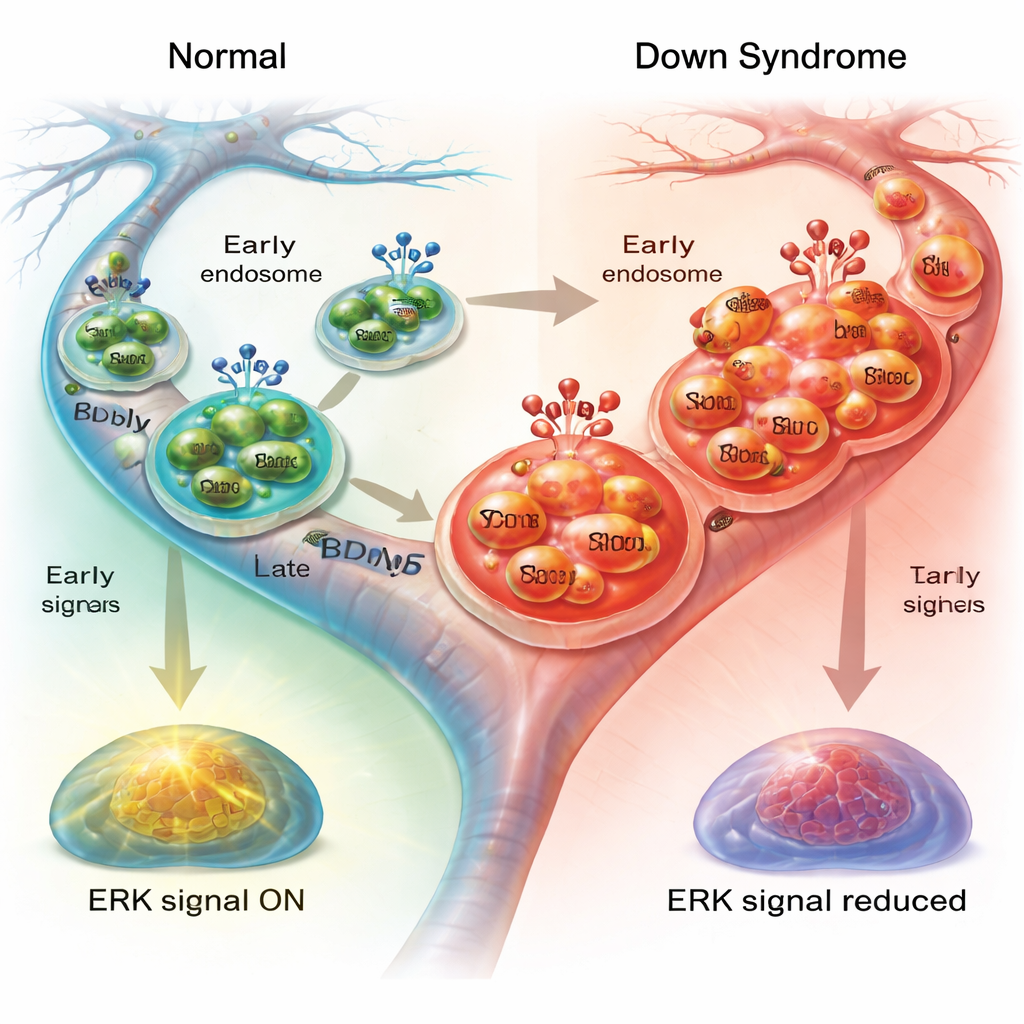
Des signaux intracellulaires atténués
Pour que ces vésicules mobiles soutiennent la santé neuronale, elles doivent activer des voies de signalisation internes une fois arrivées à destination. Une voie clé implique ERK1/2, une paire d’enzymes qui relaie le message du BDNF vers le noyau et aide à réguler le cytosquelette et la machinerie de transport de la cellule. Lorsque les chercheurs ont mesuré l’activation d’ERK1/2 après un traitement au BDNF, ils ont observé une hausse nette dans les neurones normaux mais une réponse beaucoup plus faible dans les neurones de trisomie 21, en particulier dans les axones. Le blocage d’ERK1/2 dans des neurones sains reproduisait partiellement le transport ralenti observé dans les cellules de trisomie 21, ralentissant les endosomes et augmentant leurs pauses. En revanche, le blocage d’ERK1/2 avait peu d’effet supplémentaire dans les neurones de trisomie 21, cohérent avec une signalisation déjà atténuée.
Ce que cela signifie pour le vieillissement cérébral dans la trisomie 21
Pris ensemble, les résultats suggèrent un problème auto-renforçant dans des neurones vulnérables : Rab5 est hyperactif, les endosomes précoces gonflent et les complexes BDNF–TrkB se retrouvent piégés dans des compartiments qui ne se déplacent pas efficacement. En conséquence, moins de signaux de croissance atteignent le corps cellulaire, la signalisation ERK1/2 est affaiblie et la machinerie qui alimente le transport longue distance est encore plus compromise. Au fil des années, ce système de communication défaillant pourrait contribuer à la perte précoce et sévère des neurones du télencéphale basal observée chez les personnes atteintes de la maladie d’Alzheimer associée à la trisomie 21. En mettant en lumière ce lien entre le « contrôle du trafic » endosomal et la signalisation des facteurs de croissance, l’étude ouvre la voie à de nouvelles idées thérapeutiques visant à normaliser l’activité de Rab5, restaurer la fonction des endosomes et renforcer les réponses au BDNF pour protéger ces neurones essentiels.
Citation: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Mots-clés: trisomie 21, maladie d’Alzheimer, BDNF, transport axonal, endosomes