Clear Sky Science · fr
La signalisation endothéliale IRE1 maintient l’intégrité de la barrière hémato‑encéphalique et limite la neuro‑inflammation après un traumatisme crânien
Pourquoi protéger la paroi interne du cerveau est important
Après un coup à la tête, les dommages immédiats ne racontent qu’une partie de l’histoire. Dans les heures et les jours qui suivent, le cerveau déclenche une puissante réponse de stress et immunitaire qui peut prolonger silencieusement la lésion. Cette étude explore comment un petit système de détection du stress à l’intérieur des cellules qui tapissent les vaisseaux sanguins cérébraux contribue à maintenir la paroi interne du cerveau — la barrière hémato‑encéphalique — étanche et calme après un traumatisme crânien. Comprendre cette défense cachée pourrait indiquer de nouvelles voies thérapeutiques pour limiter les incapacités persistantes après un traumatisme crânien.
Les gardiens du cerveau sous stress
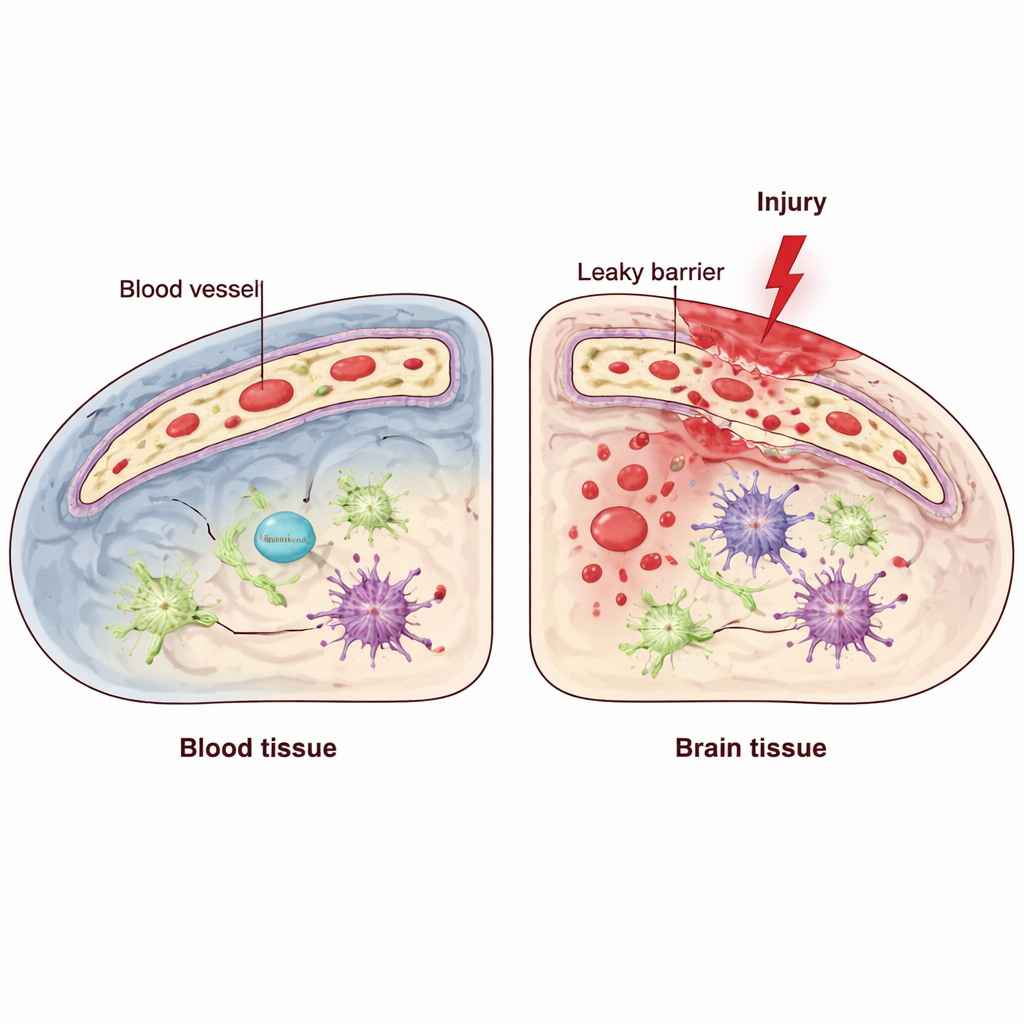
Le cerveau dépend d’une barrière spécialisée formée par les cellules endothéliales, qui tapissent l’intérieur des vaisseaux et contrôlent strictement ce qui peut passer du sang au tissu cérébral. Le traumatisme crânien (TCC) peut perturber cette barrière hémato‑encéphalique, permettant à des molécules inflammatoires et à des cellules immunitaires d’affluer et d’aggraver les lésions. À l’intérieur de ces cellules endothéliales se trouve un système de contrôle de la qualité appelé réponse aux protéines mal repliées (unfolded protein response), qui aide les cellules à faire face au stress au niveau du réticulum endoplasmique. L’un de ses composants clés, nommé IRE1, agit comme capteur et régulateur lorsque les cellules sont sous pression. Les chercheurs se sont demandé : ce capteur de stress endothélial défend‑il la barrière après un TCC, ou aggrave‑t‑il la situation ?
Désactiver un capteur cellulaire dans les cellules des vaisseaux
Pour le savoir, l’équipe a utilisé des souris génétiquement modifiées dans lesquelles IRE1 pouvait être désactivé de manière sélective uniquement dans les cellules endothéliales. Ils ont ensuite provoqué une lésion contrôlée dans la zone motrice du cortex, reproduisant certains aspects du TCC humain, et comparé ces animaux à leurs congénères normaux. Ils ont évalué la motricité avec des tâches mesurant l’équilibre et le placement précis des pattes, et examiné le tissu cérébral par microscopie haute résolution et techniques moléculaires. Chez les souris normales, l’activité d’IRE1 augmentait dans les cellules des vaisseaux proches de la lésion peu après le traumatisme, suggérant que les cellules endothéliales détectent et répondent rapidement au stress. Lorsque IRE1 était absent spécifiquement dans ces cellules, les animaux obtenaient de moins bons résultats aux tests moteurs, indiquant une récupération fonctionnelle altérée.
Vaisseaux qui fuient, plus de cellules immunitaires et neurones mourants
Les chercheurs ont ensuite examiné la résistance de la barrière hémato‑encéphalique. Normalement, de grosses protéines sanguines comme les anticorps restent à l’intérieur des vaisseaux. Après un TCC, une certaine fuite est attendue près de la lésion, mais les souris dépourvues d’IRE1 endothélial présentaient une infiltration beaucoup plus étendue de ces protéines dans le cerveau. La microscopie a révélé qu’une molécule de jonction clé, la VE‑cadherine, qui aide à sceller les cellules endothéliales entre elles, était réduite dans la zone lésée lorsque IRE1 faisait défaut, même si le nombre total de vaisseaux paraissait similaire. Cette perméabilité accrue s’accompagnait d’un afflux de cellules immunitaires dans le cerveau autour de la lésion et de niveaux plus élevés de signaux inflammatoires. Dans ces mêmes régions, les neurones montraient davantage de signes de dégénérescence et d’apoptose, et la zone de tissu endommagé entourant le cœur de la lésion était visiblement plus étendue.
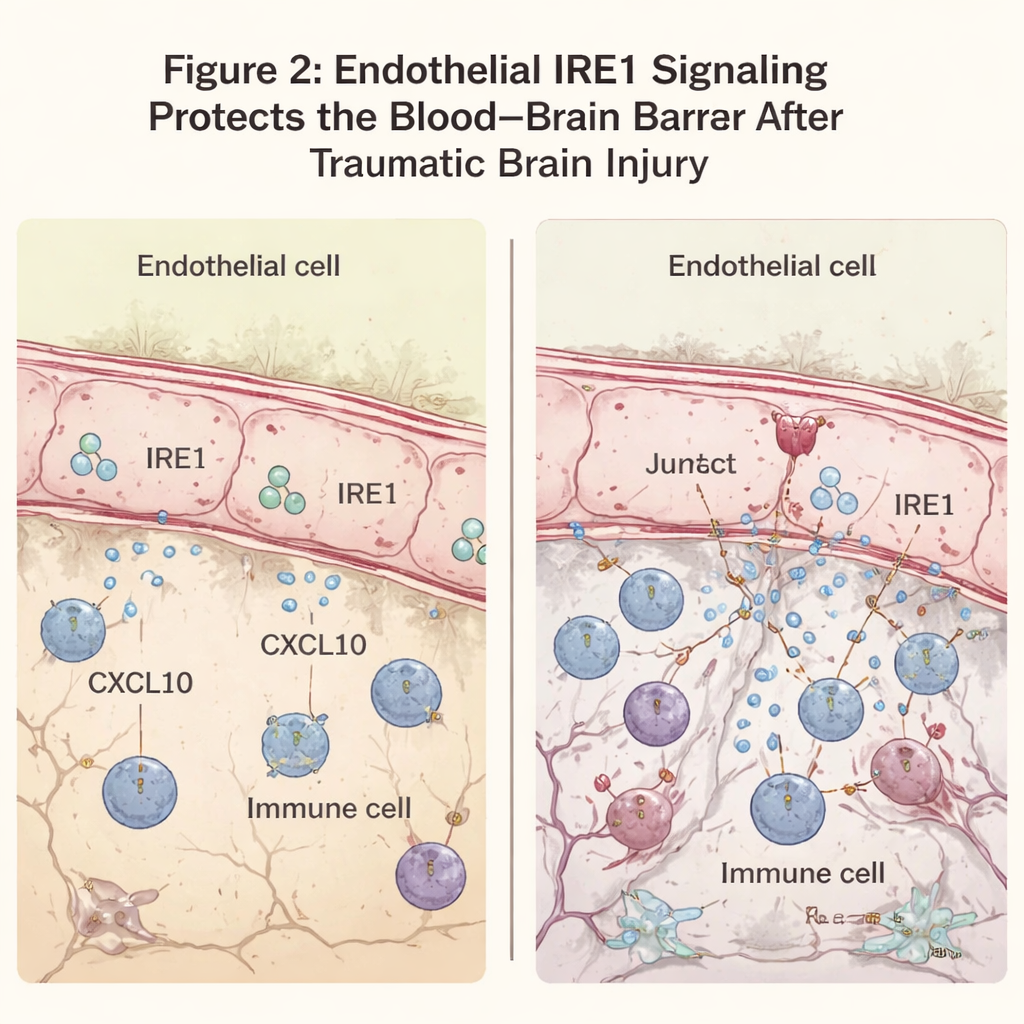
Un médicament anti‑stress calme la tempête de signaux
Pour comprendre les mécanismes moléculaires, l’équipe a analysé les gènes activés après la lésion. Chez les souris sans IRE1 endothélial, les gènes impliqués dans les réponses antivirales et inflammatoires étaient fortement augmentés. Parmi eux se distinguait CXCL10, une chimiokine — une sorte de signal moléculaire — qui attire les cellules immunitaires et peut fragiliser davantage la barrière. CXCL10 était particulièrement élevé dans les cellules endothéliales proches de la lésion en l’absence d’IRE1. Dans des cultures de cellules endothéliales cérébrales exposées à un déclencheur inflammatoire, réduire le stress du réticulum endoplasmique avec un médicament appelé TUDCA a abaissé à la fois l’activité d’IRE1 et la production de CXCL10. Administré aux souris blessées, le TUDCA a réduit CXCL10 et les marqueurs cellulaires immunitaires dans le cortex endommagé et amélioré les performances motrices, suggérant qu’atténuer cette voie de stress peut limiter les lésions secondaires.
Ce que cela signifie pour les personnes victimes de traumatismes crâniens
En bref, ce travail suggère que le capteur de stress IRE1, présent dans les cellules qui tapissent les vaisseaux sanguins du cerveau, agit comme un gardien après un traumatisme crânien. Lorsqu’il est présent et fonctionnel, il aide à maintenir la barrière hémato‑encéphalique étanche, réduit la libération de signaux chimiques qui attirent les cellules immunitaires et limite la propagation de l’inflammation et la perte neuronale autour de la lésion. Lorsqu’il est désactivé, la barrière devient plus perméable, les cellules immunitaires affluent et davantage de tissu cérébral est endommagé. Parce que les cellules vasculaires sont relativement accessibles aux médicaments circulant dans le sang, cibler leurs réponses au stress — avec des composés comme le TUDCA ou des thérapies futures plus ciblées — pourrait devenir une stratégie pratique pour réduire les séquelles à long terme après un traumatisme crânien.
Citation: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Mots-clés: traumatisme crânien, barrière hémato‑encéphalique, cellules endothéliales, neuro‑inflammation, stress cellulaire