Clear Sky Science · fr
CD36 augmente la sensibilité des cellules du cancer du sein triple négatif à la ferroptose induite par le palmitate
Pourquoi la graisse autour des tumeurs peut être à la fois amie et ennemie
Les tumeurs mammaires se développent dans un tissu naturellement riche en graisses, et l’on sait que les cellules cancéreuses « se nourrissent » d’acides gras voisins. Cette étude explore un retournement surprenant : dans certaines conditions, l’un des lipides les plus répandus dans l’organisme, l’acide palmitique, peut en fait contribuer à tuer une forme particulièrement agressive de cancer du sein en déclenchant un type spécifique de mort cellulaire. Comprendre ce mécanisme pourrait indiquer de nouvelles pistes thérapeutiques pour des patientes qui disposent aujourd’hui de peu d’options.
Un cancer du sein difficile à traiter sous la loupe
Le cancer du sein triple négatif (CSTN) est dépourvu des récepteurs hormonaux et des récepteurs de facteurs de croissance ciblés par de nombreux traitements modernes, ce qui en fait l’un des types de cancer du sein les plus difficiles à soigner. Ces tumeurs vivent en étroite proximité avec des adipocytes, qui libèrent d’importantes quantités d’acides gras, dont le gras saturé l’acide palmitique. Les auteurs ont voulu savoir si l’acide palmitique se contente d’alimenter la tumeur ou s’il crée aussi une faiblesse exploitable pour tuer les cellules cancéreuses.
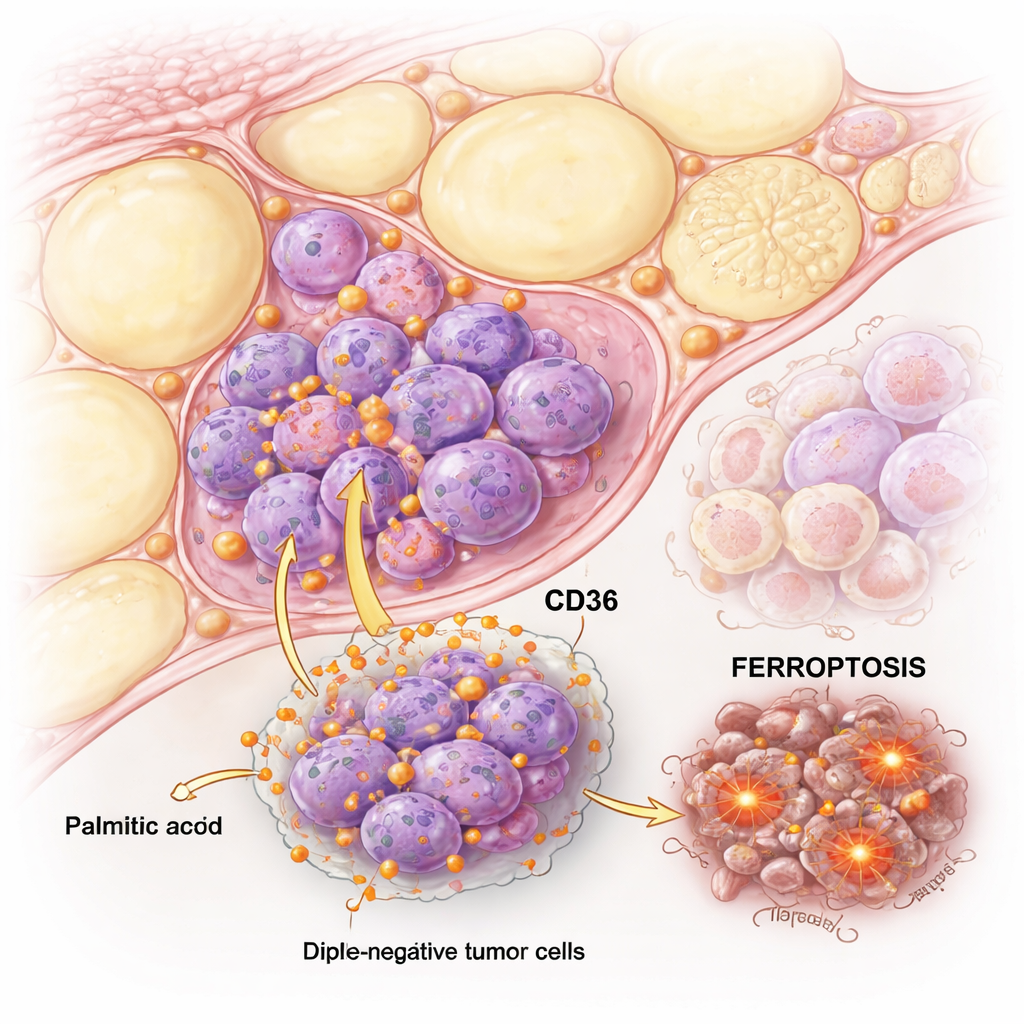
Quand l’acide palmitique pousse les cellules cancéreuses au-delà du seuil
L’équipe a comparé des cellules de CSTN avec des cellules de cancer du sein « luminal » sensibles aux hormones et les a exposées à des doses croissantes d’acide palmitique. Les deux types de cellules pouvaient être endommagés par des fortes concentrations, mais les cellules de CSTN étaient bien plus sensibles. Des tests détaillés ont montré que dans les cellules luminales l’acide palmitique déclenchait principalement l’apoptose classique, une forme ordonnée de mort cellulaire. Dans les cellules de CSTN, en revanche, l’acide palmitique induisait à la fois l’apoptose et une autre voie moins familière appelée ferroptose, dépendante du fer et de la destruction des lipides des membranes cellulaires.
Une porte d’entrée pour les acides gras nommée CD36
Pour comprendre pourquoi les cellules de CSTN réagissaient si différemment, les chercheurs se sont penchés sur CD36, une protéine de surface agissant comme une porte d’entrée pour les acides gras à longue chaîne. Les cellules de CSTN exprimaient naturellement beaucoup plus de CD36 que les cellules luminales, et l’exposition à l’acide palmitique augmentait encore l’expression de CD36. Cela signifiait que les cellules de CSTN importaient davantage d’acide palmitique, accumulaient plus de lipides endommagés, produisaient davantage d’espèces réactives oxygénées dans leurs mitochondries et accumulaient plus de fer libre à l’intérieur de la cellule — autant de signaux clés de la ferroptose. Lorsque CD36 était bloqué par un médicament ou réduit par des outils génétiques, la ferroptose induite par l’acide palmitique diminuait fortement.
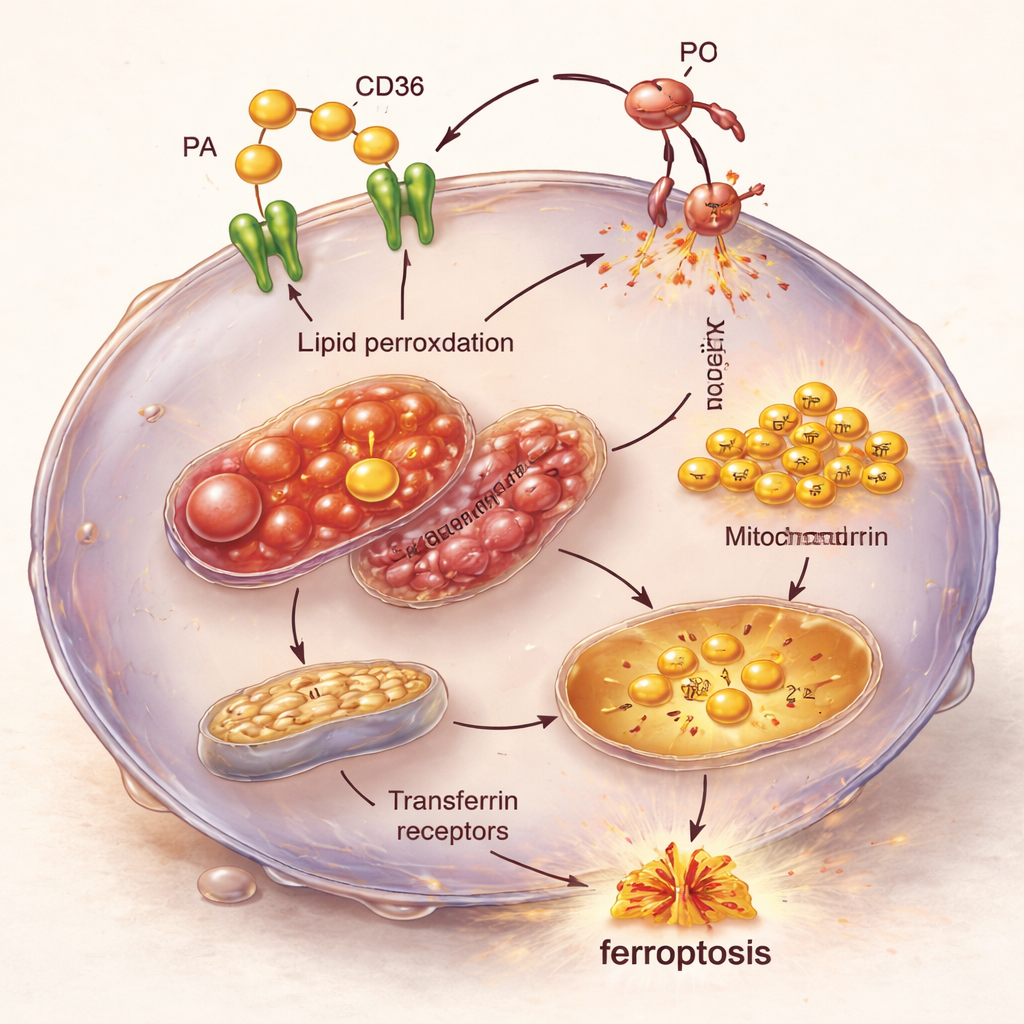
Zoom sur la réaction en chaîne à l’intérieur de la cellule
La microscopie et les analyses d’activité génique ont révélé la réaction en chaîne interne à l’origine de cette vulnérabilité. Les cellules de CSTN surchargées en acide palmitique et en CD36 présentaient des mitochondries gonflées et structurellement endommagées et des niveaux croissants de fer apporté via les récepteurs de la transferrine. Parallèlement, des gènes favorisant la ferroptose étaient activés, tandis que des gènes protégeant normalement contre cette forme de mort cellulaire étaient réprimés. Le résultat est une tempête parfaite : surcharge lipidique, plus de fer disponible pour conduire des réactions chimiques et défense affaiblie contre les dommages lipidiques, poussant ensemble les cellules de CSTN vers la ferroptose.
Quels patients pourraient en bénéficier le plus ?
Le cancer n’est pas uniforme, même au sein du CSTN. À partir d’échantillons tumoraux cultivés chez la souris et de larges bases de données de patientes, les auteurs ont trouvé que CD36 était particulièrement élevé dans un sous-type de CSTN appelé luminal récepteur aux androgènes (LAR), déjà noté comme plus sensible à la ferroptose. D’autres sous-types de CSTN présentant une forte captation de fer montraient également tendance à exprimer davantage de CD36. Ce profil suggère que CD36 pourrait servir de marqueur pour identifier les patientes dont les tumeurs sont naturellement prédisposées aux thérapies basées sur la ferroptose.
Transformer un lipide courant en allié thérapeutique
En termes simples, ce travail montre qu’un lipide abondant dans l’alimentation et l’organisme, l’acide palmitique, peut contribuer à tuer certaines cellules de cancer du sein triple négatif lorsqu’elles expriment des niveaux élevés du transporteur de lipides CD36. En provoquant une surcharge lipidique, une accumulation de fer et des dommages aux membranes cellulaires, CD36 rend ces cellules cancéreuses plus susceptibles de subir la ferroptose, un sort destructeur dont elles ne peuvent s’échapper. Si des traitements futurs peuvent stimuler en toute sécurité cette voie — ou la combiner avec des médicaments qui affaiblissent encore davantage les défenses des cellules —, les cliniciens pourraient transformer une faiblesse métabolique en une nouvelle façon plus ciblée d’attaquer certains des tumeurs mammaires les plus agressives.
Citation: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Mots-clés: cancer du sein triple négatif, ferroptose, CD36, acide palmitique, métabolisme tumoral