Clear Sky Science · fr
La déubiquitination médiée par USP30 de l’hexokinase 2 contrôle le destin métabolique du glucose et la progression tumorale
Comment les cellules cancéreuses réorientent leur usage du sucre
Les cellules cancéreuses sont réputées pour leur « dent sucrée » : elles brûlent le sucre de façons inhabituelles pour alimenter une croissance rapide. Cette étude révèle un nouvel interrupteur, une protéine appelée USP30, qui aide les cellules tumorales à décider comment utiliser le glucose. En modulant une autre protéine, l’hexokinase 2 (HK2), USP30 peut pousser les cellules cancéreuses à consommer davantage de sucre et à croître plus vite, ce qui désigne une nouvelle cible potentielle pour de futurs médicaments anticancéreux. 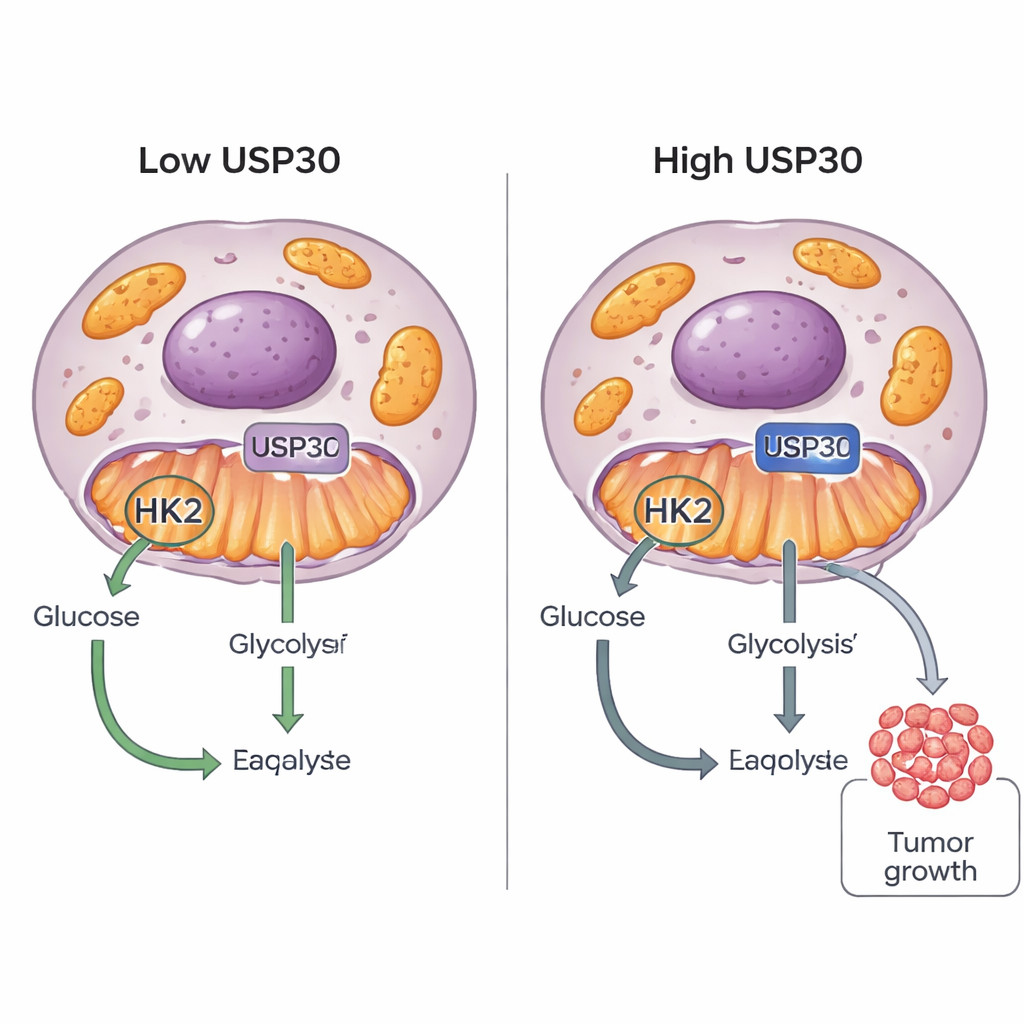
Un mode de vie affamé de sucre au sein des tumeurs
La plupart des cellules saines extraient l’énergie des nutriments de manière efficace, mais de nombreuses cellules cancéreuses privilégient une voie rapide et peu économe appelée glycolyse aérobique, aussi connue sous le nom d’effet Warburg. Elles font entrer de grandes quantités de glucose et le convertissent rapidement en lactate, même lorsque l’oxygène est abondant. Cette stratégie ne sert pas seulement à produire de l’énergie : elle fournit des éléments de construction pour l’ADN, les lipides et les protéines, aide les tumeurs à survivre au stress et peut même affaiblir les attaques du système immunitaire. À la porte d’entrée de cette voie se trouve l’hexokinase, une enzyme qui marque le glucose entrant par l’ajout d’un groupe phosphate, l’engageant ainsi dans la dégradation et la chimie favorisant la croissance.
Une enzyme mitochondriale qui monte sur le devant de la scène
USP30 est une enzyme située à la surface externe des mitochondries, les centrales énergétiques de la cellule. Elle appartient à une famille de « déubiquitinases » qui retirent de petites étiquettes protéiques appelées ubiquitine d’autres protéines, modifiant souvent leur stabilité, leur localisation ou leur activité. USP30 était déjà connue pour des rôles dans les cellules cérébrales et pour le contrôle de la qualité mitochondriale, mais son impact sur le cancer restait flou. En explorant de larges bases de données génomiques tumorales, les chercheurs ont remarqué que les tumeurs présentant des niveaux élevés de USP30 avaient tendance à afficher des signatures de combustion du glucose plus marquées et des signatures de combustion des lipides plus faibles, suggérant que USP30 pourrait aider les cancers à basculer vers un mode de vie alimenté par le sucre.
Relier USP30 aux gardiens du sucre de la cellule
Pour sonder ce lien, l’équipe a réduit ou supprimé USP30 dans plusieurs lignées cellulaires cancéreuses et mesuré leur métabolisme. À l’aide d’instruments qui suivent en temps réel la production d’acide et la consommation d’oxygène, ils ont constaté que la perte de USP30 réduisait fortement à la fois la glycolyse et la respiration mitochondriale. La production de lactate et la consommation de glucose ont diminué, montrant que le moteur de combustion du sucre des cellules avait ralenti. Une série d’expériences de spectrométrie de masse a ensuite révélé que USP30 interagit physiquement avec plusieurs enzymes liées au métabolisme du glucose, en particulier les hexokinases HK1 et HK2. Des tests complémentaires ont montré que cette interaction dépend de l’activité catalytique de USP30 et se produit directement, et non via des partenaires indirects.
Une prise moléculaire précise sur l’hexokinase 2
En approfondissant, les chercheurs ont découvert qu’USP30 retire des types spécifiques de chaînes d’ubiquitine — des liaisons dites atypiques — sur HK1 et HK2. Pour HK2, cet éditing a lieu sur un seul acide aminé crucial, la lysine 144 (K144). Lorsque K144 est mutée de façon à ne plus pouvoir transporter d’ubiquitine, HK2 devient plus stable, se lie plus fortement à une protéine de canal appelée VDAC1 sur les mitochondries et présente une activité enzymatique plus élevée. Des cellules génétiquement modifiées pour porter cette mutation K144 ont envoyé davantage de HK2 vers les mitochondries, consommé plus de glucose, libéré plus de lactate et montré une croissance et une mobilité accrues en culture. Chez la souris, des tumeurs issues de cellules portant HK2 mutant K144 ont grandi plus grandes et plus vite que celles avec HK2 normal, soulignant la puissance de ce petit interrupteur moléculaire. 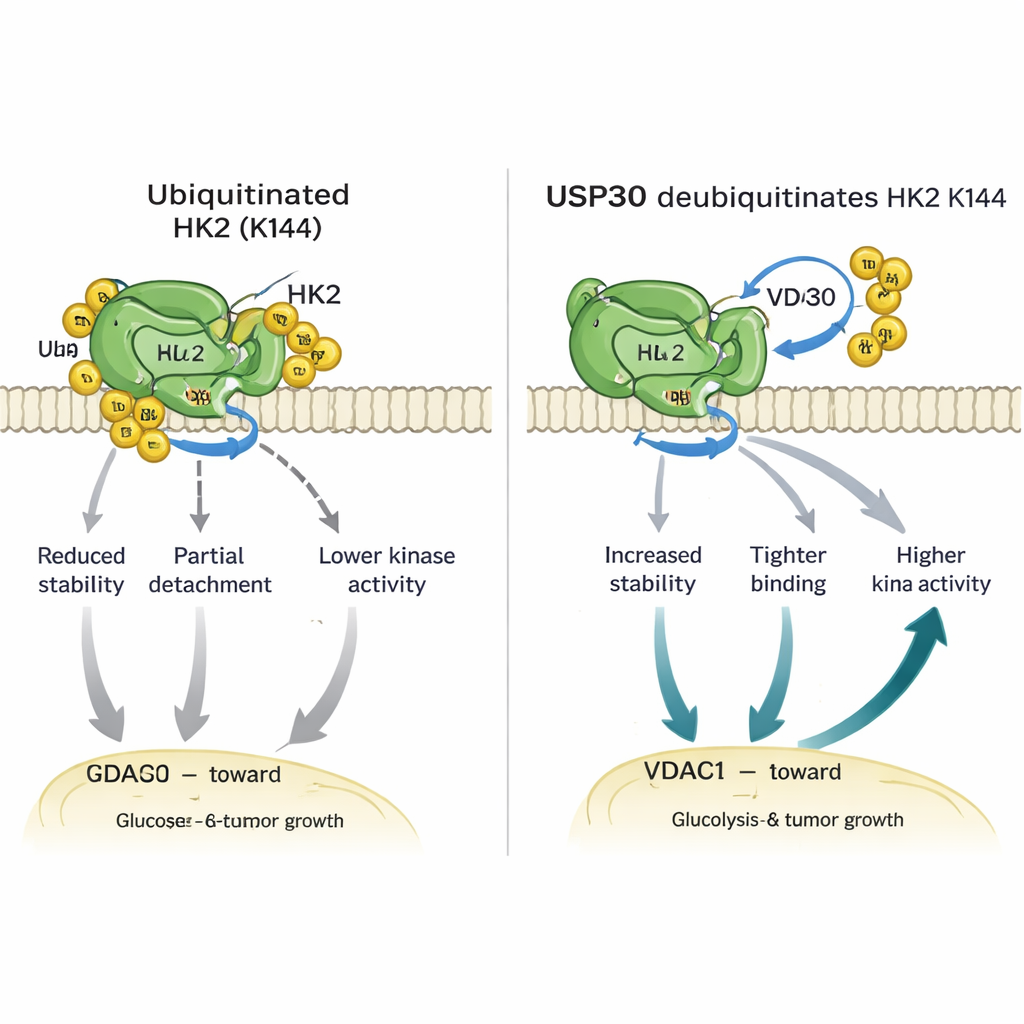
Transformer un commutateur métabolique en avantage de croissance
Ces résultats cartographient une chaîne d’événements claire : USP30 se lie à HK2, enlève les étiquettes d’ubiquitine sur K144 et, ce faisant, maintient HK2 actif et ancré sur les mitochondries. Cela stimule la glycolyse, alimente la division et la migration des cellules tumorales et accélère finalement la croissance tumorale. Lorsque USP30 manque ou est inactif, HK2 devient moins stable et moins efficace, et les cellules cancéreuses perdent une partie de leur avantage métabolique. Pour un non-spécialiste, USP30 agit comme un mécanicien qui garde le moteur sucré de la cellule cancéreuse réglé et fixé — retirez le mécanicien, et le moteur tousse.
Ce que cela signifie pour les traitements anticancéreux futurs
Pour un lecteur non spécialiste, l’idée principale est que les cellules cancéreuses dépendent d’un contrôle fin de la façon dont elles brûlent le sucre, et USP30 constitue un bouton récemment découvert sur ce panneau de contrôle. En stabilisant HK2 en un site spécifique, USP30 aide les tumeurs à maintenir un métabolisme gourmand en glucose et à croître de façon plus agressive. Des médicaments qui bloquent USP30, ou qui perturbent son interaction avec HK2 au niveau de la lysine 144, pourraient fragiliser les tumeurs en privant leur moteur sucré sans nécessairement nuire dans la même mesure aux cellules normales. Ce travail apporte donc une pièce importante au puzzle de la réécriture métabolique du cancer et suggère un nouvel angle prometteur pour des thérapies ciblées.
Citation: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Mots-clés: métabolisme du cancer, glycolyse, hexokinase 2, USP30, effet Warburg