Clear Sky Science · fr
La MLKL dans les cellules parenchymateuses du foie favorise le cancer hépatique dans une maladie hépatique stéatosique associée à un dysfonctionnement métabolique chez la souris
Pourquoi un foie gras peut se transformer en cancer
À mesure que l’obésité et le diabète de type 2 se répandent, un nombre croissant de personnes développe également une affection hépatique grasse et inflammatoire désormais appelée stéatohépatite associée au dysfonctionnement métabolique (MASH). Une partie de ces patients finira par développer un cancer du foie, mais les raisons restent incomplètement comprises. Cette étude examine une protéine nommée MLKL à l’intérieur des cellules hépatiques et pose une question simple aux implications importantes : la MLKL contribue‑t‑elle à faire basculer un foie malade et gras vers le cancer, et l’inhiber pourrait‑il réduire le risque de cancer hépatique ?
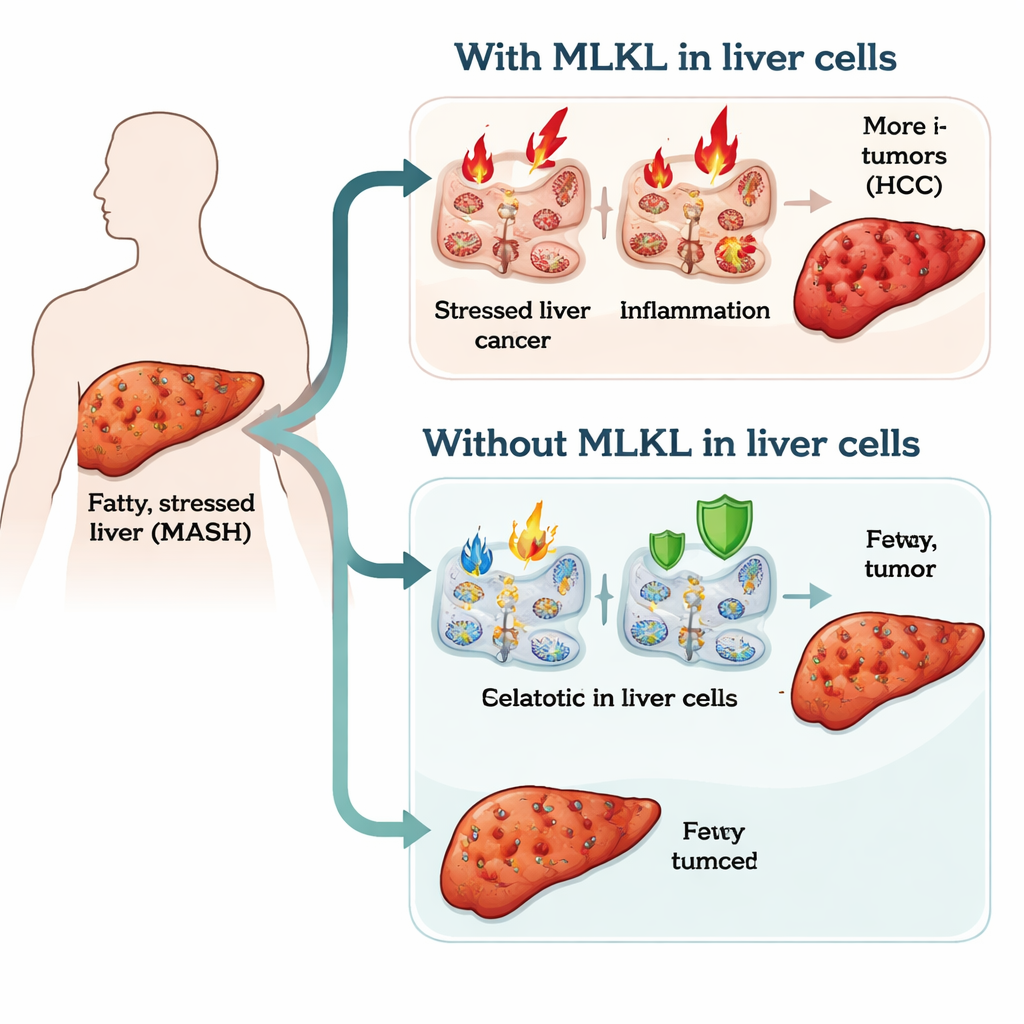
Un examen plus attentif des lésions hépatiques dans une épidémie moderne
Le cancer du foie est aujourd’hui l’un des principaux tueurs parmi les cancers dans le monde, et une grande partie de cette hausse est liée à la maladie hépatique grasse associée à une alimentation déséquilibrée et à des troubles métaboliques. Dans la MASH, les cellules hépatiques sont surchargées de lipides, soumises au stress et entourées d’une inflammation chronique. Sur plusieurs années, cet environnement peut endommager l’ADN et permettre à des cellules mutées de se développer en tumeurs. La protéine MLKL est surtout connue pour déclencher une forme de mort cellulaire violente qui fait éclater les cellules et alimente l’inflammation. Pour cette raison, les chercheurs ont supposé que la MLKL pourrait être un des interrupteurs qui transforment une lésion hépatique durable en cancer du foie manifeste.
Tester le rôle de la MLKL dans un modèle murin de cancer hépatique lié à la stéatose
Pour sonder le rôle de la MLKL, les chercheurs ont mis au point des souris dont la MLKL était spécifiquement supprimée dans les cellules parenchymateuses du foie — principalement les hépatocytes, cellules hépatiques exerçant la majeure partie des fonctions — tout en laissant les autres tissus intacts. Toutes les souris ont été rendues diabétiques peu après la naissance, puis nourries soit avec un régime standard, soit avec un régime riche en graisses et en sucres qui reproduit l’environnement alimentaire responsable de la MASH chez l’humain. Sur 12 semaines, ce régime a provoqué de façon fiable une stéatose hépatique, une fibrose légère et, surtout, des tumeurs hépatiques ressemblant au carcinome hépatocellulaire humain. Cela a permis à l’équipe de comparer directement des souris normales et des souris dépourvues de MLKL dans les cellules hépatiques pour observer le déroulement de la maladie dans chaque cas.
Même foie gras, mais inflammation retardée et moins de tumeurs
De manière surprenante, l’élimination de la MLKL dans les cellules hépatiques n’a pas empêché les stades précoces de la maladie : les deux groupes de souris ont pris du poids de manière comparable, accumulé des lipides dans le foie et développé une fibrose légère similaire. Les différences marquantes sont apparues dans la vitesse d’apparition de l’inflammation et du cancer. Les souris avec une MLKL normale ont présenté une élévation plus précoce des signaux inflammatoires hépatiques, davantage de cellules immunitaires activées dans le foie et la rate, ainsi qu’une splénomégalie — signes d’une forte réponse inflammatoire systémique. En revanche, les souris dépourvues de MLKL dans les cellules hépatiques ont connu une phase inflammatoire retardée et moins de cellules immunitaires fortement activées aux premiers stades. Au fil du temps, cela s’est traduit par moins de tumeurs et de plus petites lésions hépatiques, un taux inférieur de lésions précancéreuses avancées et une incidence nettement réduite de carcinome hépatocellulaire complet.
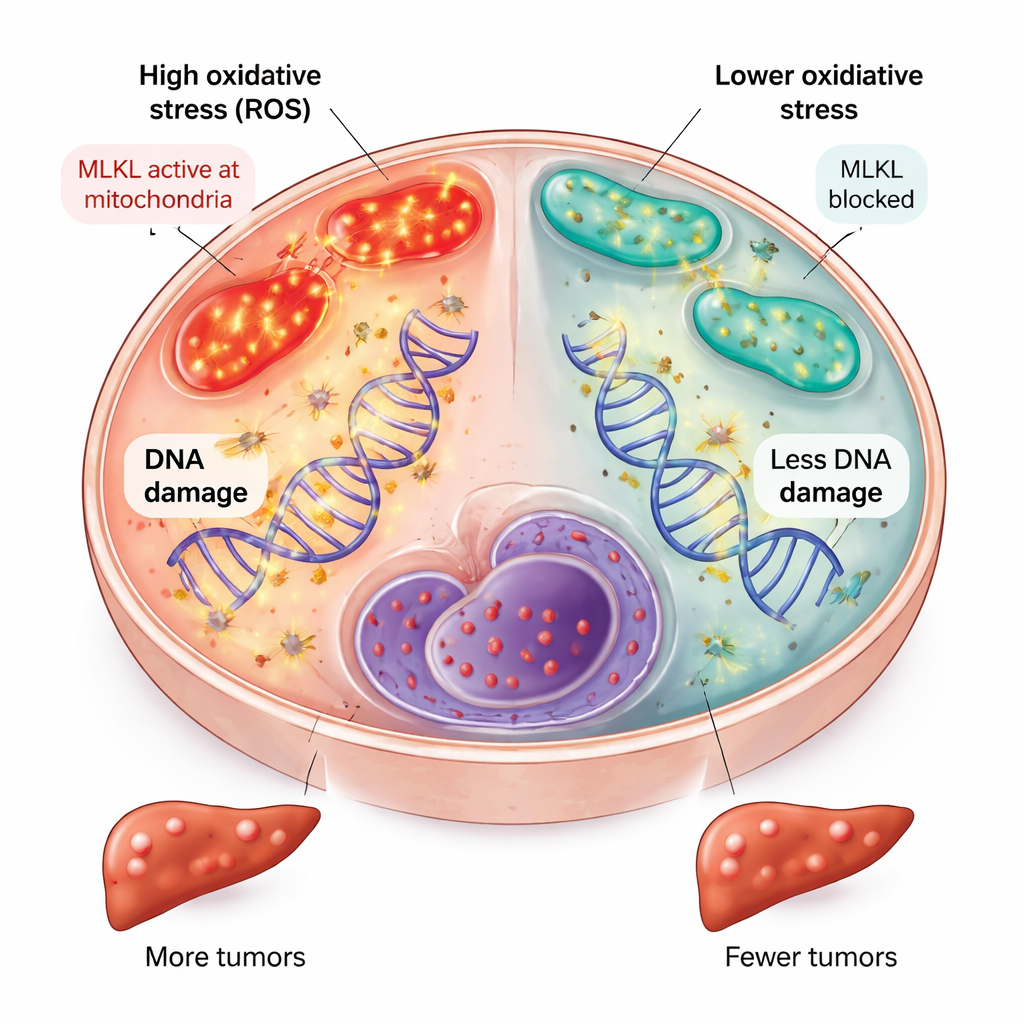
Moins de stress oxydatif et moins de dommages à l’ADN en l’absence de MLKL
L’équipe a ensuite cherché à comprendre pourquoi l’absence de MLKL dans les cellules hépatiques ralentissait le développement du cancer. Ils ont constaté qu’aux premiers stades de la maladie, les foies dépourvus de MLKL présentaient une expression plus faible de gènes induits par le stress oxydatif, des signes biochimiques réduits de stress métabolique dans certaines lipides appelés sphingolipides, et un état plus équilibré du coenzyme Q dans les mitochondries, les centrales énergétiques de la cellule. Ces changements indiquent tous une production moindre d’espèces réactives de l’oxygène. Conformément à cela, les cellules hépatiques sans MLKL accumulaient moins de dommages oxydatifs à l’ADN, comme le montrait une coloration réduite d’un marqueur de dommages dans les noyaux cellulaires. Parce que les dommages oxydatifs persistants à l’ADN sont un moteur clé des mutations favorisant le cancer, l’atténuation de ce stress a probablement contribué à la charge tumorale réduite.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, ces résultats suggèrent que la MLKL présente dans les cellules parenchymateuses du foie agit comme un promoteur discret du cancer hépatique dans le contexte d’une maladie hépatique grasse et inflammatoire. Elle semble le faire non seulement en provoquant la mort cellulaire, mais aussi en perturbant l’équilibre mitochondrial, en augmentant le stress oxydatif et en contribuant au maintien d’une inflammation et de lésions de l’ADN délétères. Pour les patients, le message est que la MLKL pourrait constituer une cible médicamenteuse intéressante : bloquer son activité spécifiquement dans les cellules hépatiques pourrait aider à prévenir ou retarder le cancer du foie lié à la MASH. En parallèle, comme la MLKL joue d’autres rôles utiles dans les cellules immunitaires, toute thérapie future devra être précisément ciblée afin que l’inhibition de cette protéine protège le foie sans affaiblir les défenses générales de l’organisme.
Citation: Imerzoukene, G., Kara-Ali, G.H., Heitz-Marchaland, C. et al. MLKL in liver parenchymal cells promotes liver cancer in murine metabolic dysfunction-associated steatotic liver disease. Cell Death Dis 17, 229 (2026). https://doi.org/10.1038/s41419-026-08458-x
Mots-clés: stéatose hépatique, cancer du foie, inflammation, stress oxydatif, protéine MLKL