Clear Sky Science · fr
Suppression spécifique aux ovocytes des sous-unités d’eIF2 provoquant l’apoptose des ovocytes de souris au sein des follicules en croissance précoce via des dysfonctionnements mitochondriaux et des dommages à l’ADN
Pourquoi la vie des cellules œuf importe
Les femmes naissent avec la totalité des cellules œuf qu’elles auront jamais, stockées dans de minuscules structures de l’ovaire appelées follicules. Lorsque ces follicules sont perdus trop rapidement, les femmes peuvent développer une insuffisance ovarienne prématurée (IOP), un trouble qui conduit à une infertilité précoce et souvent à des symptômes similaires à la ménopause à un âge jeune. Cette étude chez la souris pose une question simple mais cruciale : que se passe-t-il à l’intérieur des ovocytes lorsqu’une étape clé de la synthèse des protéines se dérègle, et comment cela peut-il mener à une perte précoce de fertilité ?
Le commutateur de démarrage des protéines de la cellule
Pour rester en bonne santé, les ovocytes doivent constamment produire les bonnes protéines au bon moment. Une pièce centrale de ce processus est une machine moléculaire en trois parties appelée eIF2, qui aide à lancer la production protéique à partir des messages génétiques. Les chercheurs ont désactivé sélectivement deux des sous-unités d’eIF2, nommées eIF2α et eIF2β, uniquement dans les ovocytes de souris aux premiers stades de croissance folliculaire. Lorsqu’une des sous-unités manquait, les femelles devenaient complètement infertiles. Leurs ovaires étaient plus petits et la progression normale des follicules précoces vers des follicules mûrs relâchant des ovules était largement bloquée, avec beaucoup moins de follicules à chaque stade ultérieur. Au fil du temps, presque tous les follicules étaient épuisés, reproduisant un état sévère ressemblant à une IOP d’apparition précoce.
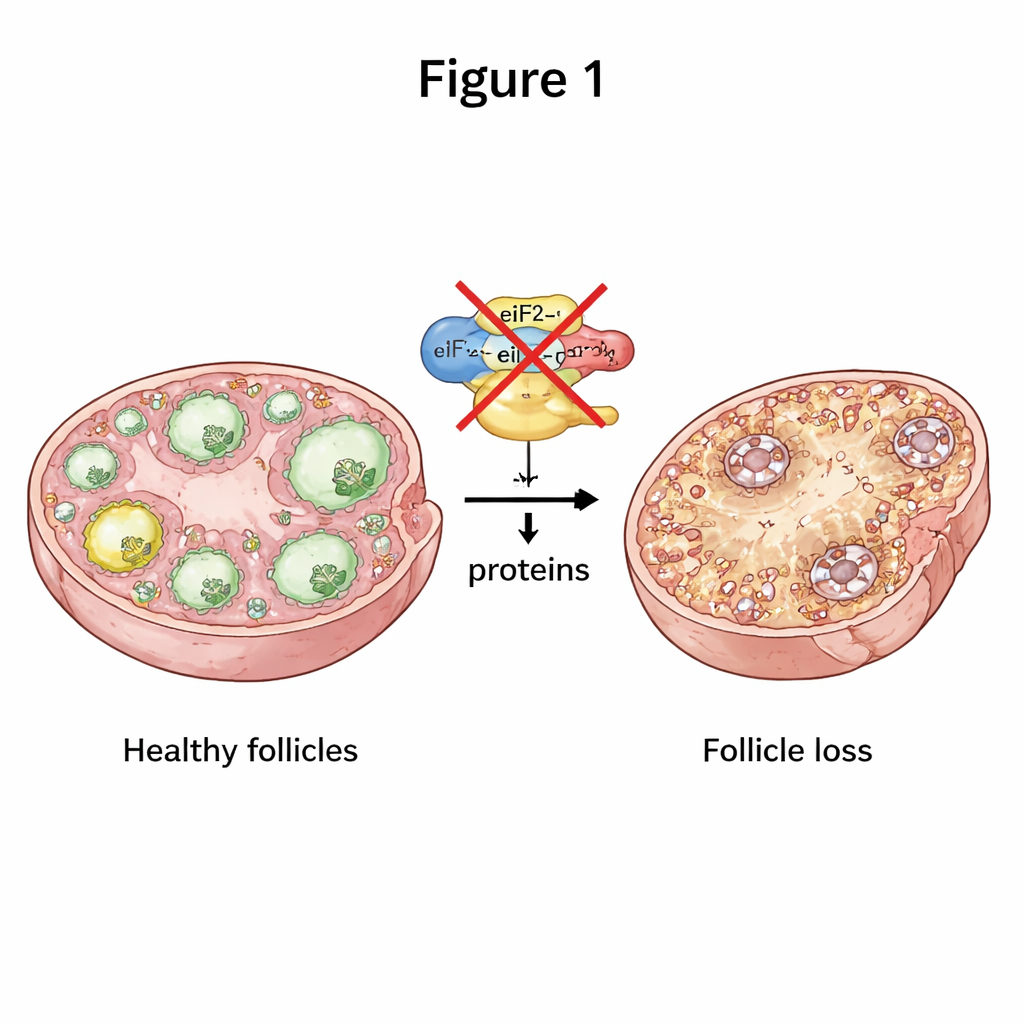
Quand la communication dans l’ovaire se dérègle
Les follicules ne sont pas de simples ovocytes isolés ; ils forment un partenariat étroit entre un ovocyte et les cellules « assistantes » environnantes appelées cellules de la granulosa. L’équipe a constaté qu’en l’absence d’eIF2β, les ovocytes produisaient beaucoup moins de plusieurs protéines de signalisation cruciales qui soutiennent normalement la croissance des cellules de la granulosa et l’apport nutritif. Les ponts physiques entre l’ovocyte et les cellules de la granulosa étaient désorganisés et raccourcis, et les microvillosités à la surface de l’ovocyte apparaissaient atrophiées et endommagées au microscope électronique. Les cellules de la granulosa de ces follicules se divisaient moins et mouraient plus fréquemment. Cette rupture de la communication bidirectionnelle empêchait la croissance normale des follicules, poussant l’ovaire vers la perte folliculaire.
Panne d’énergie dans les « batteries » de l’ovocyte
Les mitochondries, souvent appelées centrales électriques de la cellule, sont particulièrement importantes dans les ovocytes car elles fournissent l’énergie nécessaire à la croissance et au développement embryonnaire ultérieur. Chez les ovocytes déficients en eIF2β, le taux global de synthèse protéique a diminué et de nombreuses protéines liées aux mitochondries étaient réduites. Les mitochondries devenaient anormalement allongées, agglomérées près de la surface cellulaire, et montraient une moindre potentialité de membrane, des niveaux d’énergie (ATP) plus faibles et moins de copies d’ADN mitochondrial. Parallèlement, les cellules accumulaient des niveaux élevés d’espèces réactives de l’oxygène (ROS), des molécules oxygénées agressives susceptibles d’endommager les composants cellulaires. Ensemble, ces changements révèlent un effondrement profond de la dynamique et de la fonction mitochondriales.
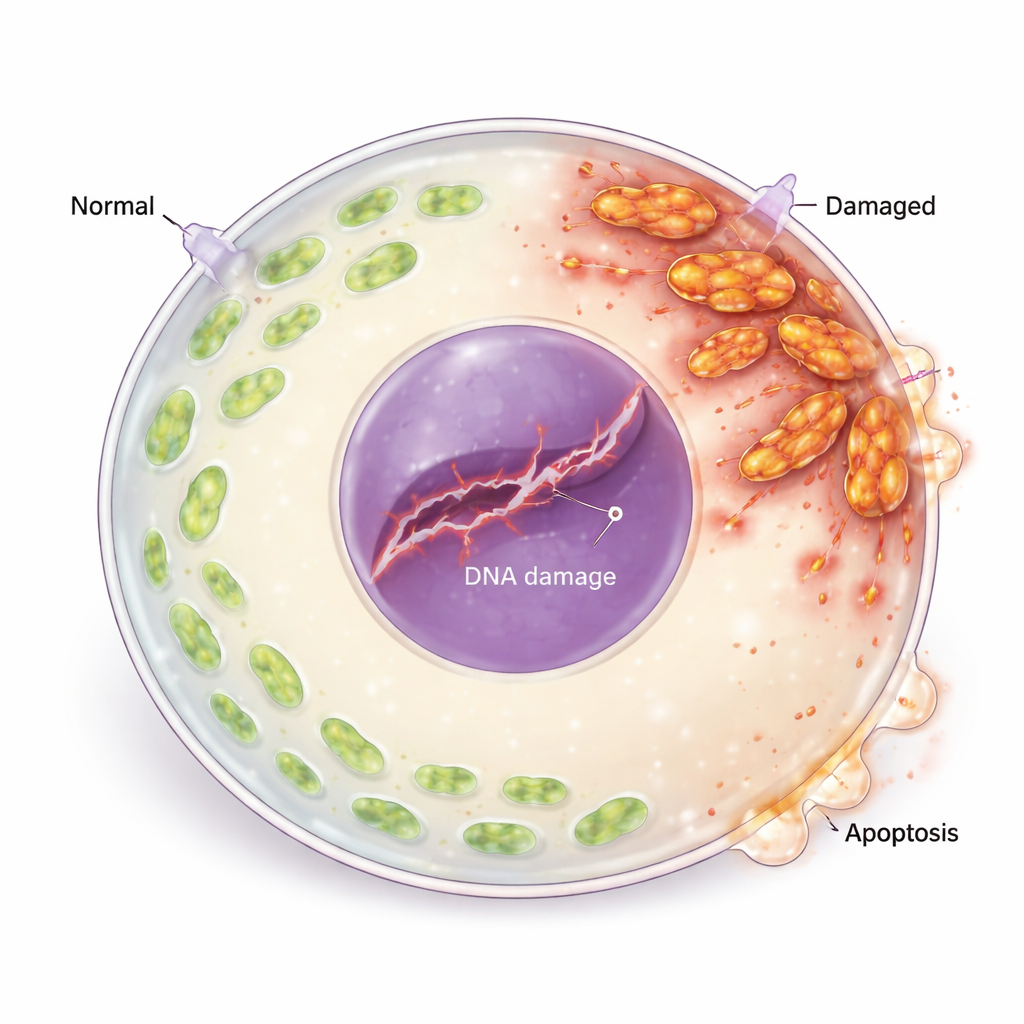
Du stress oxydatif aux lésions de l’ADN et à la mort cellulaire
L’excès de ROS n’endommageait pas que les mitochondries ; il affectait aussi le matériel génétique de l’ovocyte. Les chercheurs ont observé une augmentation des marqueurs de bris d’ADN et l’activation des voies de réponse aux dommages de l’ADN, y compris des protéines qui détectent et signalent les lésions génétiques. Une protéine clé de réparation était réduite, suggérant que les dommages n’étaient pas efficacement réparés. En aval, l’équilibre des régulateurs de la survie bascula : les protéines pro-apoptotiques augmentèrent tandis que les protéines protectrices diminuèrent, et les ovocytes montraient des signes clairs de mort cellulaire programmée (apoptose). Lorsque l’équipe traita les ovocytes avec un antioxydant (N-acétylcystéine), les niveaux de ROS chutèrent, les marqueurs de dommages à l’ADN et d’apoptose diminuèrent, et la maturation des ovocytes s’améliora, établissant un lien direct entre le stress oxydatif et la perte des ovocytes.
Ce que cela signifie pour l’insuffisance ovarienne précoce
En retraçant les événements partant d’un seul complexe moléculaire (eIF2) jusqu’à une synthèse protéique défaillante, une dégradation mitochondriale, un stress oxydatif, des dommages à l’ADN et enfin la mort des ovocytes, ce travail décrit une chaîne d’événements détaillée pouvant anéantir la réserve ovarienne. L’étude renforce l’idée que des mutations dans des facteurs initiant la traduction, déjà identifiées chez certaines femmes atteintes d’IOP, peuvent directement endommager les ovocytes via cette voie. Elle indique également des pistes potentielles d’intervention : des antioxydants, des modulateurs de la réponse au stress, ou des traitements protégeant les follicules précoces (comme l’hormone anti-Müllérienne, qui a partiellement préservé les follicules dormants chez ces souris) pourraient un jour aider à préserver la fertilité chez des patientes dont les ovaires sont vulnérables à des stress similaires.
Citation: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Mots-clés: insuffisance ovarienne prématurée, apoptose des ovocytes, dysfonction mitochondriale, traduction protéique, espèces réactives de l’oxygène