Clear Sky Science · fr
Les hépatocytes diploïdes résistent aux lésions hépatiques induites par l’acétaminophène grâce à une signalisation JNK atténuée
Pourquoi certains foies supportent mieux les surdoses
L’acétaminophène (paracétamol) se trouve dans d’innombrables trousses de secours, et pourtant en prendre trop est une cause majeure d’insuffisance hépatique aiguë. Cette étude pose une question apparemment simple mais aux implications fortes : toutes les cellules hépatiques réagissent-elles de la même façon à une surdose ? Les chercheurs montrent qu’un type particulier de cellule hépatique, appelé hépatocyte diploïde, survit et répare étonnamment bien les dégâts après une surdose d’acétaminophène, grâce à une voie de stress interne atténuée.
Deux types de cellules hépatiques, deux destins différents
Le foie est atypique parce que la plupart de ses cellules actives (les hépatocytes) portent des jeux de chromosomes supplémentaires, les rendant polyploïdes. Une fraction plus petite reste diploïde, avec seulement deux jeux de chromosomes comme la plupart des cellules du corps. Les scientifiques savaient que ces groupes diffèrent dans leur division et leur régénération, mais leur rôle dans les lésions médicamenteuses restait flou. Les auteurs ont utilisé des souris élevées pour avoir un foie majoritairement composé d’hépatocytes diploïdes mais fonctionnant par ailleurs normalement, et les ont comparées à des souris typiques dont le foie est surtout polyploïde. Les deux groupes ont reçu des doses faibles et élevées d’acétaminophène pour observer la réponse hépatique au fil du temps.
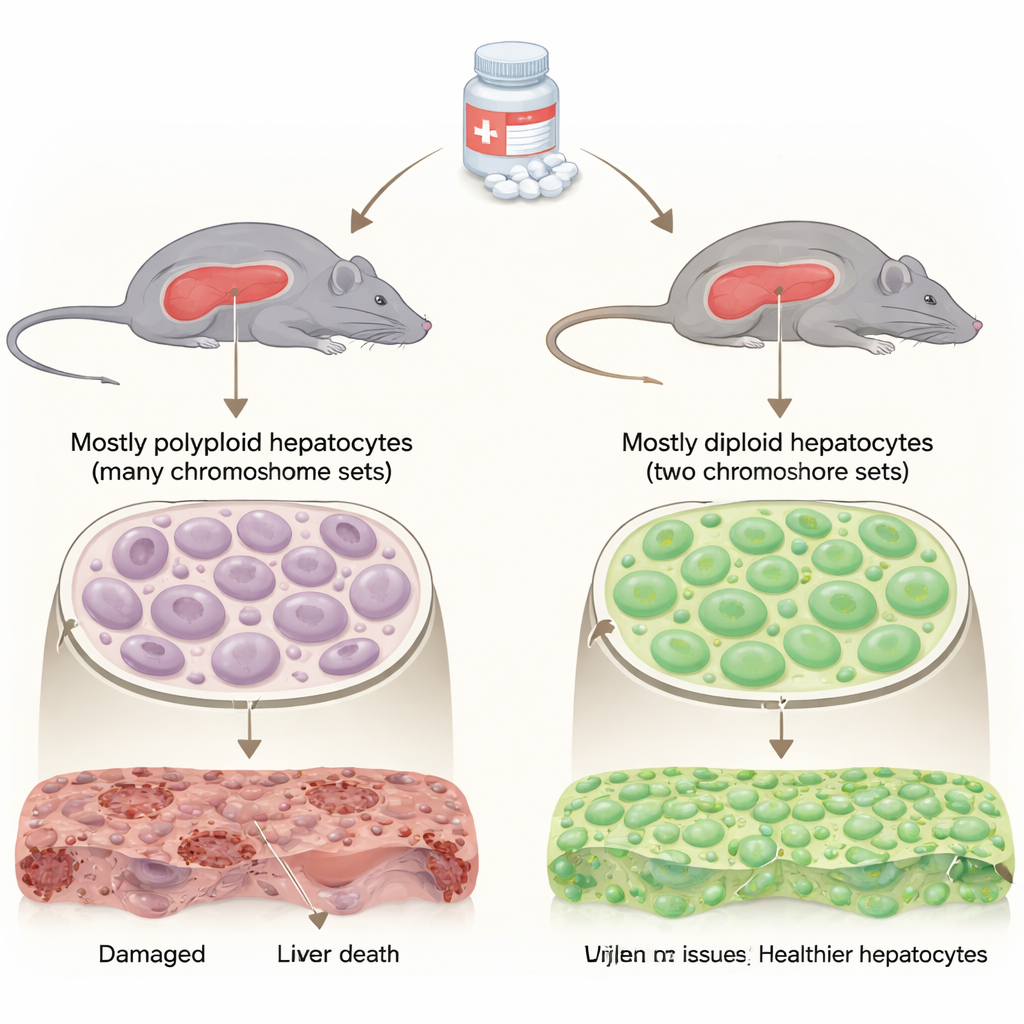
Les foies riches en diploïdes survivent aux surdoses et récupèrent plus vite
Après une « surdose régénératrice » d’acétaminophène, les deux groupes ont montré des lésions hépatiques, mais les souris riches en diploïdes s’en sont nettement mieux sorties. Elles présentaient une survie plus élevée, des niveaux plus faibles d’enzymes hépatiques dans le sang (signe de dommages réduits) et des zones de tissu mort et d’ADN fragmenté plus petites au microscope. Même à une dose plus sévère, dite « non régénératrice » — qui cause habituellement des lésions durables et la mort — plus de la moitié des souris riches en diploïdes ont survécu, contre moins d’une sur dix chez les témoins. Malgré cette protection, les foies à prédominance diploïde n’étaient pas inactifs : ils ont activé plus tôt des protéines de division cellulaire, suggérant qu’ils résistent aux dommages et entament la reconstruction plus rapidement.
Ce n’est pas le médicament, mais le câblage du stress
Une hypothèse évidente était que les foies riches en diploïdes métabolisent simplement l’acétaminophène différemment. L’équipe a mesuré des enzymes clés qui convertissent le médicament en son sous-produit toxique, les niveaux du protecteur glutathion, et la quantité de médicament liée aux protéines hépatiques. Tous étaient similaires entre les deux types de souris, ce qui signifie que les deux produisaient et manipulaient la même quantité de toxine. La différence cruciale est apparue ensuite, dans la manière dont les cellules ont répondu à cette toxine. Dans les foies typiques, riches en polyploïdes, les gènes et protéines impliqués dans le stress cellulaire, les dommages à l’ADN et les lésions mitochondriales étaient fortement activés. Dans les foies riches en diploïdes, ces réponses étaient atténuées et résolues plus rapidement, tandis que les gènes liés à la régénération s’activaient plus tôt.
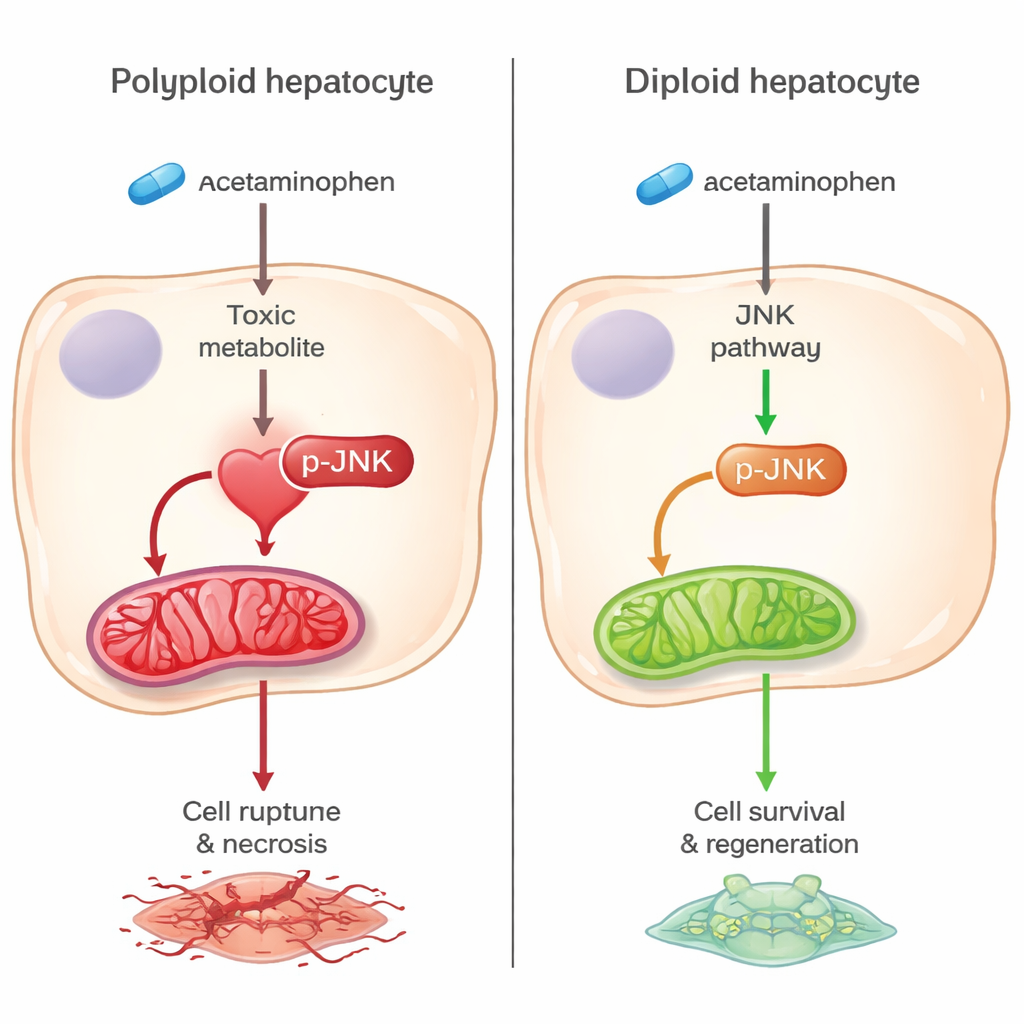
Une voie de mort plus discrète protège les cellules diploïdes
Le protagoniste central de cette différence est une voie de signalisation du stress connue sous le nom de voie JNK. Dans les foies standards, le sous-produit toxique de l’acétaminophène active des enzymes en amont qui déclenchent JNK, lequel migre ensuite vers les mitochondries, les centrales énergétiques de la cellule, provoquant des dommages oxydatifs et la mort cellulaire. Dans les foies riches en diploïdes, l’activation de ces enzymes en amont et de JNK lui-même était fortement réduite, et beaucoup moins de JNK atteignait les mitochondries. Les marqueurs du stress oxydatif et de la dégradation mitochondriale étaient également plus faibles, indiquant que ces organites restaient plus intacts. Fait important, lorsque les mêmes gènes ont été supprimés uniquement dans des foies d’adultes sans modifier la ploïdie cellulaire, il n’y a pas eu de protection, ce qui pointe vers l’abondance d’hépatocytes diploïdes — et non la manipulation génétique elle-même — comme facteur clé.
Pourquoi le type cellulaire compte pour les lésions hépatiques humaines
Pour vérifier si ce schéma se confirme plus généralement, les chercheurs ont exposé en culture des cellules hépatiques de souris normales à l’acétaminophène. Les cellules avec de nombreux jeux de chromosomes (hautement polyploïdes) mouraient plus facilement, tandis que les cellules diploïdes et de faible ploïdie avaient plus de chances de survivre. Globalement, les résultats soutiennent un modèle dans lequel les hépatocytes diploïdes sont les « premiers intervenants » du foie face à une lésion toxique aiguë : ils freinent une voie majeure de mort cellulaire, préservent leurs mitochondries et entrent rapidement en régénération. Les cellules polyploïdes peuvent rester bénéfiques dans d’autres contextes, comme la protection contre le cancer ou l’adaptation à des dommages chroniques à long terme. Mais lors d’une surdose unique, disposer de plus d’hépatocytes diploïdes pourrait faire la différence entre la guérison et l’insuffisance hépatique.
Citation: Wilson, S.R., Delgado, E.R., Alencastro, F. et al. Diploid hepatocytes resist acetaminophen-induced liver injury through suppressed JNK signaling. Cell Death Dis 17, 203 (2026). https://doi.org/10.1038/s41419-026-08448-z
Mots-clés: surdosage d’acétaminophène, lésion hépatique, ploïdie des hépatocytes, signalisation JNK, régénération hépatique