Clear Sky Science · fr
La transglutaminase 2 aggrave la survie du cancer ovarien en inactivant directement GSK3β
Pourquoi cette recherche compte pour la santé des femmes
Le cancer ovarien est l’un des cancers féminins les plus meurtriers car il est souvent détecté tard et récidive fréquemment malgré des chimiothérapies intensives. Cette étude révèle comment une protéine peu connue, la transglutaminase 2 (TGase 2), aide les cellules du cancer ovarien à survivre au traitement et à se disséminer dans l’organisme. En mettant au jour ce complice caché du cancer, les auteurs ouvrent la voie à de nouvelles stratégies pour rendre les traitements existants plus efficaces et ralentir ou empêcher les métastases mortelles.
Un moteur caché au sein des tumeurs agressives
Les cliniciens observent depuis longtemps que de nombreux cancers ovariens deviennent résistants à la chimiothérapie et se diffusent largement dans l’abdomen. Un responsable majeur est un processus appelé transition épithélio-mésenchymateuse (EMT), dans lequel les cellules cancéreuses relâchent leurs connexions, gagnent en mobilité et se comportent davantage comme des « vagabondes » invasives plutôt que comme des cellules tissulaires organisées. Les auteurs montrent que la TGase 2, présente à des niveaux très faibles dans l’ovaire normal mais beaucoup plus élevée dans les tumeurs ovariennes, est fortement liée à ce basculement. Dans un large panel d’échantillons humains, les niveaux de TGase 2 augmentaient progressivement des tumeurs précoces aux stades avancés et métastatiques, et son abondance correspondait étroitement à l’activité de nombreux gènes liés à l’EMT qui contrôlent le mouvement cellulaire, la croissance et la formation de vaisseaux sanguins. 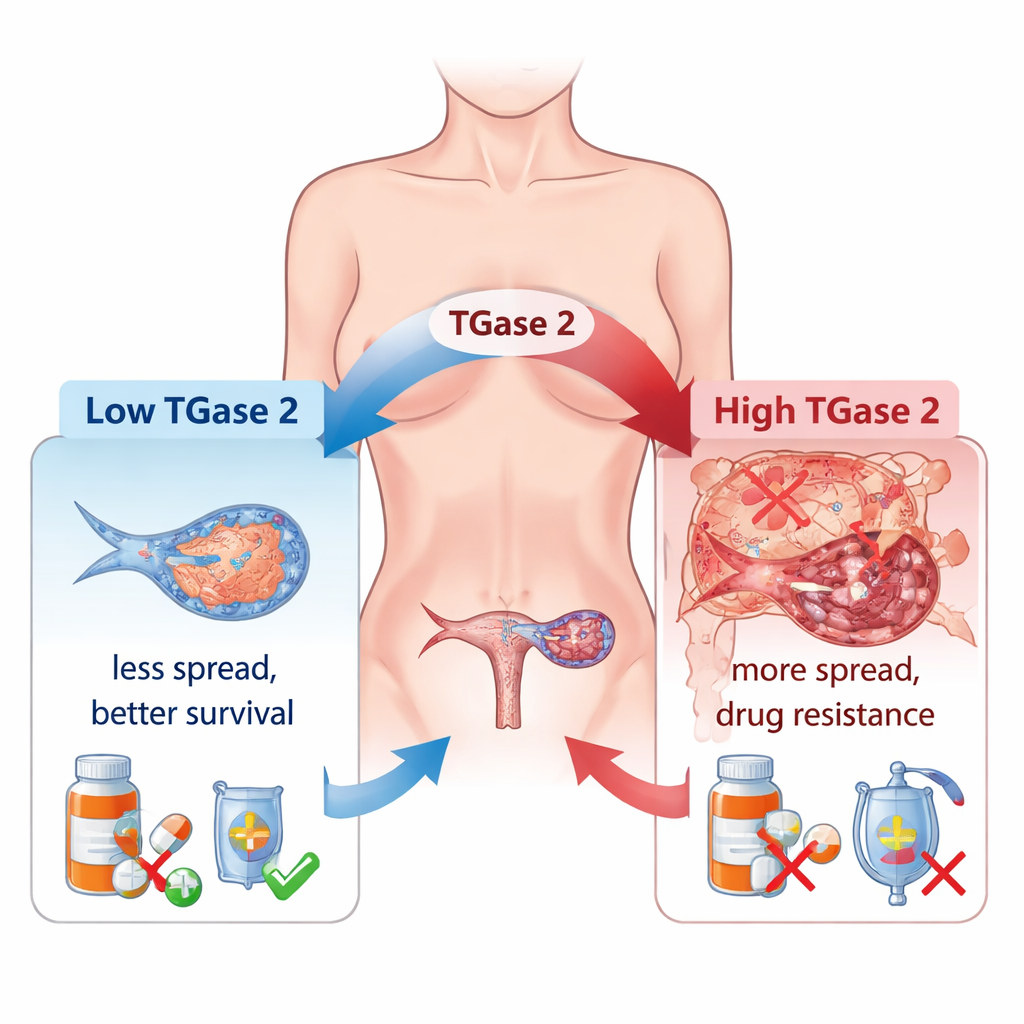
Comment la TGase 2 coupe un interrupteur de sécurité clé
Pour comprendre ce que fait réellement la TGase 2 dans les cellules cancéreuses, les chercheurs se sont concentrés sur sa relation avec une autre protéine, GSK3β. Dans des conditions saines, GSK3β agit comme un frein à l’invasion : il maintient de faibles niveaux d’une molécule de signalisation appelée β-caténine, ce qui restreint les gènes qui favorisent l’EMT. L’équipe a découvert que la TGase 2 se lie physiquement à GSK3β et affaiblit son activité tout en favorisant son élimination via le système de recyclage cellulaire, une voie appelée autophagie. Quand la TGase 2 était abondante, les cellules de cancer ovarien migraient plus facilement et présentaient des niveaux plus élevés de marqueurs classiques de l’EMT tels que la fibronectine, la vimentine et la β-caténine. Lorsque les chercheurs ont réduit la TGase 2 par des outils génétiques, ces caractéristiques invasives ont diminué et la signalisation par β-caténine a été atténuée, montrant que la TGase 2 neutralise un interrupteur de sécurité crucial contre les métastases.
Des cellules cancéreuses aux animaux vivants
Les auteurs ont ensuite demandé si bloquer la TGase 2 pouvait effectivement ralentir le cancer chez l’animal. Ils ont modifié des cellules de cancer ovarien pour supprimer le gène TGase 2 et les ont implantées chez des souris. Par rapport aux souris ayant reçu des cellules cancéreuses normales, les animaux recevant des cellules déficientes en TGase 2 développaient une charge tumorale plus faible et vivaient plus longtemps. Dans un modèle distinct reproduisant la dissémination par la circulation sanguine, les souris injectées avec des cellules déficientes en TGase 2 ont développé beaucoup moins de métastases pulmonaires, et celles-ci étaient plus petites. Fait important, ces foyers métastatiques présentaient des niveaux plus élevés de GSK3β, ce qui s’accorde avec l’idée que la suppression de la TGase 2 restaure le frein naturel à l’invasion et contribue à contenir la maladie.
Transformer une piste de laboratoire en stratégie médicamenteuse
Comme supprimer un gène n’est pas praticable chez les patients, les auteurs ont testé une petite molécule appelée streptonigrine, connue pour se lier à la même extrémité de la TGase 2 utilisée pour capturer d’autres protéines. Ils ont constaté que la streptonigrine pouvait perturber l’interaction TGase 2–GSK3β dans les cellules, réduire leur colocalisation et limiter la migration des cellules cancéreuses. Dans des modèles murins du cancer ovarien, un traitement oral par streptonigrine ralentissait la croissance tumorale, réduisait les lésions métastatiques et prolongeait la survie. Plus frappant encore, lorsque la streptonigrine était combinée aux chimiothérapies classiques telles que le cisplatine ou le paclitaxel, les souris vivaient des semaines de plus que sous chimiothérapie seule. La chimiothérapie seule avait tendance à augmenter les niveaux de TGase 2 et à diminuer GSK3β, poussant indirectement les cellules vers l’EMT, mais l’ajout de l’inhibiteur de TGase 2 inversait cette tendance et freinait la nouvelle mobilité des cellules. 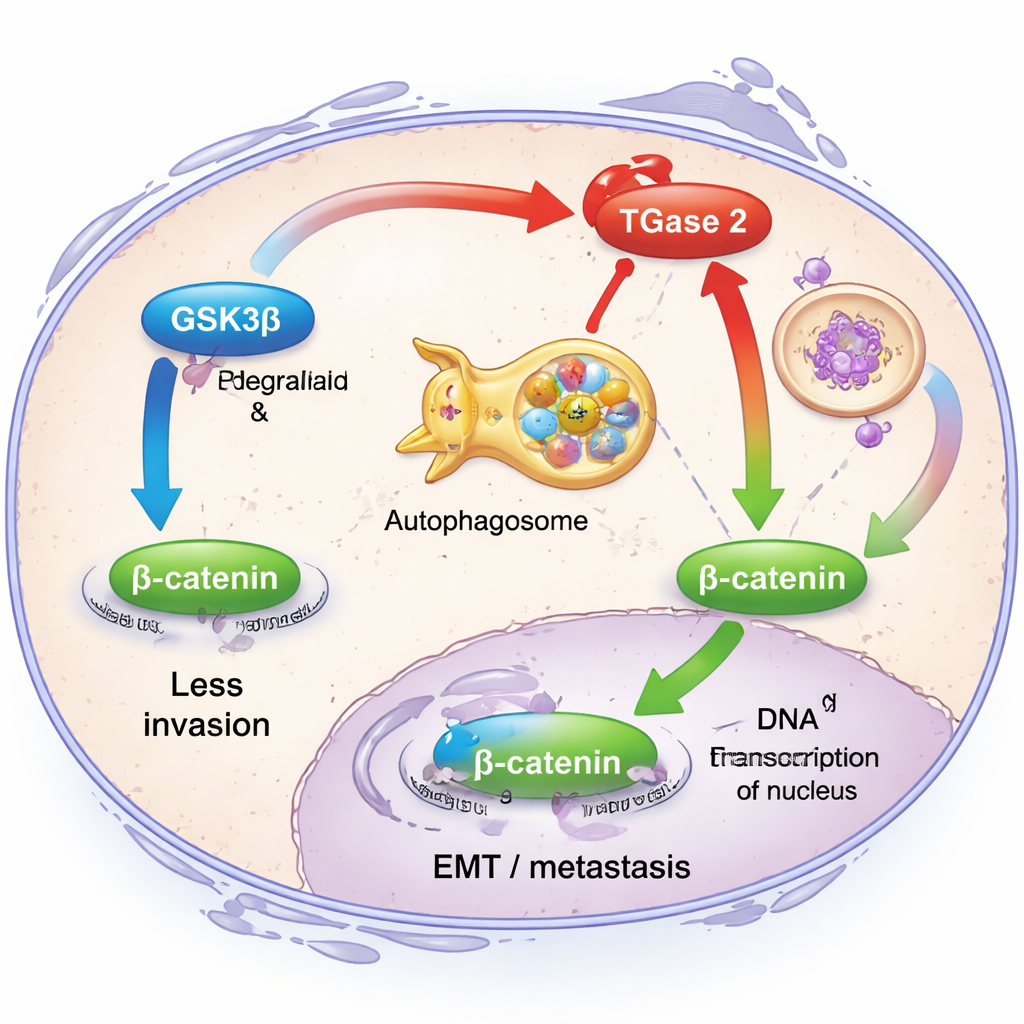
Ce que cela pourrait signifier pour les traitements futurs
Pour un public non spécialiste, le message principal est que les cellules du cancer ovarien exploitent la TGase 2 pour désactiver un frein anti-métastatique intrinsèque et pour résister aux effets de la chimiothérapie. En inactivant directement GSK3β et en stabilisant la β-caténine, la TGase 2 rend les tumeurs plus invasives et résistantes aux médicaments. Ce travail suggère que des médicaments visant la région N-terminale de la TGase 2—comme la streptonigrine ou de futures molécules plus sûres s’en inspirant—pourraient améliorer l’efficacité des chimiothérapies existantes, réduire le risque de rechute et améliorer la survie. En termes simples, cibler la TGase 2 pourrait fermer une « voie d’évasion » du cancer, rendant les tumeurs ovariennes plus sensibles au traitement et moins aptes à se propager.
Citation: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Mots-clés: cancer ovarien, résistance aux médicaments, métastase, transition épithélio-mésenchymateuse, thérapie ciblée